- Definición de cromatografía
- ¿Qué es una fase estacionaria?
- ¿Qué es la fase móvil?
- 2. Cromatografía de intercambio aniónico
-
3. Cromatografía de intercambio catiónico
- Principio de la cromatografía de intercambio catiónico
- Pasos de la cromatografía de intercambio catiónico
- Usos de la cromatografía de intercambio catiónico
- Ejemplos de cromatografía de intercambio catiónico
- Principio de la cromatografía en columna
- Pasos de la cromatografía en columna
- Usos de la cromatografía en columna
- Ejemplos de cromatografía en columna
-
5. Cromatografía flash
- Principio de la cromatografía flash
- Pasos de la cromatografía flash
- Usos de la cromatografía flash
- Principio de la cromatografía de gases
- Pasos de la cromatografía de gases
- Usos de la cromatografía de gases
- Ejemplos de cromatografía de gases
- Principio
- Pasos
- Utiliza
- Ejemplos
- Principio de la HPLC
- Pasos de la HPLC
- Usos de la HPLC
- Ejemplo de HPLC
-
9. Cromatografía de interacción hidrofóbica
- Principio de la cromatografía de interacción hidrofóbica
- Pasos de la cromatografía de interacción hidrofóbica
- Usos de la cromatografía de interacción hidrofóbica
- Ejemplo de cromatografía de interacción hidrofóbica
- Principio de la cromatografía de intercambio iónico
- Pasos de la cromatografía de intercambio iónico
- Usos de la cromatografía de intercambio iónico
- Ejemplos de cromatografía de intercambio iónico
- 11. Cromatografía líquida
-
13. Cromatografía en fase inversa
- Principio de la cromatografía en fase inversa
- Pasos de la cromatografía en fase inversa
- Usos de la cromatografía de fase inversa
- Ejemplos de cromatografía en fase inversa
- Principio de la cromatografía en capa fina (TLC)
- Pasos de la cromatografía en capa fina (TLC)
- Usos de la cromatografía en capa fina (TLC)
- Referencias
- Fuentes
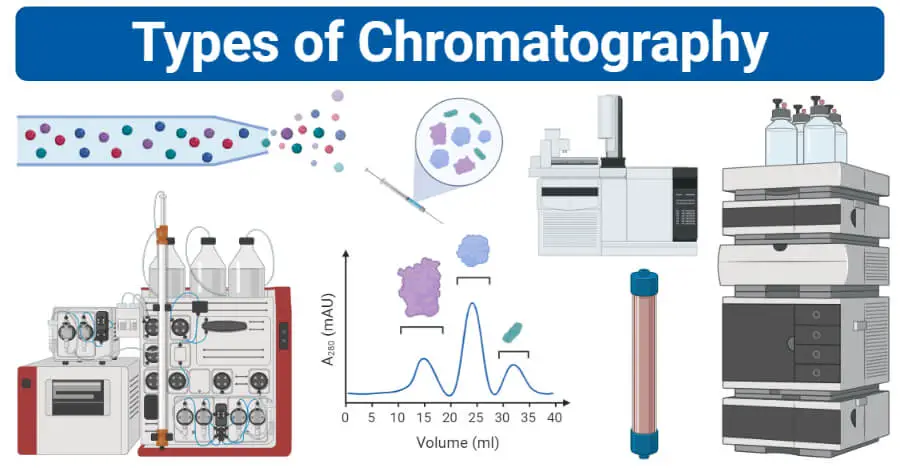
Definición de cromatografía
La cromatografía es una importante técnica biofísica que permite la separación, identificación y purificación de los componentes de una mezcla para su análisis cualitativo y cuantitativo.
- Una amplia gama de procedimientos cromatográficos utiliza las diferencias de tamaño, afinidades de unión, carga y otras propiedades para separar materiales.
- Es una poderosa herramienta de separación que se utiliza en todas las ramas de la ciencia y a menudo es el único medio de separar componentes de mezclas complejas.
- La cromatografía es una técnica muy útil, ya que permite separar los componentes de una mezcla en función de su naturaleza, estructura, tamaño y otras propiedades.
- La cromatografía, en general, se basa en el principio de que los componentes de una mezcla se separan cuando la mezcla añadida a una fase móvil se mueve a través de una fase estacionaria (que en su mayoría es una superficie sólida), lo que hace que algunos componentes de la mezcla se adhieran a la fase estacionaria. Al mismo tiempo, el resto pasa junto con la fase móvil.
- Por tanto, hay dos componentes esenciales en todas las técnicas de cromatografía.
¿Qué es una fase estacionaria?
La fase estacionaria en cromatografía es la fase que es una partícula sólida o líquida adherida a una superficie de vidrio o de metal en la que se absorben selectivamente los componentes de la mezcla que se quiere separar.
- El término estacionario se refiere al hecho de que esta fase permanece estacionaria mientras la otra fase se mueve.
- La mayoría de las sustancias utilizadas como fases estacionarias son porosas, lo que permite la fijación de los componentes durante la cromatografía.
- La fase estacionaria que debe seleccionarse para un proceso cromatográfico depende de la naturaleza de los componentes que deben separarse y del tipo de cromatografía.
- Según el tipo de cromatografía, se utilizan como fase estacionaria perlas de gel, papel fino y uniforme, sílice, vidrio, algunos gases o incluso componentes líquidos.
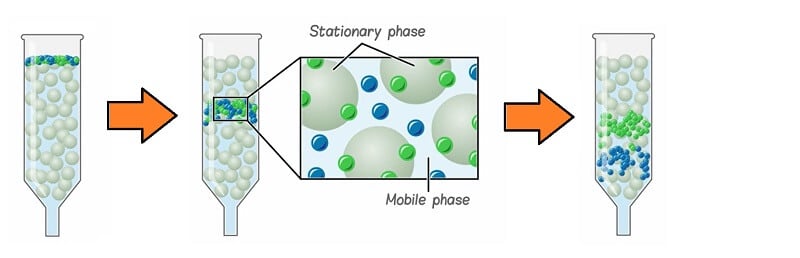
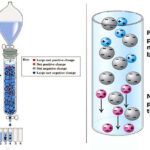 Cromatografía de intercambio iónico - Definición, principio, partes, pasos, usos
Cromatografía de intercambio iónico - Definición, principio, partes, pasos, usosFuente de la imagen: Diseñada por Cerotec Estudios.
¿Qué es la fase móvil?
La fase móvil en cromatografía es la fase líquida o gaseosa que se hace pasar por un sistema cromatográfico en el que los componentes de la mezcla se separan a diferentes ritmos mediante su adsorción a la fase estacionaria.
Lectura relacionada: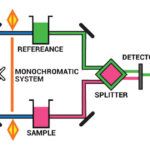 Espectroscopia de infrarrojos (IR) - Definición, principio, partes, usos
Espectroscopia de infrarrojos (IR) - Definición, principio, partes, usos- La fase móvil es el disolvente que transporta la mezcla al desplazarse por la fase estacionaria.
- El término móvil indica que la fase se desplaza por el sistema cromatográfico, mientras que la otra fase permanece estacionaria.
- Las sustancias utilizadas como fases móviles se seleccionan para un proceso cromatográfico en función de la naturaleza de los componentes que se van a separar y del tipo de cromatografía.
- El alcohol, el agua, el ácido acético, la acetona o algunos gases son las fases móviles más utilizadas en diferentes técnicas cromatográficas.
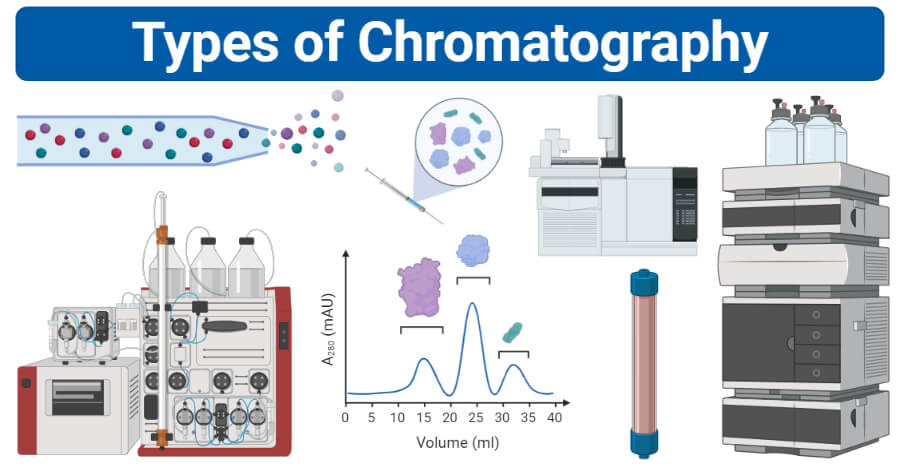
Tipos de cromatografía
La cromatografía de afinidad es una técnica de separación en la que los componentes de una mezcla se separan en función de su afinidad hacia la fase estacionaria del sistema.
Principio de la cromatografía de afinidad
- Esta técnica de cromatografía se basa en el principio de que los componentes de una mezcla se separan cuando el elemento que tiene afinidad hacia la fase estacionaria se une a ella. En cambio, los demás componentes se eluyen con la fase móvil.
- El sustrato/ligando se une a la fase estacionaria para que queden expuestos los sitios reactivos para la unión de los componentes.
- Ahora, la mezcla se hace pasar por la fase móvil, donde los componentes con sitios de unión al sustrato se unen al sustrato en la fase estacionaria, mientras que el resto de los componentes se eluyen con la fase móvil.
- Los componentes unidos a la fase estacionaria se eluyen entonces cambiando el pH, la fuerza iónica u otras condiciones.
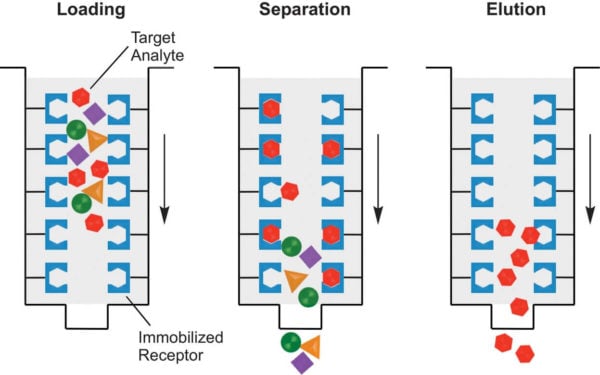
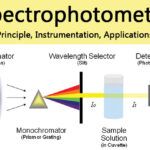 Espectrofotómetro - Principio, Instrumentación, Aplicaciones
Espectrofotómetro - Principio, Instrumentación, AplicacionesFigura: Cromatografía de afinidad. Fuente de la imagen: Creative Biostructure.
Pasos de la cromatografía de afinidad
- La columna se prepara cargándola con un soporte sólido como la agarosa o la celulosa, sobre el que se fija el sustrato/ligando con el brazo espaciador.
- La fase móvil que contiene la mezcla se vierte en la columna a un ritmo constante.
- Una vez completado el proceso, el complejo ligando-molécula se eluye de la fase estacionaria cambiando las condiciones que favorecen la separación del ligando y los componentes de la mezcla.
Usos de la cromatografía de afinidad
- La cromatografía de afinidad se utiliza como técnica de separación básica de enzimas y otras proteínas.
- Este principio también se aplica en las reacciones antígeno-anticuerpo in vitro.
- Esta técnica se utiliza para la separación de componentes, así como para la eliminación de impurezas de una mezcla.
- La cromatografía de afinidad puede utilizarse en la detección de mutaciones y polimorfismos de nucleótidos en ácidos nucleicos.
Ejemplos de cromatografía de afinidad
- La purificación de la β-galactosidasa de coli a partir de una mezcla de proteínas utilizando la agarosa p-aminofenil-1-β-D-galactopiranosil como matriz de afinidad.
- La eliminación del exceso de albúmina y α2-macroglobulina de la albúmina sérica.
2. Cromatografía de intercambio aniónico
La cromatografía de intercambio aniónico es la técnica de separación de moléculas cargadas negativamente por su interacción con la fase estacionaria cargada positivamente en forma de resina de intercambio iónico.
Principio de la cromatografía de intercambio aniónico
- Esta técnica se basa en el principio de atracción de la resina cargada positivamente y el analito cargado negativamente. Aquí se produce el intercambio de iones con carga positiva para eliminar las moléculas con carga negativa.
- Primero se recubre la fase estacionaria con cargas positivas, donde se unirán los componentes de la mezcla con cargas negativas.
- A continuación, una resina de intercambio aniónico con mayor afinidad por los componentes con carga negativa se une a los componentes, desplazando a la resina con carga positiva.
- A continuación, el complejo resina de intercambio aniónico-componente se elimina utilizando diferentes tampones.
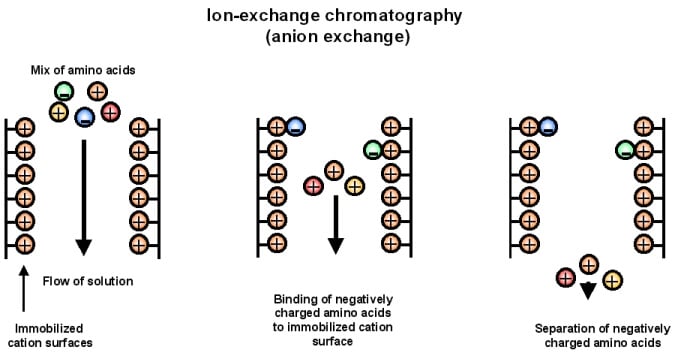
Figura: Cromatografía de intercambio aniónico. Fuente de la imagen: https://sites.google.com/site/chromospectrum/i-exchange
Pasos de la cromatografía de intercambio aniónico
- Se toma como fase estacionaria una columna empaquetada con resina cargada positivamente.
- La mezcla con las partículas cargadas se hace pasar por la columna, donde las moléculas cargadas negativamente se unen a las resinas cargadas positivamente.
- A continuación, la resina de intercambio aniónico se hace pasar por la columna, donde las moléculas cargadas negativamente se unen ahora a la resina de intercambio aniónico, desplazando a la resina cargada positivamente.
- Ahora se aplica un tampón adecuado a la columna para separar el complejo de resinas de intercambio aniónico y las moléculas cargadas.
Usos de la cromatografía de intercambio aniónico
- La cromatografía de intercambio aniónico se utiliza para separar proteínas y aminoácidos de sus mezclas.
- Los ácidos nucleicos cargados negativamente pueden separarse, lo que ayuda a su posterior análisis.
- Este método también puede utilizarse para la purificación del agua, donde los aniones se intercambian por iones hidroxilo.
- Las resinas de intercambio aniónico pueden utilizarse para la separación de metales, ya que suelen tener complejos cargados negativamente que se unen a los intercambiadores de aniones.
Ejemplos de cromatografía de intercambio aniónico
- La separación de ácidos nucleicos de una mezcla obtenida tras la destrucción de células.
- La separación de las proteínas de la mezcla cruda obtenida del suero sanguíneo.
3. Cromatografía de intercambio catiónico
La cromatografía de intercambio aniónico es la técnica de separación de moléculas cargadas positivamente por su interacción con la fase estacionaria cargada negativamente en forma de resina de intercambio iónico.
Principio de la cromatografía de intercambio catiónico
- Esta técnica se basa en el principio de atracción de la resina cargada negativamente y el analito cargado positivamente. Aquí se produce el intercambio de iones cargados negativamente para eliminar las moléculas cargadas positivamente.
- Primero se recubre la fase estacionaria con cargas negativas, donde se unirán los componentes de la mezcla con cargas positivas.
- A continuación, una resina de intercambio catiónico con mayor afinidad por los componentes con carga positiva se une a los componentes, desplazando a la resina con carga negativa.
- A continuación, el complejo resina de intercambio catiónico-componente se elimina utilizando diferentes tampones.
Pasos de la cromatografía de intercambio catiónico
- Se toma como fase estacionaria una columna empaquetada con resina cargada negativamente.
- La mezcla con las partículas cargadas se hace pasar por la columna, donde las moléculas cargadas positivamente se unen a las resinas cargadas negativamente.
- A continuación, se hace pasar la resina de intercambio catiónico por la columna, donde las moléculas cargadas positivamente se unen ahora a la resina de intercambio catiónico, desplazando a la resina cargada negativamente.
- Ahora se aplica un tampón adecuado a la columna para separar el complejo de resinas de intercambio catiónico y las moléculas cargadas.
Usos de la cromatografía de intercambio catiónico
- La cromatografía de intercambio catiónico se utiliza para el análisis de los productos obtenidos tras la hidrólisis de los ácidos nucleicos.
- También puede utilizarse para la separación de metales, donde los propios iones metálicos se unen a las resinas cargadas negativamente para eliminar los complejos cargados negativamente.
- La cromatografía de intercambio catiónico ayuda a purificar el agua intercambiando los iones cargados positivamente por los iones de hidrógeno.
- También se utiliza para analizar las rocas y otras moléculas inorgánicas.
Ejemplos de cromatografía de intercambio catiónico
- La separación de los iones lantanoides cargados positivamente que se obtienen de la corteza terrestre.
- La determinación de las sales totales disueltas en las aguas naturales mediante el análisis de la presencia de iones de calcio.
La cromatografía en columna es la técnica de separación en la que los componentes de una mezcla se separan en función de su adsorción diferencial con la fase estacionaria, lo que hace que se muevan a diferentes velocidades al pasar por una columna.
Es una técnica de cromatografía sólido-líquido en la que la fase estacionaria es un sólido y la fase móvil es un líquido o un gas.
Principio de la cromatografía en columna
- Esta técnica se basa en el principio de la adsorción diferencial, según el cual las diferentes moléculas de una mezcla tienen diferentes afinidades con el absorbente presente en la fase estacionaria.
- Las moléculas con mayor afinidad permanecen adsorbidas durante más tiempo, lo que disminuye su velocidad de movimiento a través de la columna.
- Sin embargo, las moléculas con menor afinidad se mueven con mayor rapidez, lo que permite separar las moléculas en fracciones diferentes.
- En este caso, la fase estacionaria en la cromatografía en columna, también denominada absorbente, es un sólido (principalmente sílice) y la fase móvil es un líquido que permite que las moléculas se muevan a través de la columna suavemente.
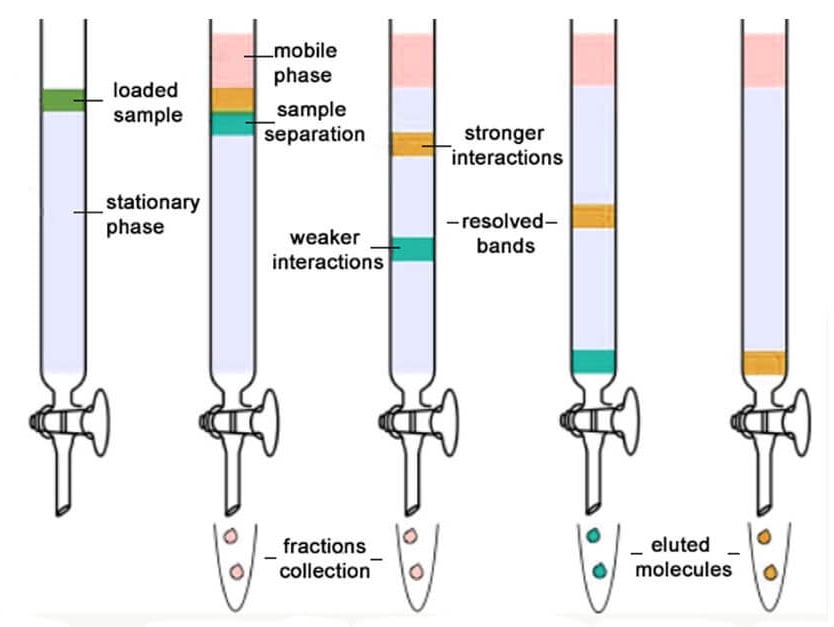
Figura: Cromatografía en columna. Fuente de la imagen: PrepGenie.
Pasos de la cromatografía en columna
- La columna se prepara tomando un tubo de vidrio que se seca y se recubre con una capa fina y uniforme de fase estacionaria (celulosa, sílice).
- A continuación se prepara la muestra añadiendo la mezcla a la fase móvil. La muestra se introduce en la columna por la parte superior y se deja pasar la muestra bajo la influencia de la gravedad.
- Las moléculas unidas a la columna se separan mediante una técnica de elución en la que se utiliza una solución de la misma polaridad (técnica isocrática), o bien se utilizan diferentes muestras con polaridades distintas (técnica de gradiente).
- Las moléculas separadas pueden analizarse posteriormente con diversos fines.
Usos de la cromatografía en columna
- La cromatografía en columna se utiliza habitualmente para la separación de impurezas y la purificación de diversas mezclas biológicas.
- Esta técnica también puede utilizarse para el aislamiento de moléculas activas y metabolitos de diversas muestras.
- La cromatografía en columna se utiliza cada vez más para la detección de fármacos en extractos crudos.
Ejemplos de cromatografía en columna
- Extracción de pesticidas de muestras de alimentos sólidos de origen animal que contienen lípidos, ceras y pigmentos.
- Síntesis de la Pramlintida, que es un análogo de la Amilina, una hormona peptídica, para tratar diabéticos de tipo 1 y 2.
- Purificación de glicolípidos bioactivos, que muestran actividad antiviral frente al VHS-1 (Virus del Herpes).
5. Cromatografía flash
La cromatografía flash es una técnica de separación en la que se utilizan partículas de gel de menor tamaño como fase estacionaria, y se utiliza gas a presión para impulsar el disolvente a través de la columna.
Principio de la cromatografía flash
- El principio de la cromatografía flash es similar al de la cromatografía en columna, donde los componentes se separan en función de su adsorción diferencial a la fase estacionaria.
- La muestra aplicada se pasa utilizando un gas presurizado que hace que el proceso sea más rápido y eficaz.
- Las moléculas se unen a la fase estacionaria en función de su afinidad, mientras que el resto del disolvente se eluye aplicando el gas a presión, lo que acelera el proceso.
- Aquí, la fase estacionaria es sólida, la fase móvil y la solución de elución son líquidas, y se utiliza un gas presurizado adicional.
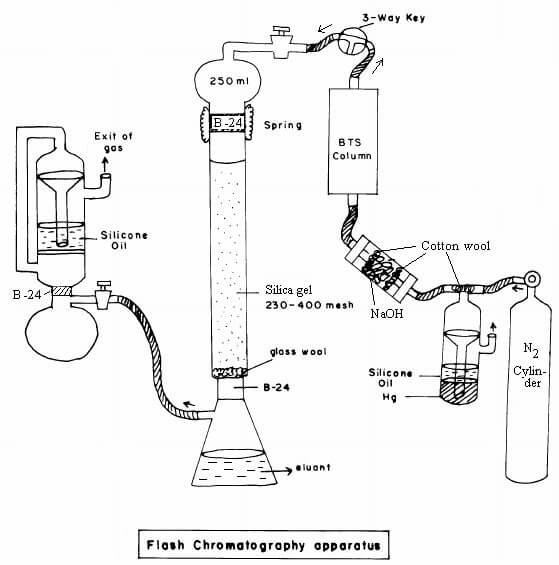
Figura: Cromatografía flash. Fuente de la imagen: Siddhartha S. Baisya (Research Gate)
Pasos de la cromatografía flash
- La columna se prepara tomando un tubo de vidrio que se seca y se recubre con una capa fina y uniforme de fase estacionaria (celulosa, sílice). El fondo y la parte superior de la columna se rellenan con algodón para evitar que el gel se escape.
- A continuación se prepara la muestra añadiendo la mezcla a la fase móvil. La muestra se introduce en la columna por la parte superior, y se utiliza una muestra bombeada para hacerla pasar a una velocidad constante.
- Las moléculas unidas a la columna se separan mediante una solución de elución en la que se utiliza una solución de la misma polaridad (técnica isocrática), o bien se utilizan muestras diferentes con polaridades distintas (técnica de gradiente).
- El disolvente de elución se aplica con una presión mínima constante necesaria para hacer descender el soluto por la columna.
- Las moléculas separadas pueden analizarse posteriormente con diversos fines.
Usos de la cromatografía flash
- La cromatografía flash se utiliza como método rápido y más eficaz de separación de los componentes de diferentes mezclas.
- Se utiliza para eliminar las impurezas de los extractos crudos de mezclas naturales y sintéticas.
La cromatografía de gases es una técnica de separación en la que las moléculas se separan en función de su tiempo de retención, según la afinidad de las moléculas a la fase estacionaria.
La muestra es un líquido o un gas que se vaporiza en el punto de inyección.
Principio de la cromatografía de gases
- La cromatografía de gases se basa en el principio de que los componentes que tienen una mayor afinidad con la fase estacionaria tienen un mayor tiempo de retención, ya que tardan más en salir de la columna.
- Sin embargo, los componentes que tienen una mayor afinidad con la fase estacionaria tienen un menor tiempo de retención, ya que se mueven junto con la fase móvil.
- La fase móvil es un gas, principalmente helio, que transporta la muestra a través de la columna.
- La muestra, una vez inyectada en la fase de vapor, se hace pasar por un detector para determinar el tiempo de retención.
- Los componentes se recogen por separado a medida que salen de la fase estacionaria en diferentes momentos.
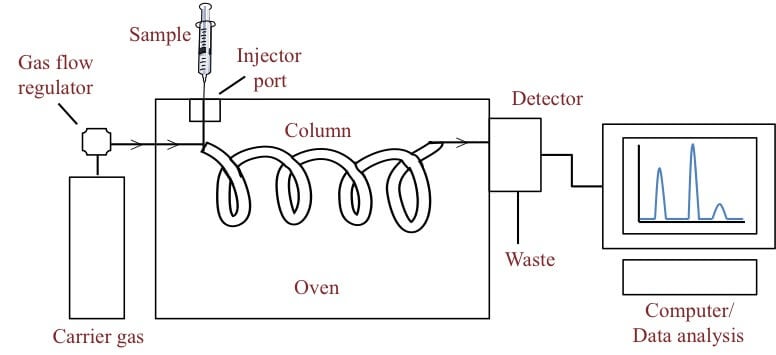
Figura: Cromatografía de gases. Fuente de la imagen: Bitesize Bio.
Pasos de la cromatografía de gases
- La muestra se inyecta en la columna, donde se vaporiza en estado gaseoso. El componente vaporizado se mezcla entonces con la fase móvil para ser transportado por el resto de la columna.
- La columna se coloca con la fase estacionaria, donde las moléculas se separan en función de su afinidad a la fase estacionaria.
- Los componentes de la mezcla llegan al detector en momentos diferentes debido a las diferencias en el tiempo que permanecen en la columna.
Usos de la cromatografía de gases
- Esta técnica se utiliza para calcular la concentración de diferentes sustancias químicas en diversas muestras.
- Se utiliza en el análisis de contaminantes atmosféricos, vertidos de petróleo y otras muestras.
- La cromatografía de gases también puede utilizarse en la ciencia forense para identificar y cuantificar diversas muestras biológicas encontradas en la escena del crimen.
Ejemplos de cromatografía de gases
- La identificación de la droga inductora del rendimiento en la orina del deportista.
- La separación y cuantificación de una droga sólida en muestras de suelo y agua.
La cromatografía de filtración en gel es una forma de cromatografía de partición utilizada para separar moléculas de diferentes tamaños moleculares.
Esta técnica también ha recibido otros nombres, como permeación en gel, exclusión en gel, exclusión por tamaño y cromatografía de tamiz molecular.
Principio
- Las moléculas se reparten entre una fase móvil y una fase estacionaria en función de sus tamaños relativos.
- La fase estacionaria es una matriz de polímero poroso que tiene poros de tamaños específicos.
- Cuando se inyecta la muestra con la fase móvil, ésta ocupa los poros de la fase estacionaria.
- Si el tamaño de las moléculas es lo suficientemente adecuado para entrar en los poros, permanecen en ellos parcial o totalmente.
- Sin embargo, las moléculas de mayor tamaño son retenidas para que no entren en los poros, lo que hace que se desplacen con la fase móvil, fuera de la columna.
- Si la fase móvil utilizada es una solución acuosa, el proceso se denomina cromatografía de filtración en gel.
- Si la fase móvil utilizada es un disolvente orgánico, se denomina cromatografía de permeación en gel.
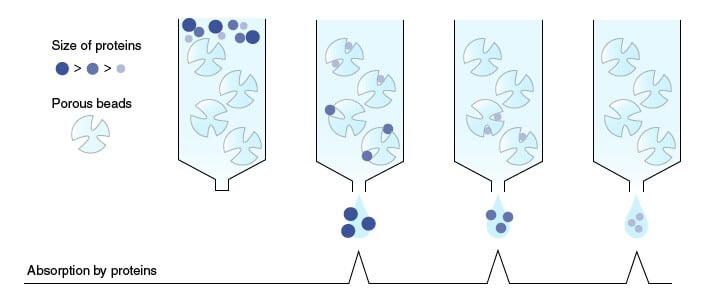
Figura: Cromatografía de filtración en gel. Fuente de la imagen: MBL Life Science.
Pasos
- La columna se rellena con perlas de gel polimérico semipermeables y porosas con un rango bien definido de tamaños de poros.
- La muestra, mezclada con la fase móvil, se inyecta en la columna desde la parte superior de la misma.
- Las moléculas unidas a la columna se separan mediante una solución de elución en la que se utiliza una solución de la misma polaridad (técnica isocrática), o bien se utilizan muestras diferentes con polaridades distintas (técnica de gradiente).
- Se pueden seleccionar las condiciones de elución (pH, iones esenciales, cofactores, inhibidores de la proteasa, etc.), que complementarán los requisitos de la molécula de interés.
Utiliza
- Una de las principales ventajas de la cromatografía de filtración en gel es que la separación puede realizarse en condiciones específicamente diseñadas para mantener la estabilidad y la actividad de la molécula de interés sin comprometer la resolución.
- La ausencia de un paso de unión entre la molécula y la matriz también evita daños innecesarios a las moléculas frágiles, lo que garantiza que las separaciones por filtración en gel suelen dar altas recuperaciones de actividad.
- Debido a su modo único de separación, la cromatografía de filtración en gel se ha utilizado con éxito en la purificación de proteínas y péptidos de diversas fuentes.
- La cromatografía de filtración en gel se ha utilizado para separar varias especies de ácidos nucleicos, como el ADN, el ARN y el ARNt, así como sus bases constitutivas, adenina, guanina, timina, citosina y uracilo.
Ejemplos
- Separación del factor estimulante de colonias de granulocitos humano recombinante (rhG-CSF) de los cuerpos de inclusión en alto rendimiento mediante cromatografía de exclusión por tamaño en gradiente de urea.
- La separación de la lisozima de huevo de gallina utilizando columnas de gel a base de acrilamida y dextrano.
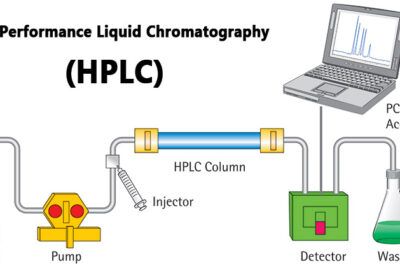
La cromatografía líquida de alto rendimiento es una forma modificada de cromatografía en columna en la que los componentes de una mezcla se separan en función de su afinidad con la fase estacionaria.
Principio de la HPLC
- Esta técnica se basa en el principio de la adsorción diferencial, según el cual las diferentes moléculas de una mezcla tienen un grado de interacción variable con el absorbente presente en la fase estacionaria.
- Las moléculas con mayor afinidad permanecen adsorbidas durante más tiempo, lo que disminuye su velocidad de movimiento a través de la columna.
- Sin embargo, las moléculas con menor afinidad se mueven con mayor rapidez, lo que permite separar las moléculas en fracciones diferentes.
- Este proceso es ligeramente diferente al de la cromatografía en columna, ya que en este caso, el disolvente es forzado bajo altas presiones de hasta 400 atmósferas en lugar de dejarlo caer por gravedad.
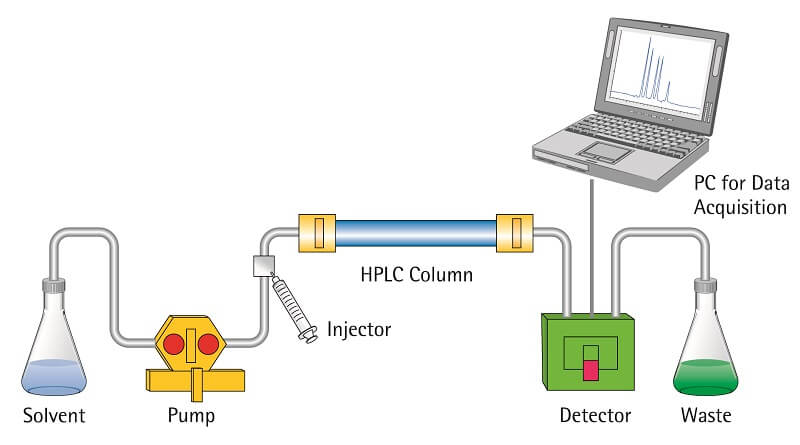
Figura: Cromatografía líquida de alto rendimiento (HPLC). Fuente de la imagen: Toppr.
Pasos de la HPLC
- La columna se prepara tomando un tubo de vidrio que se seca y se recubre con una capa fina y uniforme de fase estacionaria (celulosa, sílice).
- A continuación se prepara la muestra añadiendo la mezcla a la fase móvil. La muestra se introduce en la columna por la parte superior, y se utiliza una bomba de alta presión para hacer pasar la muestra a un ritmo constante.
- A continuación, la fase móvil desciende hasta un detector que detecta las moléculas a una determinada longitud de onda de absorción.
- Las moléculas separadas pueden analizarse posteriormente con diversos fines.
Usos de la HPLC
- La cromatografía líquida de alto rendimiento se utiliza en el análisis de los contaminantes presentes en las muestras ambientales.
- Se realiza para mantener la pureza del producto y el control de calidad de diversas producciones industriales.
- Esta técnica también puede utilizarse para separar diferentes moléculas biológicas, como las proteínas y los ácidos nucleicos.
- La mayor velocidad de esta técnica hace que el proceso sea más rápido y eficaz.
Ejemplo de HPLC
- Se ha realizado una cromatografía líquida de alto rendimiento para comprobar la eficacia de diferentes anticuerpos contra enfermedades como el ébola.
9. Cromatografía de interacción hidrofóbica
La cromatografía de interacción hidrofóbica es la técnica de separación que separa las moléculas en función de su grado de hidrofobicidad.
Principio de la cromatografía de interacción hidrofóbica
- El principio de la cromatografía de interacción hidrofóbica se basa en la interacción entre dos moléculas con grupos hidrofóbicos.
- Aquí, la fase estacionaria es un soporte sólido aplicado con grupos hidrofóbicos e hidrofílicos.
- Las moléculas de disolvente que contienen regiones hidrofóbicas interactúan con los grupos hidrofóbicos, separándolas así de las moléculas con grupos hidrofílicos.
- A continuación se invierte la interacción aplicando una solución de elución con gradiente salino decreciente, lo que hace que las moléculas con grupos hidrofóbicos se separen de la fase estacionaria.
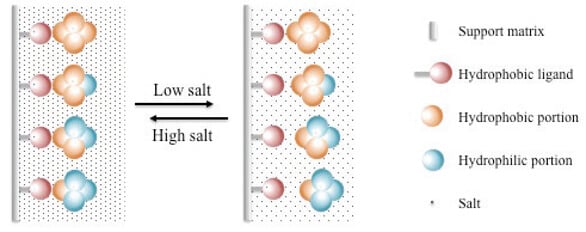
Figura: Cromatografía de interacción hidrofóbica. Fuente de la imagen: American Pharmaceutical Review.
Pasos de la cromatografía de interacción hidrofóbica
- La columna se prepara con un tubo de vidrio al que se le aplica un soporte sólido como el gel de sílice, sobre el que se adhieren grupos hidrófobos como el fenilo o el butilo.
- La muestra se prepara añadiendo la mezcla a la fase móvil.
- A continuación, se inyecta la muestra en la columna desde la parte superior de la misma.
- Las moléculas con grupos hidrofóbicos forman una interacción con los grupos hidrofóbicos de la fase estacionaria. En cambio, las moléculas sin dichos grupos salen de la columna con la fase móvil.
- A continuación, se hace pasar por la columna una solución de elución particular con un gradiente salino decreciente que elimina las moléculas unidas a la fase estacionaria.
Usos de la cromatografía de interacción hidrofóbica
- La cromatografía de interacción hidrofóbica es muy importante para la separación de proteínas con grupos hidrofóbicos.
- Esta técnica es más adecuada que otros métodos, ya que esta técnica da lugar a actividades de desnaturalización mínimas.
- Del mismo modo, este método también puede aplicarse a la separación de otros compuestos orgánicos con grupos hidrofóbicos.
- Esto permite la separación de moléculas biológicas hidrofílicas e hidrofóbicas entre sí.
Ejemplo de cromatografía de interacción hidrofóbica
- La separación de las proteínas vegetales de los extractos crudos.
La cromatografía de intercambio iónico es la técnica de separación de moléculas cargadas por su interacción con la fase estacionaria de carga opuesta en forma de resina de intercambio iónico.
Principio de la cromatografía de intercambio iónico
- Esta técnica se basa en el principio de atracción de la resina cargada y el analito con carga opuesta. Aquí se produce el intercambio de iones con carga negativa/positiva para eliminar las moléculas cargadas.
- Primero se recubre la fase estacionaria con cargas particulares donde se unirán los componentes de la mezcla con cargas opuestas.
- A continuación, una resina de intercambio catiónico o aniónico con mayor afinidad por los componentes cargados se une a los componentes, desplazando a la resina de carga opuesta.
- A continuación, el complejo resina de intercambio catiónico o aniónico-componente se elimina utilizando diferentes tampones.
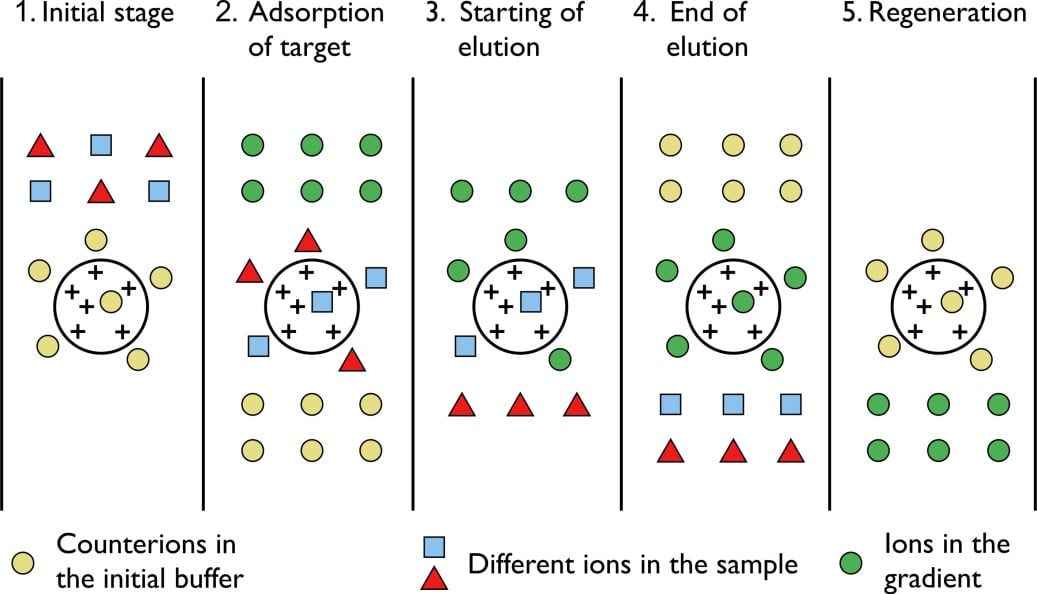
Figura: Cromatografía de intercambio iónico.
Pasos de la cromatografía de intercambio iónico
- Se toma como fase estacionaria una columna empaquetada con resina cargada que puede estar cargada positiva o negativamente.
- La mezcla con las partículas cargadas se hace pasar por la columna, donde las moléculas cargadas se unen a las resinas de carga opuesta.
- Si se utiliza una resina de intercambio catiónico, las moléculas cargadas positivamente se unen ahora a la resina de intercambio catiónico desplazando a la resina cargada negativamente.
- Del mismo modo, si se utiliza una resina de intercambio aniónico, las moléculas cargadas negativamente se unen a la resina de intercambio aniónico desplazando a la resina cargada positivamente.
- Ahora se aplica un tampón adecuado a la columna para separar el complejo de resinas de intercambio cargadas y las moléculas cargadas.
Usos de la cromatografía de intercambio iónico
- La cromatografía de intercambio iónico se utiliza en la purificación del agua, donde los iones con carga positiva se sustituyen por iones de hidrógeno, y los iones con carga negativa se sustituyen por iones de hidroxilo.
- Este método también funciona como un método eficaz para el análisis de los productos formados tras la hidrólisis de los ácidos nucleicos.
- La cromatografía de intercambio iónico también facilita la separación de metales y otros compuestos inorgánicos.
Ejemplos de cromatografía de intercambio iónico
- La separación de los iones lantanoides cargados positivamente que se obtienen de la corteza terrestre.
- La separación de las proteínas de la mezcla bruta obtenida del suero sanguíneo.
11. Cromatografía líquida
La cromatografía líquida es una técnica de separación en la que la fase móvil utilizada es líquida, y la separación puede tener lugar en una columna o en una superficie plana.
Principio de la cromatografía líquida
- El proceso de cromatografía líquida se basa en el principio de afinidad de las moléculas a la fase móvil.
- Si los componentes a separar tienen una mayor afinidad con la fase móvil, las moléculas se mueven junto con la fase móvil y salen más rápidamente de la columna.
- En cambio, si los componentes tienen un menor grado de interacción con la fase móvil, las moléculas se mueven lentamente y, por tanto, salen más tarde de la columna.
- Así, si dos moléculas de una mezcla tienen polaridades diferentes y la fase móvil es de una polaridad distinta, las dos moléculas se moverán a velocidades diferentes a través de la fase estacionaria.
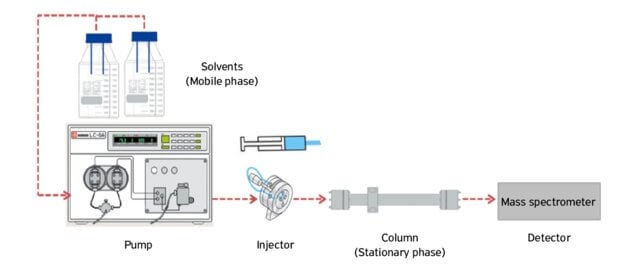
Figura: Cromatografía líquida. Fuente de la imagen: Vânia Margaret Flosi Paschoalin (Researchgate).
Pasos de la cromatografía líquida
- Se prepara la columna o papel donde se aplica la fase estacionaria (celulosa o sílice) sobre el soporte sólido.
- La muestra se añade a la fase móvil líquida, que se inyecta en el sistema cromatográfico.
- La fase móvil se mueve a través de la fase estacionaria antes de salir de la columna o del borde del papel.
- Se aplica una solución de elución al sistema para separar las moléculas de la fase estacionaria.
Usos de la cromatografía líquida
- La cromatografía líquida es un método eficaz para la separación de una solución coloreada, ya que tras la separación forman dos bandas separadas.
- Este método también puede utilizarse por encima de otras técnicas, ya que es bastante sencillo y menos costoso.
- Puede utilizarse para la separación de moléculas sólidas insolubles en agua.
Ejemplos de cromatografía líquida
- La cromatografía líquida de alto rendimiento es una forma modificada de cromatografía líquida que se utiliza en la investigación de moléculas biológicas.
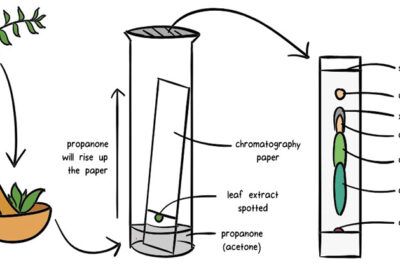
La cromatografía en papel es una técnica de separación en la que la separación se realiza en un papel especializado.
Principio de la cromatografía en papel
- La cromatografía en papel es de dos tipos basados en dos principios diferentes.
- El primero es la cromatografía de adsorción en papel que se basa en el grado variable de interacción entre las moléculas y la fase estacionaria.
- Las moléculas con mayor afinidad permanecen adsorbidas durante más tiempo, lo que disminuye su velocidad de movimiento a través de la columna.
- Sin embargo, las moléculas con menor afinidad se mueven con mayor rapidez, lo que permite separar las moléculas en fracciones diferentes.
- El segundo tipo de cromatografía de papel es la cromatografía de partición de papel. Se basa en el principio de que la humedad del papel de celulosa actúa como fase estacionaria para las moléculas que se mueven con la fase móvil.
- La separación de las moléculas se basa, por tanto, en la fuerza con la que se adsorben en la fase estacionaria.
- Durante la separación de las moléculas en la cromatografía de papel se aplica un concepto adicional de "factor de retención".
- El valor de retención de una molécula se determina como una relación entre la distancia recorrida por la molécula y la distancia recorrida por la fase móvil.
- El valor de retención de distintas moléculas puede utilizarse para diferenciarlas.
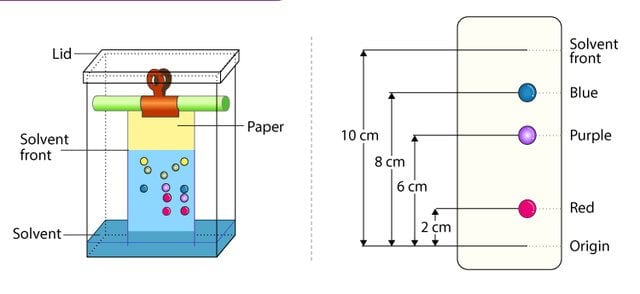
Figura: Cromatografía en papel. Fuente de la imagen: Enyoh Christian Ebere (Researchgate).
Pasos de la cromatografía de papel
- La fase estacionaria se selecciona como papel celulósico de calidad fina.
- Se toman como fase móvil diferentes combinaciones de disolventes orgánicos e inorgánicos.
- Se inyectan unos 2-200 µl de la solución de la muestra en la línea de base del papel, y se deja secar al aire.
- A continuación, el papel cargado con la muestra se sumerge cuidadosamente en la fase móvil a una altura no superior a 1 cm.
- Cuando la fase móvil llega cerca del borde del papel, se saca el papel.
- Se calcula el factor de retención, y los componentes separados se detectan mediante diferentes técnicas.
Usos de la cromatografía de papel
- La cromatografía en papel se realiza para detectar la pureza de diversos productos farmacéuticos.
- También puede emplearse para detectar la contaminación en diversas muestras, como alimentos y bebidas.
- Este método también puede utilizarse para la separación de impurezas de diversos productos industriales.
- El análisis de las mezclas de reacción en los laboratorios químicos también se realiza mediante cromatografía de papel.
Ejemplos de cromatografía de papel
- La cromatografía de papel se utiliza en la separación de mezclas de tintas u otras bebidas coloreadas.
13. Cromatografía en fase inversa
La cromatografía en fase inversa es una técnica de cromatografía líquida en la que la separación de las moléculas se consigue mediante la interacción hidrofóbica entre la fase móvil líquida y la fase estacionaria.
Principio de la cromatografía en fase inversa
- El principio de la cromatografía en fase inversa se basa en la interacción entre dos moléculas con grupos hidrofóbicos.
- En este caso, la fase estacionaria es un soporte sólido aplicado con grupos hidrofóbicos e hidrofílicos.
- Las moléculas de disolvente que contienen regiones hidrofóbicas interactúan con los grupos hidrofóbicos, separándolas así de las moléculas con grupos hidrofílicos.
- A continuación se invierte la interacción aplicando una solución de elución con gradiente salino decreciente, lo que hace que las moléculas con grupos hidrofóbicos se separen de la fase estacionaria.
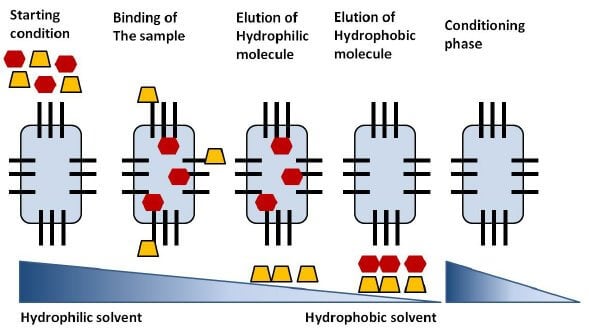
Figura: Pasos de una separación por cromatografía en fase inversa. Fuente de la imagen: Annette C Moser (Researchgate).
Pasos de la cromatografía en fase inversa
- La columna se prepara con un tubo de vidrio al que se le aplica un soporte sólido como el gel de sílice, sobre el que se adhieren grupos hidrófobos como el fenil, el butil, etc.
- La muestra se prepara añadiendo la mezcla a la fase móvil de disolventes orgánicos e inorgánicos.
- A continuación, se inyecta la muestra en la columna desde la parte superior de la misma.
- Las moléculas con grupos hidrofóbicos forman una interacción con los grupos hidrofóbicos de la fase estacionaria. En cambio, las moléculas sin dichos grupos salen de la columna con la fase móvil.
- A continuación, se hace pasar por la columna una solución de elución particular con un gradiente salino decreciente que elimina las moléculas unidas a la fase estacionaria.
Usos de la cromatografía de fase inversa
- La cromatografía inversa, en combinación con la cromatografía líquida de alto rendimiento, se utiliza cada vez más para la separación de biomoléculas.
- También se utiliza en el estudio del análisis de fármacos, metabolitos y moléculas activas.
- También puede utilizarse para eliminar impurezas de diversas muestras ambientales.
Ejemplos de cromatografía en fase inversa
- La cromatografía de interacción hidrofóbica es un ejemplo de cromatografía de fase inversa en la que se utiliza esta técnica para separar las proteínas de sus mezclas.
La cromatografía en capa fina es una técnica de separación en la que la fase estacionaria se aplica como una capa fina sobre una placa de soporte sólido con una fase móvil líquida.
Principio de la cromatografía en capa fina (TLC)
- Esta técnica de cromatografía se basa en el principio de que los componentes de una mezcla se separan cuando el componente que tiene afinidad por la fase estacionaria se une a ella. En cambio, los demás componentes se eluyen con la fase móvil.
- El sustrato/ligando se une a la fase estacionaria para que queden expuestos los sitios reactivos para la unión de los componentes.
- Ahora, la mezcla se hace pasar por la fase móvil, donde los componentes con sitios de unión al sustrato se unen al sustrato en la fase estacionaria, mientras que el resto de los componentes se eluyen con la fase móvil.
- Después de la separación, las moléculas se ven como manchas en un lugar diferente de la fase estacionaria.
- La detección de las moléculas se realiza mediante diversas técnicas.
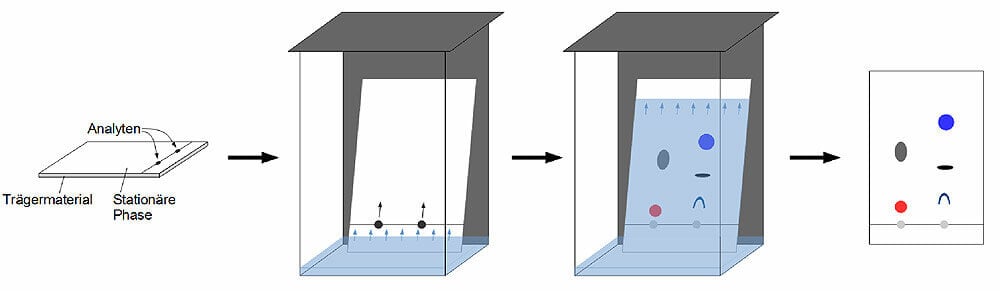
Figura: Cromatografía en capa fina (TLC). Fuente de la imagen: MZ-Analysentechnik GmbH.
Pasos de la cromatografía en capa fina (TLC)
- La fase estacionaria se aplica uniformemente sobre el soporte sólido (vidrio, placa fina o papel de aluminio) y se seca.
- La muestra se inyecta en forma de manchas sobre la fase estacionaria, aproximadamente a 1 cm por encima del borde de la placa.
- A continuación, la placa cargada con la muestra se sumerge cuidadosamente en la fase móvil a una altura no superior a 1 cm.
- Después de que la fase móvil llegue cerca del borde de la placa, se saca la placa.
- El factor de retención se calcula como en la cromatografía de papel, y los componentes separados se detectan mediante diferentes técnicas.
Usos de la cromatografía en capa fina (TLC)
- La cromatografía en capa fina se realiza de forma rutinaria en los laboratorios para identificar las diferentes sustancias presentes en una mezcla.
- Esta técnica ayuda en el análisis de fibras en la medicina forense.
- La TLC también permite ensayar diversos productos farmacéuticos.
- Ayuda a identificar las plantas medicinales y su composición.
Referencias
- Wilson, K., Walker, J. (2018). Principios y Técnicas de Bioquímica y Biología Molecular (8 eds.). Cambridge University Press: Nueva York.
- Ó'Fágáin, C., Cummins, P. M., & O'Connor, B. F. (2017). Cromatografía de filtración en gel. Methods in molecular biology (Clifton, N.J.), 1485, 15-25. https://doi.org/10.1007/978-1-4939-6412-3_2
Fuentes
- 3% – https://rd.springer.com/protocol/10.1007/978-1-4939-6412-3_2
- 1% - https://www.toppr.com/ask/question/chromatography-is-a-method-of-separation-which-works-on-the-principle-of/
- 1% - https://www.researchgate.net/publication/47556773_Hydrophobic_Interaction_Chromatography
- 1% - https://brainly.in/question/17535676
- 1% - https://answersdrive.com/what-is-the-stationary-phase-in-chromatography-73174
- <1% - https://www.workplacetesting.com/definition/1293/mobile-phase
- <1% - https://www.ukessays.com/essays/biology/the-separation-of-compounds-of-different-polarity-biology-essay.php
- <1% - https://www.thoughtco.com/gas-chromatography-4138098
- <1% - https://www.studyread.com/types-of-chromatography/
- <1% - https://www.studyread.com/chromatography-definition-principle-techniques/
- <1% - https://www.slideshare.net/shishirkawde/ion-exchange-chromatography
- <1% - https://www.slideshare.net/jabirrahaman/mobile-phase-in-chromatography
- <1% - https://www.slideshare.net/GamalAbdulHamid/high-performance-liquid-chromatograph-hplc
- <1% - https://www.slideshare.net/ajithnandanam/hydrophobic-interaction-chromatography-hic-theory-and-principle
- <1% - https://www.shimadzu.com/an/gc/support/fundamentals/gc.html
- <1% - https://www.sciencedirect.com/topics/neuroscience/chromatography
- <1% - https://www.sciencedirect.com/topics/materials-science/gel-permeation-chromatography
- <1% - https://www.sciencedirect.com/topics/earth-and-planetary-sciences/thin-layer-chromatography
- <1% - https://www.sciencedirect.com/topics/chemistry/reverse-phase-liquid-chromatography
- <1% - https://www.sciencedirect.com/topics/chemistry/mobile-phase-composition
- <1% - https://www.sciencedirect.com/topics/chemistry/liquid-liquid-chromatography
- <1% - https://www.sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/ion-exchange-chromatography
- <1% - https://www.sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/mobile-phase-composition
- <1% - https://www.sciencedirect.com/topics/agricultural-and-biological-sciences/anion-exchange-resins
- <1% - https://www.researchgate.net/publication/309743873_Separation_techniques_Chromatography
- <1% - https://www.researchgate.net/publication/259701045_Modeling_of_salt_and_pH_gradient_elution_in_ion-exchange_chromatography
- <1% - https://www.researchgate.net/publication/223628077_Separation_and_removal_of_metal_ions_from_dilute_solutions_using_micellar-enhanced_ultrafiltration
- <1% - https://www.quora.com/What-is-the-basic-principle-of-high-performance-liquid-chromatography-HPLC
- <1% - https://www.quora.com/What-is-Adsorption-Chromatography
- <1% - https://www.phmethods.net/sites/default/files/10.5530phm.2017.8.1.pdf
- <1% - https://www.pharmatutor.org/articles/flash-chromatography-area-applications
- <1% - https://www.ncbi.nlm.nih.gov/pubmed/6175345
- <1% - https://www.ncbi.nlm.nih.gov/pubmed/18179225
- <1% - https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3174051/
- <1% - https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1529816/
- <1% - https://www.mdpi.com/2223-7747/6/4/42/htm
- <1% - https://www.lenntech.com/Data-sheets/Ion-Exchange-for-Dummies-RH.pdf
- <1% - https://www.lenntech.com/Data-sheets/Dowex-Ion-Exchange-Resins-Fundamentals-L.pdf
- <1% - https://www.jove.com/science-education/10187/gas-chromatography-gc-with-flame-ionization-detection
- <1% - https://www.jove.com/science-education/10156/high-performance-liquid-chromatography-hplc
- <1% - https://www.cytivalifesciences.com/en/us/solutions/protein-research/knowledge-center/protein-purification-methods/ion-exchange-chromatography
- <1% - https://www.coursehero.com/file/p745k85/Smaller-molecules-enter-the-pores-of-the-resin-and-diffuse-further-into-the/
- <1% - https://www.coursehero.com/file/p2nmhim/Figure-1-shows-a-beaker-containing-mobile-phase-and-a-prepared-paper-stationary/
- <1% - https://www.column-chromatography.com/blogs/application-of-column-chromatography-in-pharmacy
- <1% - https://www.chemguide.co.uk/analysis/chromatography/paper.html
- <1% - https://www.chemguide.co.uk/analysis/chromatography/hplc.html
- <1% - https://www.britannica.com/science/stationary-phase-chromatography
- <1% - https://www.britannica.com/science/paper-chromatography
- <1% - https://www.britannica.com/science/cation-exchange-resin
- <1% - https://www.bio-rad.com/en-us/applications-technologies/cation-exchange-chromatography?ID=MWHB018UU
- <1% - https://www.bio-rad.com/en-us/applications-technologies/anion-exchange-chromatography?ID=MWHAZ4C4S
- <1% - https://www.bio-rad.com/en-uk/applications-technologies/anion-exchange-chromatography?ID=MWHAZ4C4S
- <1% - https://www.bio-rad.com/de-de/applications-technologies/cation-exchange-chromatography?ID=MWHB018UU
- <1% - https://www.biologydiscussion.com/biochemistry/chromatography-techniques/top-12-types-of-chromatographic-techniques-biochemistry/12730
- <1% - https://www.bbc.co.uk/bitesize/guides/zgt6b82/revision/3
- <1% - https://www.bbc.co.uk/bitesize/guides/zgbqtfr/revision/7
- <1% - https://www.answers.com/Q/What_is_the_role_of_stationary_phase_in_chromatography
- <1% - https://vlab.amrita.edu/?sub=2&brch=191&sim=341&cnt=1
- <1% - https://satyapsingh.files.wordpress.com/2012/09/chromatography-and-distillation.pdf
- <1% - https://sargenttexas.org/chromatography-2/
- <1% - https://pediaa.com/what-is-the-difference-between-mobile-phase-and-stationary-phase/
- <1% - https://pediaa.com/difference-between-normal-phase-and-reverse-phase-chromatography/
- <1% - https://oneofchemistry.blogspot.com/2011/10/thin-layer-chromatography-and-column.html
- <1% - https://medical-dictionary.thefreedictionary.com/Flash+columna+cromatografía
- <1% – https://link.springer.com/chapter/10.1007%2F978-3-319-45776-5_12
- <1% - https://instrumentationtools.com/chromatography-questions-answers/
- <1% - https://en.wikipedia.org/wiki/Stationary_phase_(química)
- <1% - https://en.wikipedia.org/wiki/Retardation_factor
- <1% - https://en.wikipedia.org/wiki/Monolithic_HPLC_column
- <1% - https://en.wikipedia.org/wiki/Metabolomics
- <1% - https://en.wikipedia.org/wiki/Chromatography,_thin_layer
- <1% - https://en.wikipedia.org/wiki/Chromatography
- <1% - https://en.wikibooks.org/wiki/Proteomics/Protein_Separations_-_Chromatography/Hydrophobic_Interaction_Chromatography_(HIC)
- <1% - https://core.ac.uk/download/pdf/147603501.pdf
- <1% - https://chrominfo.blogspot.com/2020/06/
- <1% - https://chem-net.blogspot.com/2013/07/what-is-gas-chromatography-gc.html
- <1% - https://chemistry.missouri.edu/sites/default/files/class-files/new_chromatography_lab_2.pdf
- <1% - https://chem.libretexts.org/Bookshelves/Ancillary_Materials/Demos%2C_Techniques%2C_and_Experiments/General_Lab_Techniques/Thin_Layer_Chromatography
- <1% - https://chem.libretexts.org/Bookshelves/Analytical_Chemistry/Supplemental_Modules_(Química_analítica)/Análisis_instrumental/Cromatografía/Cromatografía_de_líquidos_de_alto_rendimiento
- <1% - https://byjus.com/chemistry/thin-layer-chromatography/
- <1% - https://answersdrive.com/what-role-does-polarity-play-in-chromatography-7022293
- <1% - http://www.open.edu/openlearn/science-maths-technology/science/biology/nucleic-acids-and-chromatin/content-section-2.4
- <1% - http://vlab.amrita.edu/?sub=2&brch=191&sim=341&cnt=1
- <1% - http://orgchemboulder.com/Technique/Procedures/Columnchrom/Columnchrom.shtml
- <1% - http://europepmc.org/abstract/MED/28058406
- <1% - http://biotechisfuture.weebly.com/uploads/1/4/1/6/14160671/affinity_chromatography_1.pdf