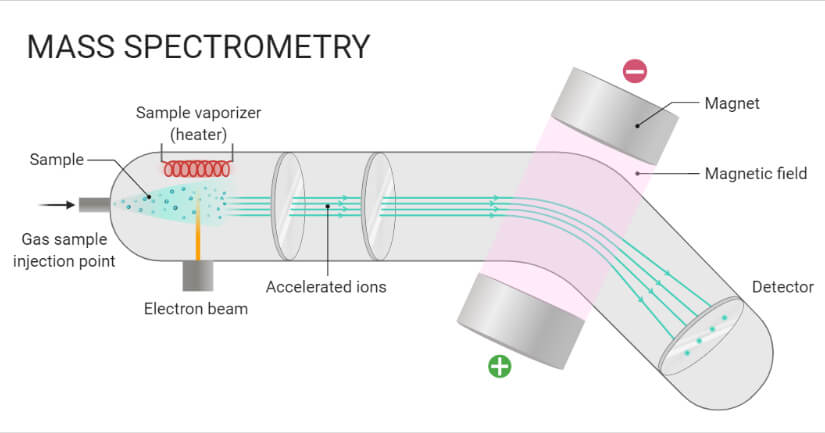
La espectrometría de masas (EM) es una técnica de química analítica que ayuda a identificar la cantidad y el tipo de sustancias químicas presentes en una muestra midiendo la relación masa-carga y la abundancia de los iones en fase gaseosa.
En esta técnica instrumental, la muestra se convierte en iones positivos que se mueven rápidamente mediante un bombardeo de electrones y las partículas cargadas se separan en función de sus masas.
Lectura relacionada: Fermentación en estado sólido (SSF)
Fermentación en estado sólido (SSF)Un espectro de masas es un gráfico de la abundancia relativa frente a la relación masa/carga (m/e).
Estos espectros se utilizan para determinar la firma elemental o isotópica de una muestra, las masas de las partículas y de las moléculas, y para dilucidar las estructuras químicas de las moléculas y otros compuestos químicos.
Principio de la espectrometría de masas (EM)
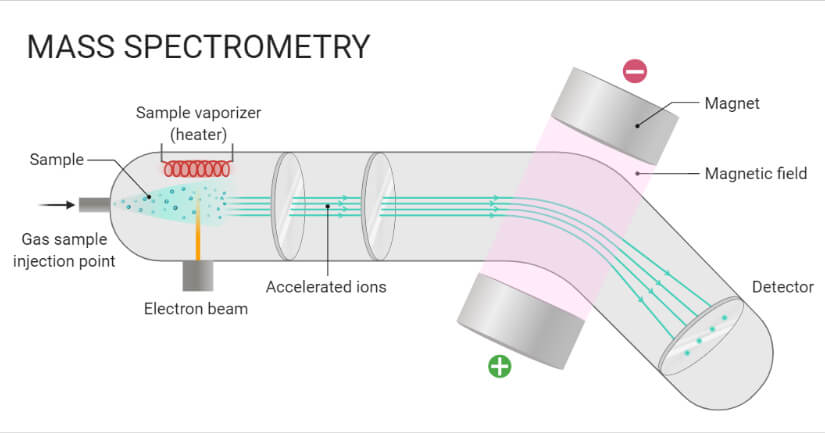
- En esta técnica, las moléculas se bombardean con un haz de electrones energéticos.
- Las moléculas se ionizan y se rompen en muchos fragmentos, algunos de los cuales son iones positivos. Cada tipo de ion tiene una relación particular entre la masa y la carga, es decir, la relación m/e (valor).
- Para la mayoría de los iones, la carga es uno y, por tanto, la relación m/e es simplemente la masa molecular del ion.
- Los iones atraviesan campos magnéticos y eléctricos para llegar al detector, donde se detectan y se registran las señales para obtener el espectro de masas.
Funcionamiento de la espectrometría de masas (EM)
- En un procedimiento típico, una muestra, que puede ser sólida, líquida o gaseosa, se ioniza, por ejemplo, bombardeándola con electrones.
- Esto puede hacer que algunas de las moléculas de la muestra se rompan en fragmentos cargados. A continuación, estos iones se separan según su relación masa-carga, normalmente acelerándolos y sometiéndolos a un campo eléctrico o magnético:
- Los iones de la misma relación masa-carga sufrirán la misma desviación.
- Los iones se detectan mediante un mecanismo capaz de detectar partículas cargadas, como un multiplicador de electrones. Los resultados se muestran como espectros de la abundancia relativa de los iones detectados en función de la relación masa-carga.
- Los átomos o moléculas de la muestra pueden identificarse mediante la correlación de masas conocidas (por ejemplo, una molécula entera) con las masas identificadas o mediante un patrón de fragmentación característico.
Instrumentación y pasos de la Espectrometría de Masas (EM)
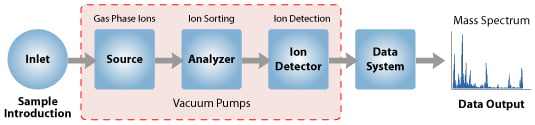
A. Entrada de la muestra
Lectura relacionada: Cromatografía de permeación en gel - Definición, principio, partes, pasos, usos
Cromatografía de permeación en gel - Definición, principio, partes, pasos, usos- Una muestra almacenada en el gran depósito desde el que las moléculas llegan a la cámara de ionización a baja presión en un flujo constante por un orificio llamado "fuga molecular".
B. Ionización
- Los átomos se ionizan eliminando uno o varios electrones para dar lugar a iones positivos mediante el bombardeo con una corriente de electrones. La mayoría de los iones positivos formados tendrán una carga de +1.
- La ionización puede lograrse mediante :
- Ionización por electrones (EI-MS)
- Ionización química (CI-MS)
- Técnica de desorción (FAB)
C. Aceleración
- Los iones se aceleran para que todos tengan la misma energía cinética.
- Los iones positivos pasan por 3 rendijas con voltaje en orden decreciente.
- La rendija del medio lleva los intermedios y los finales a cero voltios.
D. Desviación
Lectura relacionada: Cromatografía de filtración en gel - Definición, principio, tipos, partes, pasos, usos
Cromatografía de filtración en gel - Definición, principio, tipos, partes, pasos, usos- Los iones son desviados por un campo magnético debido a las diferencias de sus masas.
- Cuanto más ligera es la masa, más se desvían.
- También depende del número de carga positiva que lleve un ión; cuanto más carga positiva, más se desviará.
E. Detección
- El haz de iones que pasa por el analizador de masas es detectado por un detector en función de la relación m/e.
- Cuando un ion choca con la caja metálica, la carga se neutraliza mediante un electrón que salta del metal al ion.
- Tipos de analizadores:
- Analizadores de masas del sector magnético
- Analizadores de doble enfoque
- Analizadores de masas cuadrupolares
- Analizadores de tiempo de vuelo (TOF)
- Analizador de trampas de iones
- Analizador de ciclotrón de iones
Aplicaciones de la Espectrometría de Masas (EM)
- Control y análisis medioambiental (contaminantes del suelo, del agua y del aire, calidad del agua, etc.)
- Geoquímica: determinación de la edad, composición del suelo y de la roca, prospección de petróleo y gas
- Industria química y petroquímica - Control de calidad
- Identificar las estructuras de las biomoléculas, como los hidratos de carbono, los ácidos nucleicos
- Secuenciar biopolímeros como proteínas y oligosacáridos
- Determinación de la masa molecular de péptidos, proteínas y oligonucleótidos.
- Monitorización de los gases en la respiración de los pacientes durante la cirugía.
- Identificación de drogas de abuso y metabolitos de drogas de abuso en sangre, orina y saliva.
- Análisis de partículas de aerosol.
- Determinación de los residuos de plaguicidas en los alimentos.
Referencias y fuentes
- https://www.thermofisher.com/au/en/home/life-science/protein-biology/protein-biology-learning-center/protein-biology-resource-library/pierce-protein-methods/overview-mass-spectrometry.html
- https://www.slideshare.net/akshukumarsharma/mass-spectroscopy 55382941
- http://www.chem.ucalgary.ca/courses/350/Carey5th/Ch13/ch13-ms.html
- https://en.wikipedia.org/wiki/Mass_spectrometry
- https://www.chemguide.co.uk/analysis/masspec/howitworks.html
- https://www.slideshare.net/solairajananant/mass-spectrometry-38534267
- https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/spectrpy/massspec/masspec1.htm