
Que diferencia principal entre el número de oxidación y la carga es que Podemos determinar el número de oxidación de un átomo considerando la cantidad de electrones que ese átomo elimina o gana, mientras que la carga se determina considerando la cantidad total de electrones y protones en el átomo.
Los diferentes elementos de la tabla periódica tienen diferentes propiedades químicas y físicas. Y cuando se combinan en moléculas, diferentes elementos se combinan con otros elementos en diferentes proporciones. Entre un gran número de variaciones entre elementos, los parámetros más simples e importantes son su carga y número de oxidación. La carga y el número de oxidación de un elemento ayudan a identificar a qué grupo pertenece ese elemento en la tabla periódica. Lo que es más importante, ayuda a describir la capacidad del elemento para formar otras moléculas y compuestos de coordinación y, por lo tanto, ayuda a identificar sus fórmulas empíricas.
Lectura relacionada: Diferencia entre densidad y concentración.
Diferencia entre densidad y concentración.CONTENIDO
1. Descripción general y diferencia clave
2. ¿Cuál es el número de oxidación?
3. ¿Qué es la carga?
4. Comparación lado a lado: número de oxidación frente a carga en forma tabular
5. Resumen
¿Cuál es el número de oxidación?
El número de oxidación es una propiedad del átomo central de un compuesto de coordinación. Es la carga del átomo central de un compuesto de coordinación cuando todos los enlaces alrededor de ese átomo son iónicos. Por lo tanto, la carga y el número de oxidación son a veces similares, pero a veces diferentes. Por ejemplo, los elementos simples del bloque s y del bloque p tienen el mismo número de oxidación que su carga. Además, los iones poliatómicos tienen el mismo número de oxidación que la carga. Sin embargo, un mismo elemento químico puede tener diferentes números de oxidación dependiendo de los otros átomos que lo rodean. En un elemento libre, el número de oxidación siempre es cero. Además, los iones de metales de transición (bloque d) y los elementos tienen diferentes números de oxidación.
 Lectura relacionada:
Lectura relacionada: Diferencia entre cuarzo y feldespato.
Diferencia entre cuarzo y feldespato.Figura 01: Determinación de los números de oxidación de diferentes elementos en compuestos.
Al considerar un compuesto de coordinación, el átomo metálico central siempre debe tener orbitales vacíos a los que los ligandos donan sus pares de electrones solitarios y forman enlaces iónicos. Además, podemos indicar el número de oxidación del átomo de metal central con números romanos entre paréntesis. Por ejemplo, si el número de oxidación del metal "M" es 3, lo escribimos como M(III).
¿Qué es la carga?
La carga de cada átomo es cero. Cuando los átomos quitan o ganan electrones, adquieren una carga eléctrica. Esto se debe a que los electrones son partículas subatómicas con carga negativa, mientras que los protones tienen carga positiva. Los átomos eliminan o ganan electrones para llenar su capa de valencia de acuerdo con la regla del octeto.
Lectura relacionada: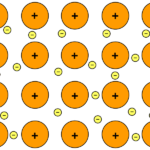 Diferencia entre enlace iónico y enlace metálico.
Diferencia entre enlace iónico y enlace metálico.En un átomo, el número de protones y electrones es igual. Como los protones tienen carga positiva y los electrones carga negativa, cuando los electrones salen de la capa de valencia, el átomo forma un ion con carga positiva porque el número de protones positivos es entonces mayor que el número de electrones en ese ion.
Determinación de la tarifa
Además, si un átomo es más electronegativo, puede atraer electrones de otros átomos. Allí absorben más electrones que protones hay en su núcleo. Así es como los átomos se convierten en iones negativos. Además, el número de electrones donados o extraídos difiere de un átomo a otro. Podemos predecir esto a partir de la posición del elemento en la tabla periódica. Normalmente, los átomos del mismo grupo forman los mismos iones cargados porque tienen el mismo número de electrones de valencia.

Figura 02: Estructura de un átomo al determinar la carga.
El número de grupo también muestra el número de electrones de valencia; Por tanto, podemos determinar la carga de los iones formados por los átomos de este grupo. Por ejemplo, los elementos del primer grupo forman iones monovalentes con una carga eléctrica de +1. Los elementos del segundo grupo forman iones divalentes cargados positivamente. Los átomos del grupo tres y del grupo cuatro forman iones cargados +3 y +4, respectivamente. Del grupo cinco al grupo siete, los átomos forman iones cargados negativamente porque es más fácil llenar sus electrones de valencia al recibir solo 2 o 3 electrones en lugar de emitir cinco, seis o siete electrones. Por lo tanto, los elementos del grupo cinco forman -3 iones cargados, mientras que los elementos del grupo 6 forman -2 iones y los elementos del grupo 7 forman -1 iones. Además de estos iones simplemente cargados, también hay iones complejos con cargas como NH4+ y compañía32-etc.
¿Cuál es la diferencia entre el número de oxidación y la carga?
El número de oxidación y la carga son dos términos relacionados en química. Sin embargo, existen algunas diferencias entre el número de oxidación y la carga. los diferencia clave entre el número de oxidación y la carga es que podemos determinar el número de oxidación de un átomo considerando la cantidad de electrones que ese átomo elimina o gana, mientras que la carga se determina considerando la cantidad total de electrones y protones en el átomo .
Además, para un mismo elemento químico, puede haber múltiples números de oxidación según los átomos que lo rodean, mientras que la carga del átomo es variable solo según la cantidad de electrones y protones en el átomo. Por lo tanto, esta es otra diferencia importante entre el número de oxidación y la carga.

Resumen - Número de oxidación frente a carga
Carga y número de oxidación son dos términos relacionados. los diferencia clave entre el número de oxidación y la carga es que podemos determinar el número de oxidación de un átomo considerando la cantidad de electrones que ese átomo elimina o gana, mientras que la carga se determina considerando la cantidad total de electrones y protones en el átomo .
Relación:
1. “Número de oxidación”. metales de transición. Disponible aquí
2. Textos libres. "El átomo". Química LibreTexts, Fundación Nacional de Ciencias, 26 de noviembre de 2018. Disponible aquí
Imagen de cortesía:
1. "Asignaciones de estado de oxidación" por SARANPHONG YIMKLAN - Trabajo propio, (Dominio público) a través de Commons Wikimedia
2. "Carga nuclear efectiva" Por trabajo propio - Carga nuclear efectiva.gif, (Dominio público) a través de Commons Wikimedia











