
Que Diferencia clave entre el clorato de potasio y el perclorato de potasio es que el clorato de potasio es muy reactivo en comparación con el perclorato de potasio.
Lectura relacionada: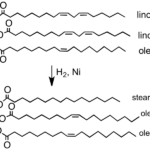 ¿Cuál es la diferencia entre aceite hidrogenado y parcialmente hidrogenado?
¿Cuál es la diferencia entre aceite hidrogenado y parcialmente hidrogenado?El clorato de potasio y el perclorato de potasio son compuestos iónicos que podemos llamar compuestos de sal inorgánica. Estos compuestos están formados por iones de potasio, átomos de cloruro y átomos de oxígeno.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el clorato de potasio?
3. ¿Qué es el perclorato de potasio?
4. Clorato de potasio frente a perclorato de potasio en forma tabular
5. Resumen: clorato de potasio frente a perclorato de potasio
¿Qué es el clorato de potasio?
El clorato de potasio es un compuesto iónico con la fórmula química KClO3. Este compuesto aparece en su forma pura como una sustancia cristalina blanca. En aplicaciones industriales, este es el segundo compuesto de clorato más común en importancia después del clorato de sodio. Se sabe que el clorato de potasio es un agente oxidante fuerte. La aplicación más común es la fabricación de fósforos. Sin embargo, esta conexión ha sido reemplazada por otras conexiones alternativas en muchas otras aplicaciones, ya que en su mayoría está obsoleta.
Lectura relacionada: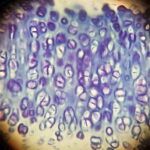 ¿Cuál es la diferencia entre metacromasia y metacromática?
¿Cuál es la diferencia entre metacromasia y metacromática?
Figura 01: clorato de potasio
Los usos comunes del clorato de potasio incluyen la fabricación de fuegos artificiales, propulsores, explosivos, la preparación de oxígeno para uso en laboratorio y generadores químicos de oxígeno. También se utiliza como desinfectante de enjuagues bucales y como herbicida agrícola.
Lectura relacionada: ¿Cuál es la diferencia entre polimorfismo y amorfismo?
¿Cuál es la diferencia entre polimorfismo y amorfismo?La producción industrial de clorato de potasio implica la reacción de metátesis de sal, que involucra clorato de sodio y cloruro de potasio. La baja solubilidad del clorato de potasio en agua ayuda a esta reacción. En algunos casos, también se utiliza la electrólisis directa de KCl para esta producción.
Normalmente, el clorato de potasio es un compuesto peligroso con el que debemos tener cuidado. Tiende a reaccionar violentamente y, a veces, incluso se enciende o explota espontáneamente cuando se mezcla con algunos materiales combustibles.
¿Qué es el perclorato de potasio?
El perclorato de potasio es un compuesto inorgánico con la fórmula química KClO4. Es una sal inorgánica. Al igual que otros percloratos, el perclorato de potasio es un agente oxidante fuerte. Pero tiende a reaccionar muy lentamente con la materia orgánica. Este compuesto aparece como un sólido cristalino incoloro.

Figura 02: Cristal de perclorato de potasio
Podemos producir perclorato de potasio industrialmente al tratar una solución acuosa de perclorato de sodio con cloruro de potasio. Es una reacción de precipitación de un solo paso. Se aprovecha de la baja solubilidad de este compuesto - solubilidad muy baja en comparación con el perclorato de sodio. Además, alternativamente podemos hacer este compuesto burbujeando cloro gaseoso a través de una solución de clorato de potasio e hidróxido de potasio.
Los usos del perclorato de potasio incluyen el uso en fuegos artificiales, cebadores de municiones, cebadores y diversos propulsores, composiciones de destellos, estrellas y bengalas. También se utilizó como propulsor de cohetes sólidos en el pasado. Sin embargo, esta aplicación ha sido sustituida por el perclorato de amonio.
¿Cuál es la diferencia entre el clorato de potasio y el perclorato de potasio?
El clorato de potasio y el perclorato de potasio son compuestos inorgánicos iónicos. La fórmula química del clorato de potasio es KClO3, mientras que la fórmula química del perclorato de potasio es KClO4. La principal diferencia entre el clorato de potasio y el perclorato de potasio es que el clorato de potasio es muy reactivo en comparación con el perclorato de potasio. Además, la producción a escala industrial de clorato de potasio involucra la reacción de metátesis de sal que involucra clorato de sodio y cloruro de potasio, mientras que la producción industrial de perclorato de potasio involucra el tratamiento de una solución acuosa de perclorato de sodio con cloruro de potasio.
La siguiente infografía enumera las diferencias entre el clorato de potasio y el perclorato de potasio en forma tabular para una comparación directa.
Resumen: clorato de potasio frente a perclorato de potasio
El clorato de potasio y el perclorato de potasio son compuestos inorgánicos iónicos. La principal diferencia entre el clorato de potasio y el perclorato de potasio es que el clorato de potasio es muy reactivo en comparación con el perclorato de potasio.
Relación:
1. “Clorato de potasio”. Centro Nacional de Información Biotecnológica. Base de datos de conexión de PubChemBiblioteca Nacional de Medicina de EE.
Imagen de cortesía:
1. "Sustancia de clorato de potasio" del cargador original fue Chemik10 en pl.wikipedia - Transferido de pl.wikipedia; Transferido a Commons por User:Pjahr usando CommonsHelper. (CC BY-SA 3.0) a través de Commons Wikimedia
2. “Perclorato de Potássio” por Taz Rodrigues Lopes – www.flickr.com (Dominio público) a través de Commons Wikimedia











