Que Diferencia clave entre el nitrato de plomo y el nitrato de zinc es que el nitrato de plomo reacciona con el hidróxido de amonio y forma un precipitado blanco que es insoluble en una solución de hidróxido de amonio en exceso, mientras que el nitrato de zinc reacciona con el hidróxido de amonio y forma un precipitado blanco que es soluble en una solución de hidróxido de amonio en exceso.
Lectura relacionada: ¿Cuál es la diferencia entre transesterificación y transesterificación?
¿Cuál es la diferencia entre transesterificación y transesterificación?El nitrato de plomo es un compuesto inorgánico con la fórmula química Pb(NO3)2, mientras que el nitrato de zinc es un compuesto inorgánico con la fórmula química Zn(NO3)2.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el nitrato de plomo?
3. ¿Qué es el nitrato de zinc?
4. Nitrato de plomo frente a nitrato de zinc en forma tabular
5. Resumen: nitrato de plomo frente a nitrato de zinc
¿Qué es el nitrato de plomo?
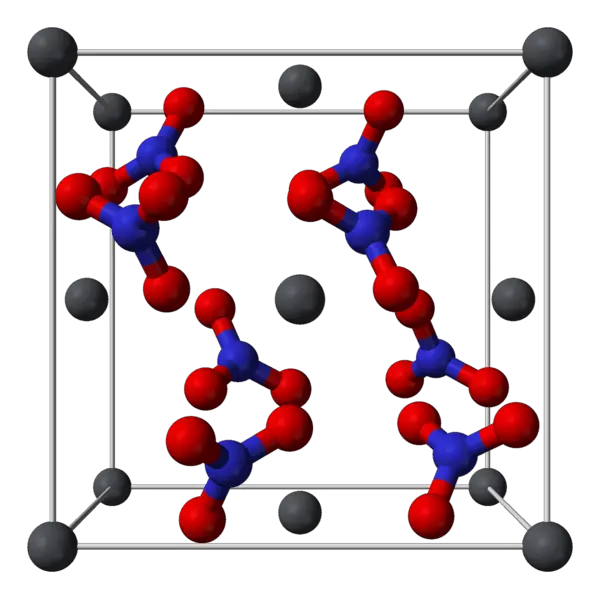
El nitrato de plomo es un compuesto inorgánico con la fórmula química Pb(NO3)2. Por lo general, se presenta en forma de cristal incoloro o polvo blanco. Se descompone a altas temperaturas. Normalmente, este compuesto es tóxico y debemos tener cuidado con él para evitar su inhalación, ingestión y contacto con la piel.
Lectura relacionada: ¿Cuál es la diferencia entre la fenitoína y la fenitoína sódica?
¿Cuál es la diferencia entre la fenitoína y la fenitoína sódica?Podemos producir compuestos de nitrato de plomo a través de la reacción entre el óxido de plomo y el ácido nítrico concentrado. También podemos prepararlo evaporando la solución obtenida al hacer reaccionar plomo metálico con ácido nítrico diluido. Además, se pueden formar cristales de nitrato de plomo durante el procesamiento de desechos de plomo y bismuto de las refinerías de plomo.

Figura 01: La disposición atómica del compuesto de nitrato de plomo.
Lectura relacionada: ¿Cuál es la diferencia entre la reducción de MPV y la oxidación de Oppenauer?
¿Cuál es la diferencia entre la reducción de MPV y la oxidación de Oppenauer?Por lo general, el nitrato de plomo tiende a descomponerse cuando se calienta. Esto es útil en pirotecnia. Además, es soluble en agua y también se disuelve en ácido nítrico diluido. Cuando agregamos compuestos alcalinos a la solución, se forman nitratos básicos. Podemos usar compuestos de nitrato de plomo para hacer complejos de coordinación. En estos complejos, el ion plomo es un aceptor fuerte y puede formar complejos fuertes al combinarse con ligandos de oxígeno y nitrógeno donadores de electrones. B. combinación de nitrato de plomo y pentaetilenglicol en presencia de acetonitrilo y metanol [Pb(NO3)2(EO5)] al evaporarse.
Hay pocas aplicaciones del nitrato de plomo, incluido su uso como estabilizador térmico en poliésteres de nailon en forma de recubrimiento para papel fototermográfico y en rodenticidas, en el proceso de cianuración de oro con fines de lixiviación y en la fabricación de isotiocianatos a partir de ditiocarbamatos.
¿Qué es el nitrato de zinc?
El nitrato de zinc es un compuesto inorgánico con la fórmula química Zn(NO3)2. Es una sal blanca cristalina que es profusamente delicuescente. Típicamente lo encontramos en forma hexahidratada. Además, esta sustancia es soluble tanto en agua como en alcohol.

Figura 02: La estructura química del nitrato de zinc.
Podemos hacer nitrato de zinc disolviendo zinc en ácido nítrico. Sin embargo, esta reacción depende de la concentración. La reacción en ácido concentrado también forma nitrato de amonio. Además, cuando calentamos el compuesto de nitrato de zinc, puede sufrir una descomposición térmica para formar óxido de zinc, dióxido de nitrógeno y oxígeno.
Hay algunos usos del nitrato de zinc, incluido su uso en la síntesis de polímeros de coordinación, la producción de varios compuestos a base de ZnO, como mordiente en el teñido, etc.
¿Cuál es la diferencia entre el nitrato de plomo y el nitrato de zinc?
El nitrato de plomo y el nitrato de zinc son compuestos inorgánicos con importantes usos industriales. La principal diferencia entre el nitrato de plomo y el nitrato de zinc es su reacción con el hidróxido de amonio. El nitrato de plomo reacciona con el hidróxido de amonio para formar un precipitado blanco que es insoluble en una solución de hidróxido de amonio en exceso, mientras que el nitrato de zinc reacciona con el hidróxido de amonio para formar un precipitado blanco que es soluble en una solución de hidróxido de amonio en exceso.
La siguiente infografía muestra las diferencias entre el nitrato de plomo y el nitrato de zinc en forma tabular para una comparación directa.
Resumen: nitrato de plomo frente a nitrato de zinc
El nitrato de plomo y el nitrato de zinc son nitratos de cationes de plomo y zinc, respectivamente. los diferencia clave entre el nitrato de plomo y el nitrato de zinc es que el nitrato de plomo reacciona con hidróxido de amonio y forma un precipitado blanco que es insoluble en exceso de solución de hidróxido de amonio mientras que el nitrato de zinc reacciona con hidróxido de amonio y forma un precipitado blanco que es soluble en exceso de solución de hidróxido de amonio .
Relación:
1. "Nitrato de zinc". Centro Nacional de Información Biotecnológica. Base de datos de conexión de PubChemBiblioteca Nacional de Medicina de EE.
Imagen de cortesía:
1. "Plomo (II)-nitrat-unit-cell-3D-balls" por Ben Mills - Trabajo propio (Dominio público) a través de Commons Wikimedia
2. "Zincnitrat" por Edgar181 - Trabajo propio (Dominio público) a través de Commons Wikimedia