Que Diferencia clave entre la solución tampón y la hidrólisis de sal. es que las soluciones amortiguadoras son soluciones que pueden, hasta cierto punto, resistir cualquier cambio en su pH, mientras que la hidrólisis de sal es una reacción química que puede cambiar el pH de una solución.
Lectura relacionada: ¿Cuál es la diferencia entre isoprenoide y esteroide?
¿Cuál es la diferencia entre isoprenoide y esteroide?Un tampón es una solución acuosa que tiende a resistir el cambio de pH. La hidrólisis de sal es una reacción en la que uno de los iones de una sal reacciona con el agua, formando una solución ácida o básica.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la solución tampón?
3. ¿Qué es la hidrólisis de sal?
4. Solución tampón frente a hidrólisis de sal en forma tabular
5. Resumen: solución tampón frente a hidrólisis salina
¿Qué es la solución tampón?
Un tampón es una solución acuosa que tiende a resistir el cambio de pH. Esta solución contiene una mezcla de un ácido débil y su base conjugada, o viceversa. El pH de estas soluciones cambia ligeramente con la adición de un ácido fuerte o una base fuerte.
Lectura relacionada: ¿Cuál es la diferencia entre sulfato de cobre hidratado y anhidro?
¿Cuál es la diferencia entre sulfato de cobre hidratado y anhidro?El ácido débil (o base) y su base conjugada (o ácido conjugado) están en equilibrio entre sí. Si agregamos un poco de ácido fuerte a este sistema, el equilibrio se desplazará hacia el ácido y formará más ácido usando los iones de hidrógeno liberados del ácido fuerte agregado. Aunque esperamos un aumento en los iones de hidrógeno con la adición del ácido fuerte, no aumenta tanto. De manera similar, cuando agregamos una base fuerte, la concentración de iones de hidrógeno disminuye menos de lo esperado para la cantidad de álcali agregado. Podemos medir esta resistencia a los cambios de pH como capacidad amortiguadora. La capacidad amortiguadora mide la resistencia de un amortiguador a un cambio en el pH cuando se agregan iones OH- (una base).

Figura 01: Capacidad del búfer
Lectura relacionada: ¿Cuál es la diferencia entre las lectinas y los oxalatos?
¿Cuál es la diferencia entre las lectinas y los oxalatos?Al considerar el uso de tampones, estas soluciones son necesarias para mantener el pH correcto para la actividad enzimática en los organismos. Además, se utilizan en la industria en procesos de fermentación, establecimiento de las condiciones adecuadas para colorantes, en análisis químicos, calibración de medidores de pH, etc.
¿Qué es la hidrólisis de sal?
La hidrólisis de sal se puede describir como una reacción en la que uno de los iones de una sal reacciona con agua, formando una solución ácida o básica. Cuando se forma una sal dada a partir de la reacción de neutralización entre un ácido débil y una base fuerte, siempre se forman soluciones salinas, que son básicas en la hidrólisis de sal. Por otro lado, cuando se forma una sal particular a partir de la reacción de neutralización entre un ácido fuerte y una base débil, siempre produce soluciones salinas básicas tras la hidrólisis de la sal. De manera similar, cuando ocurre la neutralización entre un ácido fuerte y una base fuerte, la solución salina resultante después de la hidrólisis salina tendrá un pH de 7 (solución neutra). Esto significa que las soluciones de sal neutra no están sujetas a hidrólisis de sal.

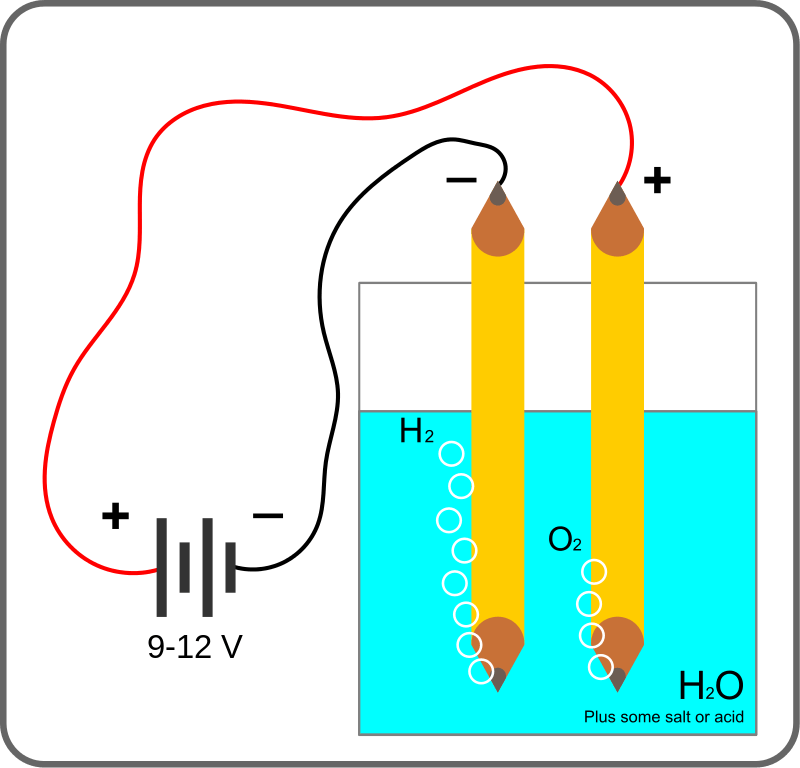
Figura 02: Electrólisis: hidrólisis de sal con corriente eléctrica.
La reacción de hidrólisis de sal se puede describir como una neutralización inversa. Cuando agregamos una sal al agua, el catión, el anión o ambos iones de la sal tienden a reaccionar con el agua, dando como resultado una solución básica o ácida en el proceso de hidrólisis.
¿Cuál es la diferencia entre la solución tampón y la hidrólisis de sal?
Las soluciones tampón y la hidrólisis de sal son términos importantes en química inorgánica y analítica. los diferencia clave entre la solución tampón y la hidrólisis de sal es que las soluciones tampón son soluciones que pueden resistir cualquier cambio en su pH hasta cierto punto, mientras que la hidrólisis de sal es una reacción química que puede cambiar el pH de una solución.
A continuación se muestra un resumen de la diferencia entre la solución tampón y la hidrólisis de sal en forma tabular para una comparación directa.
Resumen: solución tampón frente a hidrólisis de sal
Un tampón es una solución acuosa que tiende a resistir el cambio de pH. La hidrólisis de sal es una reacción en la que uno de los iones de una sal reacciona con el agua, formando una solución ácida o básica. los diferencia clave entre la solución tampón y la hidrólisis de sal es que las soluciones tampón son soluciones que pueden resistir cualquier cambio en su pH hasta cierto punto, mientras que la hidrólisis de sal es una reacción química que puede cambiar el pH de una solución.
Relación:
1. "21.21: Hidrólisis de sales - Ecuaciones". Química LibreTextsLibretextos, 22 de febrero de 2022.
Imagen de cortesía:
1. "Capacidad de búfer 2" por Quantumkinetics - Trabajo propio (CC BY-SA 4.0) a través de Commons Wikimedia
2. "Electrólisis" por © Nevit Dilmen (CC BY-SA 3.0) a través de Commons Wikimedia