Que diferencia principal entre el defecto de Schottky y el defecto de Frenkel El defecto de Schottky disminuye la densidad de un cristal mientras que el defecto de Frenkel no afecta la densidad de un cristal. Además de la principal diferencia mencionada anteriormente, otra diferencia importante entre el defecto de Schottky y el defecto de Frenkel es que el defecto de Schottky provoca una reducción en la masa del cristal mientras que el defecto de Frenkel no afecta la masa del cristal.
Lectura relacionada: Diferencia entre Cl2 y Cl3
Diferencia entre Cl2 y Cl3El término red cristalina describe la disposición simétrica de los átomos en un cristal. El defecto de Schottky y el defecto de Frenkel son dos formas de defectos puntuales que aparecen en una red cristalina. Un defecto puntual es un punto vacante creado por la pérdida de un átomo de la red cristalina. Estos defectos provocan irregularidades en las redes cristalinas.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es un defecto de Schottky?
3. ¿Qué es el defecto de Frenkel?
4. Comparación directa: defecto de Schottky frente a defecto de Frenkel en forma tabular
5. Resumen
¿Qué es un defecto de Schottky?
El defecto de Schottky es una forma de defecto puntual que se forma debido a la pérdida de un átomo en unidades estequiométricas de la red cristalina. Este defecto puntual recibió su nombre del científico Walter H. Schottky. Podemos observar este defecto tanto en cristales iónicos como no iónicos. Este defecto ocurre cuando un bloque de construcción sale de la red cristalina.
Lectura relacionada: Diferencia entre el lactato de Ringer y el cloruro de sodio
Diferencia entre el lactato de Ringer y el cloruro de sodio
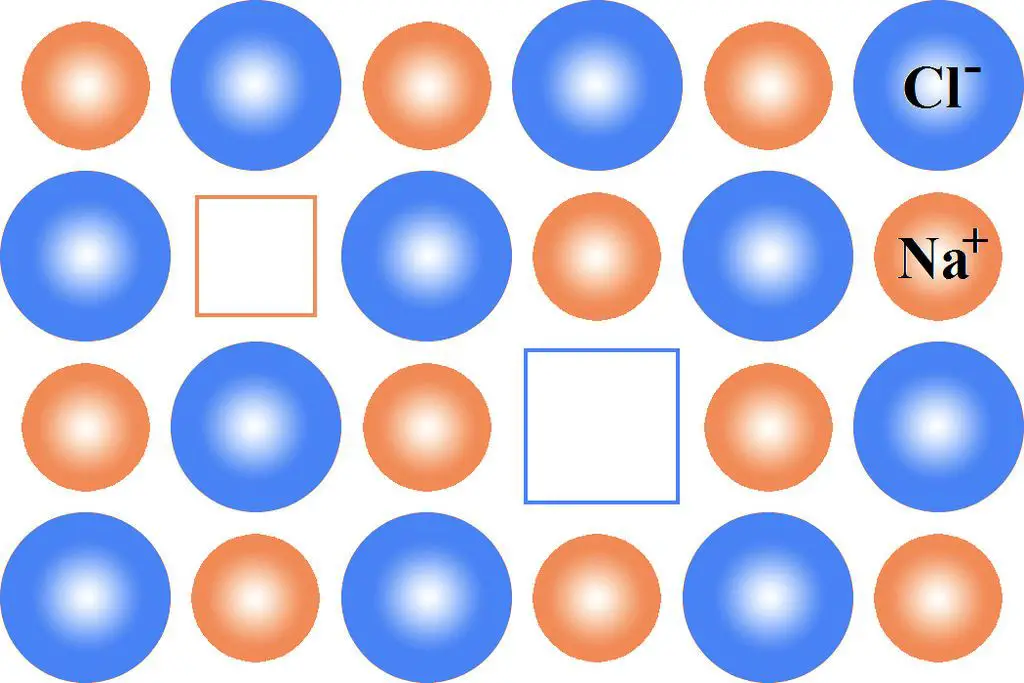
Figura 01: defecto de Schottky en NaCl
Aunque la red pierde un átomo, esto no afecta el balance de carga de la red ya que los átomos dejan una unidad estequiométrica de la red. Una unidad estequiométrica contiene átomos con cargas opuestas en proporciones iguales.
Lectura relacionada: Diferencia entre la solución de Hartmann y la solución salina normal
Diferencia entre la solución de Hartmann y la solución salina normalCuando ocurre este defecto, reduce la densidad de la red cristalina. Esta forma de defectos puntuales es común en los compuestos iónicos. Cuando ocurre en cristales no iónicos, lo llamamos defecto de vacancia. Muy a menudo, este defecto ocurre en redes cristalinas con átomos de casi el mismo tamaño. Ej.: rejilla de NaCl, rejilla de KBr, etc.
¿Qué es el defecto de Frenkel?
El defecto de Frenkel es una forma de defecto puntual en el que el defecto se produce debido a la pérdida de un átomo o un pequeño ion de la red cristalina. Esta pérdida crea un punto vacante en la cuadrícula. Los sinónimos de este defecto son trastorno de Frenkel y par de Frenkel. El defecto recibió su nombre del científico Yakov Frenkel.
Si un ion pequeño sale de la red cristalina, es un catión (un ion con carga positiva). Este ion ocupa una posición cerca del punto vacante. Por lo tanto, este defecto no afecta la densidad de la red cristalina. Esto se debe a que el átomo o los iones no abandonan completamente la red. Esta forma de defectos puntuales es común en las redes iónicas. A diferencia del defecto de Schottky, este defecto ocurre en redes con átomos o iones de diferentes tamaños.
¿Cuál es la diferencia entre el defecto de Schottky y el defecto de Frenkel?
El defecto de Schottky es una forma de defecto puntual que se forma debido a la pérdida de un átomo en unidades estequiométricas de la red cristalina. El defecto de Frenkel es una forma de defecto puntual en el que el defecto se produce debido a la pérdida de un átomo o un pequeño ion de la red cristalina. El defecto de Schottky reduce la densidad de la red cristalina, mientras que el defecto de Frenkel no afecta la densidad de la red cristalina.

Resumen: defecto de Schottky frente a defecto de Frenkel
Los defectos puntuales son defectos en las redes cristalinas que resultan de la pérdida de átomos o iones de la red, creando un punto vacante. El defecto de Schottky y el defecto de Frenkel son dos formas de defectos puntuales. La diferencia entre el defecto de Schottky y el defecto de Frenkel es que el defecto de Schottky disminuye la densidad de un cristal, mientras que el defecto de Frenkel no afecta la densidad de un cristal.
Relación:
1. “Defecto de Schottky”. Wikipedia, Fundación Wikimedia, 12 de mayo de 2018. Disponible aquí
2. "Defectos de cristal - Defectos puntuales". conductores y aisladores. Disponible aquí
Imagen de cortesía:
1. "NaCl - Defecto de Schottky" Por VladVD - Trabajo propio, (CC BY-SA 3.0) a través de Commons Wikimedia