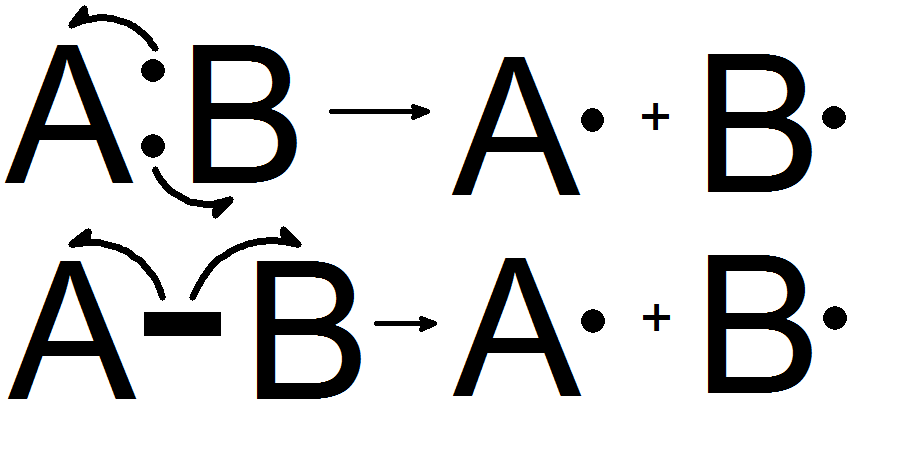Que diferencia principal entre la división homolítica y heterolítica es que la La escisión homolítica le da a cada fragmento un electrón de enlace, mientras que la escisión heterolítica le da a un fragmento dos electrones de enlace y al otro fragmento ninguno de los electrones de enlace.
Lectura relacionada: Diferencia entre ácidos binarios y oxiácidos.
Diferencia entre ácidos binarios y oxiácidos.La escisión es la ruptura de un enlace químico covalente. En otras palabras, divide una molécula en dos entidades. La escisión se produce de dos formas, la escisión homolítica forma dos unidades iguales y la escisión heterolítica forma dos unidades diferentes.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la fisión homolítica?
3. ¿Qué es la fisión heterolítica?
4. Comparación lado a lado: escisión homolítica frente a heterolítica en forma tabular
5. Resumen
¿Qué es la fisión homolítica?
La escisión homolítica es la disociación de un enlace químico y la formación de dos fragmentos iguales. Un enlace químico (enlace covalente) contiene dos electrones. En esta forma de fisión, cada uno de los fragmentos recibe un electrón desapareado. Cuando esta disociación de enlace ocurre en una molécula neutra que tiene un número par de electrones, forma dos radicales libres iguales.
Lectura relacionada: Diferencia entre carbonilo y cetona.
Diferencia entre carbonilo y cetona.
Figura 01: Escisión homolítica
La energía de disociación del enlace homolítico se refiere a la energía absorbida o liberada durante este proceso. Sin embargo, esta división solo tiene lugar bajo ciertas condiciones;
Lectura relacionada: Diferencia entre boro y bórax.
Diferencia entre boro y bórax.Además, algunos enlaces químicos específicos, como el enlace de peróxido, son lo suficientemente débiles como para disociarse espontáneamente con un ligero calentamiento.
¿Qué es la fisión heterolítica?
La escisión heterolítica es la disociación de un enlace químico y la formación de dos fragmentos diferentes. Un enlace químico (enlace covalente) contiene dos electrones. En esta forma de fisión, un fragmento recibe ambos pares de electrones de enlace, mientras que otro fragmento no recibe ninguno de los electrones de enlace.

Figura 02: escisión heterolítica
El fragmento que recibe ambos electrones de enlace forma un anión. El otro fragmento forma un catión. Allí, el fragmento que recibe ambos electrones es más electronegativo que el otro fragmento. Esta escisión se produce en enlaces covalentes simples. La energía que se absorbe o se libera con la ruptura de este enlace se denomina “energía de disociación de enlaces heterolíticos”.
¿Cuál es la diferencia entre la escisión homolítica y heterolítica?
La escisión homolítica es la disociación de un enlace químico y la formación de dos fragmentos iguales. Da a cada fragmento un electrón de enlace. La energía que se absorbe o se libera durante la escisión homolítica se denomina "energía de disociación del enlace homolítico". La escisión heterolítica es la disociación de un enlace químico y la formación de dos fragmentos diferentes. Hay dos electrones de enlace en un fragmento y ninguno de los electrones de enlace en el otro fragmento. Esta es la principal diferencia entre la fisión homolítica y heterolítica.. La energía que se absorbe o se libera durante la escisión heterolítica se denomina "energía de disociación del enlace heterolítico".

Resumen: escisión homolítica frente a heterolítica
La fisión es la disociación de enlaces. Hay dos formas como escisión homolítica y heterolítica. La diferencia entre la escisión homolítica y heterolítica es que la escisión homolítica le da a cada fragmento un electrón de enlace, mientras que la escisión heterolítica le da a un fragmento dos electrones de enlace y al otro fragmento ningún electrón de enlace.
Relación:
1. "Homólisis (química)". Wikipedia, Fundación Wikimedia, 17 de julio de 2018. Disponible aquí
2. "Activador de enzimas". Wikipedia, Fundación Wikimedia, 15 de julio de 2018. Disponible aquí
Imagen de cortesía:
1. "Arrow Pushing Homolytic" por Shoy - Trabajo propio, (Dominio público) a través de Commons Wikimedia
2. "Heterólisis (química)" Por Jürgen Martens - Jürgen Martens, (CC BY-SA 3.0) a través de Commons Wikimedia