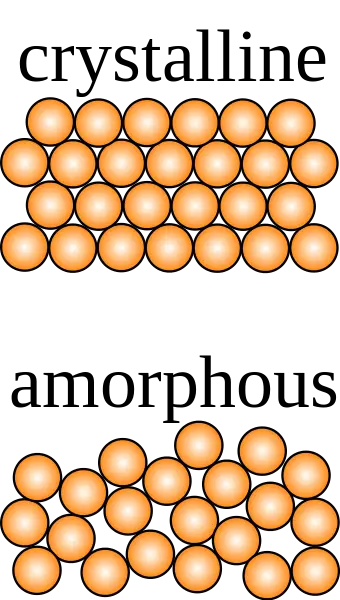
Que diferencia principal que se encuentra entre los sólidos amorfos y cristalinos Los sólidos cristalinos tienen una disposición ordenada de largo alcance de átomos o moléculas dentro de la estructura, mientras que los sólidos amorfos no tienen una disposición ordenada de largo alcance.
Podemos dividir los sólidos en cristalinos y amorfos según su disposición a nivel atómico. Sin embargo, algunos sólidos existen tanto en forma cristalina como amorfa. Dependiendo de sus necesidades, podemos preparar ambos tipos por separado.
Lectura relacionada: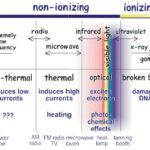 Diferencia entre radiación ionizante y no ionizante
Diferencia entre radiación ionizante y no ionizanteCONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es un sólido amorfo?
3. ¿Qué es un sólido cristalino?
4. Comparación lado a lado: sólido amorfo frente a cristalino en forma tabular
5. Resumen
¿Qué es un sólido amorfo?
El sólido amorfo es una forma de sólido que carece de una estructura cristalina. Allí no tiene un arreglo ordenado de largo alcance de átomos, moléculas o iones dentro de su estructura. Además, vidrio, geles, películas delgadas, plásticos y nanomateriales son algunos ejemplos de este tipo de sólidos.
Principalmente fabricamos vidrio con arena (sílice/SiO2) y bases tales como carbonato de sodio y carbonato de calcio. A altas temperaturas, estos materiales se derriten y, cuando los enfriamos, se forma rápidamente un vidrio rígido. Al enfriarse, los átomos se reorganizan para producir vidrio; por eso lo llamamos amorfo. Sin embargo, los átomos pueden tener un orden de corto alcance debido a las propiedades de enlace químico.
Lectura relacionada: Diferencia entre bisulfito de sodio y metabisulfito de sodio.
Diferencia entre bisulfito de sodio y metabisulfito de sodio.
Figura 01: un diagrama que muestra estructuras de estado sólido amorfas y cristalinas
Asimismo, también podemos producir otros materiales amorfos enfriando rápidamente el material fundido. Los sólidos amorfos no tienen un punto de fusión definido. Se licúan en un amplio rango de temperatura. Los sólidos amorfos como el caucho son útiles en la fabricación de neumáticos. El vidrio y los plásticos son útiles en la fabricación de artículos para el hogar, equipos de laboratorio, etc.
Lectura relacionada: Diferencia entre carbonato y bicarbonato.
Diferencia entre carbonato y bicarbonato.¿Qué es un sólido cristalino?
Los sólidos cristalinos o cristales tienen estructuras ordenadas y simetría. Los átomos, moléculas o iones en cristales que están dispuestos de una manera específica; así que haz un pedido remoto. En este tipo de sólido hay un patrón regular y repetitivo; por lo tanto, podemos identificar una unidad repetitiva.
Por definición, un cristal es “un compuesto químico homogéneo con una disposición regular y periódica de átomos. Por ejemplo, halita, sal (NaCl) y cuarzo (SiO2). Pero los cristales no se limitan a los minerales: contienen la mayoría de los sólidos, como azúcares, celulosa, metales, huesos e incluso ADN”. C
Además, como grandes rocas cristalinas como el cuarzo y el granito, los cristales son materiales naturales en la Tierra. A veces, los organismos vivos también forman cristales. Por ejemplo, la calcita es un producto de los moluscos. Hay cristales a base de agua en forma de nieve, hielo o glaciares.

Figura 02: Una estructura cristalina.
Además, podemos clasificar los cristales en función de sus propiedades físicas y químicas. Por ejemplo, cristales covalentes (p. ej., diamante), cristales metálicos (p. ej., pirita), cristales iónicos (p. ej., cloruro de sodio) y cristales moleculares (p. ej., azúcar). Además, estos cristales pueden tener diferentes formas y colores. Por lo tanto, tienen un valor estético y algunas personas creen que tienen propiedades curativas; Por lo tanto, utilizan estos cristales para crear joyas.
¿Cuál es la diferencia entre sólido amorfo y cristalino?
Los sólidos amorfos y cristalinos difieren en su estructura química. Por lo tanto, podemos decir que la principal diferencia entre los sólidos amorfos y cristalinos es que los sólidos cristalinos tienen una disposición ordenada de átomos o moléculas dentro de la estructura, mientras que los sólidos amorfos no tienen una disposición ordenada de largo alcance. Además, en los sólidos cristalinos existe una unidad repetitiva que constituye toda la estructura, pero no se puede dar ninguna unidad repetitiva para los sólidos amorfos.
Otra diferencia entre los sólidos amorfos y cristalinos: los sólidos cristalinos tienen un punto de fusión agudo, pero los sólidos amorfos no. Además, los sólidos cristalinos son anisotrópicos (diferentes propiedades en diferentes direcciones), pero los sólidos amorfos son isotrópicos (las propiedades son las mismas en todas las direcciones).

Resumen: amorfo frente a sólido cristalino
Los sólidos son principalmente de tres tipos como sólidos amorfos, semicristalinos y cristalinos. los diferencia clave entre los sólidos amorfos y cristalinos es que los sólidos cristalinos tienen una disposición ordenada de largo alcance de átomos o moléculas dentro de la estructura, mientras que los sólidos amorfos no tienen una disposición ordenada de largo alcance.
Relación:
1. Douglas, Ronald Walter, et al. "Sólido amorfo." Encyclopædia Britannica, Encyclopædia Britannica, Inc., 22 de abril de 2016. Disponible aquí
2. Textos libres. "12.1: Sólidos cristalinos y amorfos". Chemistry LibreTexts, National Science Foundation, 26 de noviembre de 2018. Disponible aquí
Imagen de cortesía:
1. "Cristalino o amorfo" Por Sbyrnes321 (conferencia) (CC BY-SA 3.0) a través de Commons Wikimedia
2. "148812" de OpenClipart-Vectors (CC0) a través de pixabay