Que diferencia principal entre aspartil cisteína y serina proteasas son sus grupos funcionales los que actúan como residuos catalíticos. El grupo funcional que actúa como restos catalíticos de la aspartil proteasa es un grupo de ácido carboxílico, mientras que en la cisteína proteasa un grupo tiol o sulfhidrilo actúa como grupo funcional sobre el resto catalítico, y en la serina proteasa un grupo hidroxilo o alcohol actúa como grupo funcional. grupo en el resto catalítico.
Las proteasas son enzimas que catalizan la proteólisis, que es la descomposición de las proteínas en polipéptidos o aminoácidos más pequeños. Este proceso tiene lugar mediante la ruptura de enlaces peptídicos dentro de las proteínas a través de un proceso de hidrólisis. Las proteasas participan en muchas funciones biológicas, como la digestión de las proteínas ingeridas, el catabolismo de las proteínas y la señalización celular. Las proteasas se encuentran en todas las formas de vida. El aspartil, la cisteína y la serina son tres proteasas importantes que desempeñan funciones clave en los organismos vivos.
Lectura relacionada: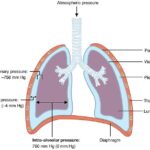 ¿Cuál es la diferencia entre presión intrapleural e intrapulmonar?
¿Cuál es la diferencia entre presión intrapleural e intrapulmonar?CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son las aspartil proteasas?
3. ¿Qué son las cisteína proteasas?
4. ¿Qué son las serina proteasas?
5. Similitudes: aspartil cisteína y serina proteasas
6. Aspartil vs cisteína vs serina proteasas en forma tabular
7. Resumen - Aspartil vs Cisteína vs Serina Proteasas
¿Qué son las aspartil proteasas?
Las aspartil proteasas son un tipo de enzima que rompe proteínas. Tienen dos aspartatos altamente conservados en el sitio activo y son óptimamente activos a pH ácido. Estas proteasas escinden enlaces dipeptídicos que contienen residuos hidrófobos y un grupo beta-metileno. El mecanismo catalítico de la aspartil proteasa es un mecanismo ácido-base. Una molécula de agua está coordinada con dos residuos de aspartato. Un aspartato activa la molécula de agua mediante la eliminación de un protón. Esto permite que el agua realice un ataque nucleofílico sobre el carbono carbonilo del sustrato. Como resultado, genera un intermedio de oxianión tetraédrico que se estabiliza mediante enlaces de hidrógeno con el segundo residuo de aspartato. El reordenamiento de este intermedio es responsable de la escisión del péptido en dos productos peptídicos.
Hay cinco superfamilias de proteasas aspárticas: Clan AA, que es una familia, Clan AC, que es una familia de peptidasas de señal II, Clan AD, que es una familia de presenilina, Clan AE, que es una familia de endopeptidasas GPR, y Clan AF, esta es una familia opcional. familia.
¿Qué son las cisteína proteasas?
Las cisteína proteasas son un grupo de enzimas hidrolasas que descomponen las proteínas. Demuestran un mecanismo catalítico que involucra un tiol de cisteína nucleofílico en una tríada o díada catalítica. El primer paso en el mecanismo catalítico de las cisteína proteasas es la desprotonación. El grupo tiol es desprotonado dentro del sitio activo de la enzima por un aminoácido vecino, como la histidina, que tiene una cadena lateral básica. El siguiente paso es el ataque nucleofílico del azufre aniónico desprotonado de la cisteína sobre el sustrato. Aquí, el fragmento del sustrato se libera con una amina y el residuo de histidina en la proteasa reconstituye su forma desprotonada. Esto conduce a la formación del intermediario tioéster del sustrato que conecta el nuevo terminal carboxi con la cisteína tiol. El enlace tioéster se hidroliza para generar un resto de ácido carboxílico en el fragmento de sustrato restante.
Lectura relacionada: ¿Cuál es la diferencia entre frotis fino y grueso?
¿Cuál es la diferencia entre frotis fino y grueso?
Figura 02: cisteína proteasa
Las cisteína proteasas juegan múltiples roles en la fisiología y el desarrollo. En las plantas, juegan un papel importante en el crecimiento, desarrollo, acumulación y movilización de proteínas de almacenamiento. En los seres humanos, son importantes para la senescencia y la apoptosis, las respuestas inmunitarias, el procesamiento de prohormonas y la remodelación de la matriz extracelular para el desarrollo de conos.
¿Qué son las serina proteasas?
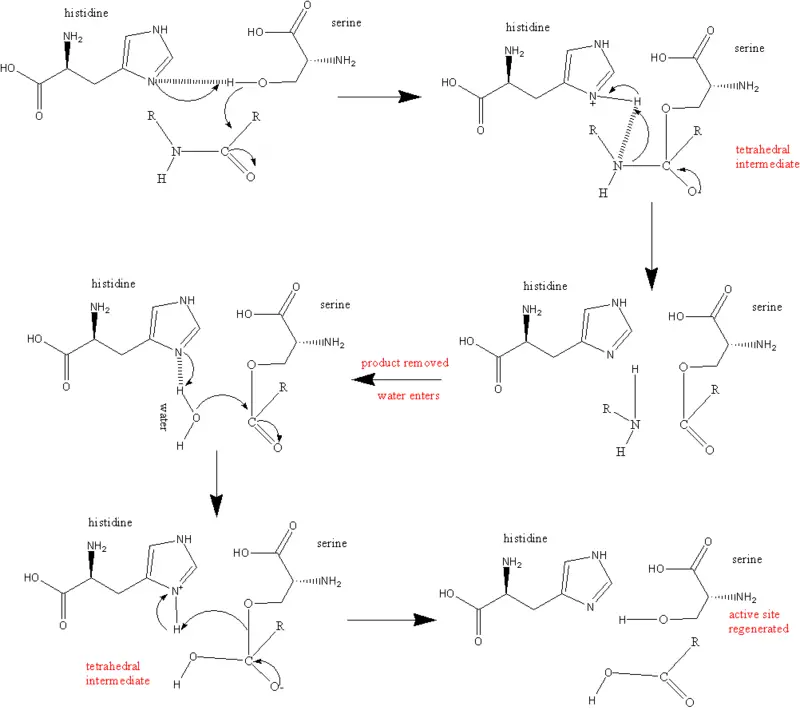
Las serina proteasas también son un grupo de enzimas proteolíticas que escinden los enlaces peptídicos en las proteínas. La serina sirve como aminoácido nucleofílico en el sitio activo de la enzima. Estos están presentes tanto en eucariotas como en procariotas. Las serina proteasas generalmente se clasifican en diferentes categorías por una estructura característica que consiste en dos dominios de barril beta que convergen en el sitio catalítico activo y también en función de su especificidad de sustrato. Son similares a la tripsina, similares a la quimotripsina, similares a la trombina, similares a la elastasa y similares a la subtilisina.

Figura 03: Serina proteasa
Las proteasas similares a la tripsina rompen los enlaces peptídicos después de un aminoácido cargado positivamente, como la lisina o la arginina. Son específicos para residuos cargados negativamente como el ácido aspártico o el ácido glutámico. Las proteasas similares a la quimotripsina son más hidrofóbicas. Su especificidad es para grandes residuos hidrófobos como tirosina, triptófano y fenilalanina. Las proteasas de tipo trombina incluyen la trombina, que es un plasminógeno activador de tejidos, y la plasmina. Estos ayudan con la coagulación de la sangre y la digestión, así como en la fisiopatología de las enfermedades neurodegenerativas. Las proteasas tipo elastasa prefieren residuos como alanina, glicina y valina. Las proteasas de tipo subtilisina incluyen serina en procariotas. Comparte un mecanismo catalítico que utiliza una tríada catalítica para generar una serina nucleófila. La regulación de la actividad de la serina proteasa requiere la activación inicial de la proteasa y la secreción de inhibidores.
¿Cuáles son las similitudes entre la aspartil cisteína y las serina proteasas?
- Las proteasas de aspartil, cisteína y serina catalizan la descomposición de las proteínas mediante la escisión de los enlaces peptídicos.
- Los mecanismos son similares cuando los residuos del sitio activo atacan los enlaces peptídicos, provocando su ruptura.
- Todos contienen nucleófilos.
- Todos son proteínas.
¿Cuál es la diferencia entre aspartil cisteína y serina proteasas?
La principal diferencia entre la aspartil cisteína y las serina proteasas depende de su grupo funcional, que actúa como residuo catalítico. En la aspartil proteasa, un grupo ácido carboxílico funciona como grupo funcional, mientras que en la cisteína proteasa, un grupo tiol o sulfhidrilo funciona como grupo funcional, y en la serina proteasa, un grupo hidroxilo o un alcohol funciona como grupo funcional.
Las aspartil proteasas tienen un sitio activo para el aspartato mientras que las cisteína proteasas tienen un sitio activo para la cisteína. El resto del sitio activo de la serina proteasa es un grupo hidroxilo. Por lo tanto, esta es también otra diferencia entre la aspartil cisteína y las serina proteasas. A diferencia de las proteasas de serina y cisteína, las proteasas de aspartil no forman un intermedio covalente durante el proceso de escisión. Por lo tanto, para las aspartil proteasas, la proteólisis ocurre en un solo paso.
La siguiente infografía tabula las diferencias entre aspartil cisteína y serina proteasas para una comparación lado a lado.
Resumen: aspartilcisteína frente a serina proteasas
Las proteasas son enzimas que catalizan la descomposición de proteínas en polipéptidos o aminoácidos más pequeños. La principal diferencia entre la aspartil cisteína y las serina proteasas es el grupo funcional que actúa como su resto catalítico. Un grupo ácido carboxílico actúa como grupo funcional en la aspartil proteasa, mientras que un grupo tiol o sulfhidrilo actúa como grupo funcional en la cisteína proteasa. Un grupo hidroxilo o un alcohol actúa como grupo funcional en la serina proteasa.
Relación:
1. "Mecanismos de proteasa". Scitable, Nature News, Nature Publishing Group.
2. "Proteasa de cisteína". ciencia directamente.
3. "Serina proteasa". ciencia directamente.
Imagen de cortesía:
1. "Mecanismo de aspartil proteasa" Por el usuario de Wikipedia en inglés Roadnottaken (CC BY-SA 3.0) a través de Commons Wikimedia
2. "Mecanismo de reacción de cisteína proteasa" por NEUROtiker - Trabajo propio (Dominio público) a través de Commons Wikimedia
3. "Mecanismo de serina proteasa de Snellios" Por Snellios en la Wikipedia en inglés (CC BY-SA 3.0) a través de Commons Wikimedia