Celdas Galvánicas o Voltaicas
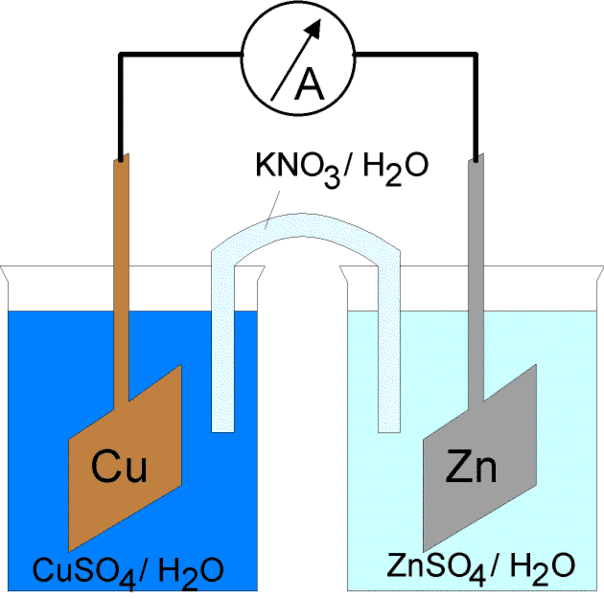
Diagrama de una celda electroquímica con un puente salino.
Cmx, Licencia de Documentación Gratuita
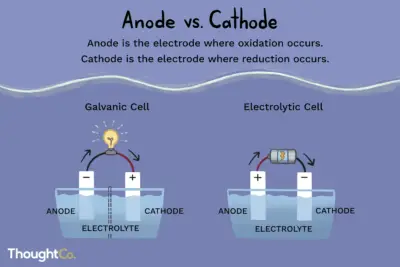
Las reacciones de oxidación-reducción o redox tienen lugar en celdas electroquímicas. Hay dos tipos de celdas electroquímicas. Las reacciones espontáneas ocurren en celdas galvánicas (voltaicas); las reacciones no espontáneas ocurren en celdas electrolíticas. Ambos tipos de células contienen electrodos donde se producen las reacciones de oxidación y reducción. La oxidación se produce en el electrodo denominado ánodo y la reducción ocurre en el electrodo llamado cátodo.
Electrodos y carga
Lectura relacionada: Cómo Funciona el Juguete Científico para Pájaros Bebedores
Cómo Funciona el Juguete Científico para Pájaros Bebedores
El ánodo de una celda electrolítica es positivo (el cátodo es negativo) ya que el ánodo atrae aniones de la solución. Sin embargo, el ánodo de una celda galvánica está cargado negativamente, ya que la oxidación espontánea en el ánodo es la fuente de los electrones o carga negativa de la célula. El cátodo de una celda galvánica es su terminal positivo. Tanto en celdas galvánicas como electrolíticas, la oxidación tiene lugar en el ánodo y los electrones fluyen desde el ánodo al cátodo.
Celdas Galvánicas o Voltaicas
La reacción redox en una celda galvánica es una reacción espontánea. Por esta razón, las celdas galvánicas se usan comúnmente como baterías. Las reacciones galvánicas de las celdas suministran energía que se utiliza para realizar el trabajo. La energía se aprovecha situando las reacciones de oxidación y reducción en recipientes separados, unidos por un aparato que permite que los electrones fluyan. Una celda galvánica común es la celda Daniell.
Lectura relacionada: Leyes de Termoquímica y Ecuaciones de Entalpía
Leyes de Termoquímica y Ecuaciones de Entalpía
Celdas Electrolíticas
Celda Electrolítica.
Todd Helmenstine
La reacción redox en una celda electrolítica es no espontánea. Se requiere energía eléctrica para inducir la reacción de electrólisis. A continuación se muestra un ejemplo de una celda electrolítica, en la que el NaCl fundido se electroliza para formar sodio líquido y cloro gaseoso. Los iones sodio migran hacia el cátodo, donde se reducen a sodio metálico. De manera similar, los iones cloruro migran al ánodo y se oxidan para formar cloro gaseoso. Este tipo de célula se utiliza para producir sodio y cloro. El gas cloro puede recogerse rodeando la celda. El sodio metálico es menos denso que la sal fundida y se elimina a medida que flota en la parte superior del recipiente de reacción.
 Cuál Es el Punto de Ebullición del Tetracloruro de Carbono?
Cuál Es el Punto de Ebullición del Tetracloruro de Carbono?