Puede suponer que las valencias de los elementos, el número de electrones con los que se unirá o formará un átomo, son los que se pueden derivar al observar los grupos (columnas) de la tabla periódica. Si bien estas son las valencias más comunes, el comportamiento real de los electrones es menos simple.
Aquí hay una tabla de valencias de elementos. Recuerde que la nube de electrones de un elemento se volverá más estable al llenar, vaciar o llenar hasta la mitad la capa. Además, las capas no se apilan ordenadamente una encima de la otra, por lo que no siempre asuma que la valencia de un elemento está determinada por el número de electrones en su capa exterior.
Lectura relacionada:
 Ejemplos de Radiación (y Lo que No es Radiación)
Ejemplos de Radiación (y Lo que No es Radiación)| Número | Elemento | Valencia |
| 1 | Hidrógeno | (-1), +1 |
| 2 | Helio | 0 |
| 3 | Litio | +1 |
| 4 | Berilio | +2 |
| 5 | Boro | -3, +3 |
| 6 | Carbono | (+2), +4 |
| 7 | Nitrógeno | -3, -2, -1, (+1), +2, +3, +4, +5 |
| 8 | Oxígeno | -2 |
| 9 | Flúor | -1, (+1) |
| 10 | Neón | 0 |
| 11 | Sodio | +1 |
| 12 | Magnesio | +2 |
| 13 | Aluminio | +3 |
| 14 | Silicio | -4, (+2), +4 |
| 15 | Fósforo | -3, +1, +3, +5 |
| 16 | Azufre | -2, +2, +4, +6 |
| 17 | Cloro | -1, +1, (+2), +3, (+4), +5, +7 |
| 18 | Argón | 0 |
| 19 | Potasio | +1 |
| 20 | Calcio | +2 |
| 21 | Escandio | +3 |
| 22 | Titanio | +2, +3, +4 |
| 23 | Vanadio | +2, +3, +4, +5 |
| 24 | Cromo | +2, +3, +6 |
| 25 | Manganeso | +2, (+3), +4, (+6), +7 |
| 26 | Hierro | +2, +3, (+4), (+6) |
| 27 | Cobalto | +2, +3, (+4) |
| 28 | Níquel | (+1), +2, (+3), (+4) |
| 29 | Cobre | +1, +2, (+3) |
| 30 | Cinc | +2 |
| 31 | Galio | (+2). +3 |
| 32 | Germanio | -4, +2, +4 |
| 33 | Arsénico | -3, (+2), +3, +5 |
| 34 | Selenio | -2, (+2), +4, +6 |
| 35 | Bromo | -1, +1, (+3), (+4), +5 |
| 36 | Criptón | 0 |
| 37 | Rubidio | +1 |
| 38 | Estroncio | +2 |
| 39 | Itrio | +3 |
| 40 | Circonio | (+2), (+3), +4 |
| 41 | Niobio | (+2), +3, (+4), +5 |
| 42 | Molibdeno | (+2), +3, (+4), (+5), +6 |
| 43 | Tecnecio | +6 |
| 44 | Rutenio | (+2), +3, +4, (+6), (+7), +8 |
| 45 | Rodio | (+2), (+3), +4, (+6) |
| 46 | Paladio | +2, +4, (+6) |
| 47 | Plata | +1, (+2), (+3) |
| 48 | Cadmio | (+1), +2 |
| 49 | Indio | (+1), (+2), +3 |
| 50 | Estaño | +2, +4 |
| 51 | Antimonio | -3, +3, (+4), +5 |
| 52 | Telurio | -2, (+2), +4, +6 |
| 53 | Yodo | -1, +1, (+3), (+4), +5, +7 |
| 54 | Xenón | 0 |
| 55 | Cesio | +1 |
| 56 | Bario | +2 |
| 57 | Lantano | +3 |
| 58 | Cerio | +3, +4 |
| 59 | Praseodimio | +3 |
| 60 | Neodimio | +3, +4 |
| 61 | Prometio | +3 |
| 62 | Samario | (+2), +3 |
| 63 | Europio | (+2), +3 |
| 64 | Gadolinio | +3 |
| 65 | Terbio | +3, +4 |
| 66 | Disprosio | +3 |
| 67 | Holmio | +3 |
| 68 | Erbio | +3 |
| 69 | Tulio | (+2), +3 |
| 70 | Iterbio | (+2), +3 |
| 71 | Lutecio | +3 |
| 72 | Hafnio | +4 |
| 73 | Tantalio | (+3), (+4), +5 |
| 74 | Tungsteno | (+2), (+3), (+4), (+5), +6 |
| 75 | Renio | (-1), (+1), +2, (+3), +4, (+5), +6, +7 |
| 76 | Osmio | (+2), +3, +4, +6, +8 |
| 77 | Iridio | (+1), (+2), +3, +4, +6 |
| 78 | Platino | (+1), +2, (+3), +4, +6 |
| 79 | Oro | +1, (+2), +3 |
| 80 | Mercurio | +1, +2 |
| 81 | Talio | +1, (+2), +3 |
| 82 | Plomo | +2, +4 |
| 83 | Bismuto | (-3), (+2), +3, (+4), (+5) |
| 84 | Polonio | (-2), +2, +4, (+6) |
| 85 | Astato | ? |
| 86 | Radón | 0 |
| 87 | Francio | ? |
| 88 | Radio | +2 |
| 89 | Actinio | +3 |
| 90 | Torio | +4 |
| 91 | Protactinio | +5 |
| 92 | Uranio | (+2), +3, +4, (+5), +6 |
Fuentes
- Brown, I. David. "El Enlace Químico en Química Inorgánica: El Modelo de Valencia del Enlace", 2a ed. Unión Internacional de Cristalografía. Oxford: Oxford Science Publications, 2016.
- Lange, Norbert A. "Manual de química de Lange", 8a ed. Editores de manuales, 1952.
- O'Dwyer, M. F., J. E. Kent y R. D. Brown. "Valencia."Nueva York: Springer-Verlag, 1978.
- Smart, Lesley E. y Elaine A. Moore. "Solid State Chemistry An Introduction", cuarta edición. Boca Ratón: CRC Press, 2016.
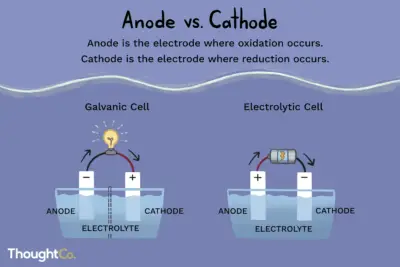
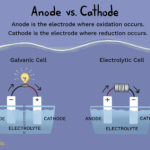 Cómo Definir Ánodo y Cátodo
Cómo Definir Ánodo y Cátodo