Que Diferencia clave entre el acetato de sodio y el trihidrato de acetato de sodio es que el acetato de sodio es un compuesto químico con la fórmula química NaCH3COO, mientras que el trihidrato de acetato de sodio es la forma hidratada más común de acetato de sodio, que consta de tres moléculas de agua unidas a una molécula de acetato de sodio.
Lectura relacionada: ¿Cuál es la diferencia entre la lidocaína y la tetracaína?
¿Cuál es la diferencia entre la lidocaína y la tetracaína?El acetato de sodio es la sal de sodio del ácido acético. El trihidrato de acetato de sodio es la forma hidratada más común de acetato de sodio.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el acetato de sodio?
3. ¿Qué es el trihidrato de acetato de sodio?
4. Acetato de sodio frente a trihidrato de acetato de sodio en forma tabular
5. Resumen - Acetato de sodio frente a trihidrato de acetato de sodio
¿Qué es el acetato de sodio?
El acetato de sodio es el compuesto químico con la fórmula química NaCH3COO. Podemos abreviarlo como NaOAc. Es la sal de sodio del ácido acético. El acetato de sodio es una sal delicuescente incolora con una amplia gama de usos.
Lectura relacionada: ¿Cuál es la diferencia entre betadina y povidona yodada?
¿Cuál es la diferencia entre betadina y povidona yodada?
Figura 01: La estructura química del acetato de sodio.
Los usos principales del acetato de sodio incluyen el uso como fuente de carbono para el cultivo de bacterias en aplicaciones biotecnológicas, uso en la industria textil para neutralizar las corrientes de desechos de ácido sulfúrico, uso en la durabilidad del concreto para migrar los daños causados por el agua al concreto al actuar como sellador de concreto en la industria alimentaria como condimento, en la fabricación de la solución tampón de acetato de sodio y ácido acético, uso en almohadillas térmicas, calentadores de manos y hielo caliente, etc.
Lectura relacionada: ¿Cuál es la diferencia entre alosterismo positivo y negativo?
¿Cuál es la diferencia entre alosterismo positivo y negativo?El acetato de sodio es un compuesto económico que generalmente se compra en lugar de una preparación de laboratorio. Podemos producir acetato de sodio en pruebas de laboratorio haciendo reaccionar ácido acético (5-8%) con carbonato de sodio, bicarbonato de sodio e hidróxido de sodio. Estas reacciones pueden producir acetato de sodio y agua.
Mirando la estructura química del acetato de sodio, tiene una estructura cristalina en forma anhidra. Podemos describirlo como capas alternas de carboxilato de sodio y grupos metilo. Este compuesto se puede descarboxilar en condiciones forzadas para formar metano.
¿Qué trihidrato de acetato de sodio?
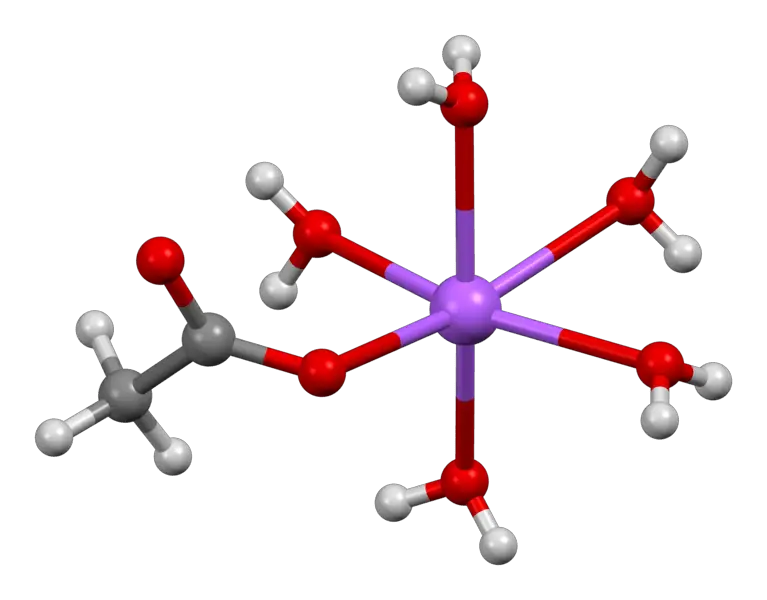
El trihidrato de acetato de sodio es la forma hidratada más común de acetato de sodio. Tiene tres moléculas de agua unidas a una molécula de acetato de sodio.

Figura 02: La estructura química del trihidrato de acetato de sodio.
La estructura de este compuesto contiene una coordinación octaédrica distorsionada en el ion de sodio. Aparece como una estructura de cadena unidimensional.
¿Cuál es la diferencia entre el acetato de sodio y el trihidrato de acetato de sodio?
El acetato de sodio es la sal de sodio del ácido acético. El trihidrato de acetato de sodio es la forma hidratada más común de acetato de sodio. La diferencia clave entre el acetato de sodio y el trihidrato de acetato de sodio es que el acetato de sodio es el compuesto químico con la fórmula química NaCH3COO, mientras que el trihidrato de acetato de sodio es la forma hidratada más común de acetato de sodio, que se compone de tres moléculas de agua unidas a un acetato de sodio. molécula.
Hay muchos usos del acetato de sodio, incluido el uso como fuente de carbono para el cultivo de bacterias en aplicaciones biotecnológicas, el uso en la industria textil para neutralizar las corrientes de desechos de ácido sulfúrico, el uso en la durabilidad del concreto para ayudar a que los daños causados por el agua migren al concreto al usarlo como sellador de concreto. usos como agente aromatizante en la industria alimentaria, etc. Los usos del trihidrato de acetato de sodio incluyen como fuente de iones de sodio en soluciones, para diálisis, como agente alcalinizante sistémico y urinario, como diurético y como expectorante.
La siguiente infografía enumera las diferencias entre el acetato de sodio y el trihidrato de acetato de sodio en forma tabular para una comparación en paralelo.
Resumen: acetato de sodio frente a trihidrato de acetato de sodio
El acetato de sodio y el trihidrato de acetato de sodio son sales de sodio del ácido acético. La diferencia clave entre el acetato de sodio y el trihidrato de acetato de sodio es que el acetato de sodio es el compuesto químico con la fórmula química NaCH3COO, mientras que el trihidrato de acetato de sodio es la forma hidratada más común de acetato de sodio, que se compone de tres moléculas de agua unidas a un acetato de sodio. molécula.
Relación:
1. “Trihidrato de acetato de sodio”. Centro Nacional de Información Biotecnológica. Base de datos de conexión de PubChemBiblioteca Nacional de Medicina de EE.
Imagen de cortesía:
1. "Esqueleto 2D de acetato de sodio" (Dominio público) a través de Commons Wikimedia
2. "Sodio-acetato-trihidrato-xtal-Na-coordinación-3D-bs-17" por Ben Mills - Trabajo propio (Dominio público) a través de Commons Wikimedia