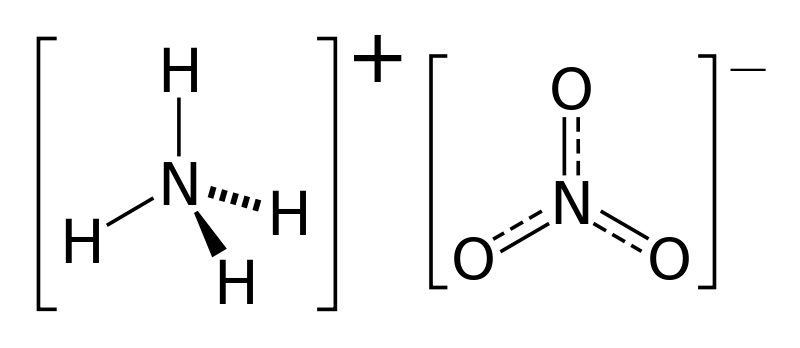Que Diferencia clave entre el nitrato de amonio y el sulfato de amonio. es que el nitrato de amonio se forma a partir de la reacción entre el amoníaco y el ácido nítrico, mientras que el sulfato de amonio se forma a partir de la reacción entre el amoníaco y el ácido sulfúrico.
Lectura relacionada: ¿Cuál es la diferencia entre acetilcisteína y N-acetilcisteína?
¿Cuál es la diferencia entre acetilcisteína y N-acetilcisteína?El nitrato de amonio es un compuesto inorgánico con la fórmula química NH4NO3 y el sulfato de amonio es un compuesto inorgánico con la fórmula química (NH4) 2SO4. Ambos son sales de amoníaco con un olor fuerte e irritante.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el nitrato de amonio?
3. ¿Qué es el sulfato de amonio?
4. Nitrato de amonio versus sulfato de amonio en forma tabular
5. Resumen: nitrato de amonio frente a sulfato de amonio
¿Qué es el nitrato de amonio?
El nitrato de amonio es un compuesto inorgánico con la fórmula química NH4NO3. Esta sustancia es una sal compuesta por un catión amonio y un anión nitrato. Además, aparece como un sólido blanco a temperatura ambiente y puede disolverse fácilmente en agua. Además, el nitrato de amonio se presenta como un mineral natural en la naturaleza.
Lectura relacionada: ¿Cuál es la diferencia entre el gluconato ferroso y el fumarato ferroso?
¿Cuál es la diferencia entre el gluconato ferroso y el fumarato ferroso?
Figura 01: La estructura química del nitrato de amonio.
Algunos datos químicos sobre este compuesto son los siguientes:
Lectura relacionada: ¿Cuál es la diferencia entre el alcohol cetílico y el alcohol cetoestearílico?
¿Cuál es la diferencia entre el alcohol cetílico y el alcohol cetoestearílico?- La masa molar es 80.043 g/mol.
- Aparece como un sólido blanco o gris
- El punto de fusión es 169,6 °C
- Se descompone por encima de 210 °C
- La estructura cristalina del compuesto es trigonal.
El principal uso de los compuestos de nitrato de amonio es en la agricultura; es muy útil como fertilizante con alto contenido de nitrógeno. Aparte de eso, podemos usarlo para crear mezclas explosivas para minería y canteras. Debido a que la disolución de este compuesto en agua es altamente endotérmica, también es útil en algunas bolsas de frío instantáneo.
¿Qué es el sulfato de amonio?
El sulfato de amonio es un compuesto inorgánico con la fórmula química (NH4)2SO4. Por lo general, consiste en un catión de amonio unido a un anión de sulfato. Por lo tanto, este compuesto tiene dos cationes de amonio por anión sulfato. Es una sal de sulfato inorgánico con muchos usos importantes.

Figura 02: La estructura química del sulfato de amonio.
La masa molar del sulfato de amonio es 132,14 g/mol. Este compuesto se presenta como gránulos o cristales finos e higroscópicos. Además, el punto de fusión de este compuesto puede oscilar entre 235 y 280 °C; Por encima de este rango de temperatura, el compuesto tiende a descomponerse. Podemos hacer compuestos de sulfato de amonio tratando el amoníaco con ácido sulfúrico. Para esta preparación podemos utilizar una mezcla de gas amoníaco y vapor de agua en un reactor. Además, necesitamos poner ácido sulfúrico concentrado en este reactor, y luego la reacción entre estos componentes formará sulfato de amonio.
Si consideramos los usos del sulfato de amonio, podemos usarlo como fertilizante, principalmente para suelos alcalinos. Además, podemos utilizarlo para producir insecticida, herbicida, fungicida, etc. Además, utilizamos este compuesto para purificar proteínas por precipitación en el laboratorio bioquímico. También es útil como aditivo alimentario.
¿Cuál es la diferencia entre el nitrato de amonio y el sulfato de amonio?
El nitrato de amonio y el sulfato de amonio son sales de amonio. La diferencia clave entre el nitrato de amonio y el sulfato de amonio es que el nitrato de amonio se forma a partir de la reacción entre el amoníaco y el ácido nítrico, mientras que el sulfato de amonio se forma a partir de la reacción entre el amoníaco y el ácido sulfúrico. Además, el nitrato de amonio está disponible como un sólido cristalino blanco, mientras que el sulfato de amonio está disponible como polvo fino, gránulos o cristales higroscópicos.
La siguiente infografía muestra las diferencias entre el nitrato de amonio y el sulfato de amonio en forma tabular para una comparación directa.
Resumen: nitrato de amonio frente a sulfato de amonio
El nitrato de amonio es un compuesto inorgánico con la fórmula química NH4NO3, mientras que el sulfato de amonio es un compuesto inorgánico con la fórmula química (NH4) 2SO4. La diferencia clave entre el nitrato de amonio y el sulfato de amonio es que el nitrato de amonio se forma a partir de la reacción entre el amoníaco y el ácido nítrico, mientras que el sulfato de amonio se forma a partir de la reacción entre el amoníaco y el ácido sulfúrico.
Relación:
1. "Nitrato de amonio". Centro Nacional de Información Biotecnológica. Base de datos de conexión de PubChemBiblioteca Nacional de Medicina de EE.
Imagen de cortesía:
1. "Nitrato de amonio-2D" por Mikayé - Trabajo propio basado en: Nitrato de amonio-2D.png (Dominio público) a través de Commons Wikimedia
2. "Sulfato de amonio" por Edgar181 - Trabajo propio (Dominio público) a través de Commons Wikimedia