Que diferencia principal entre ácidos binarios y ácidos poliatómicos que es Los ácidos binarios contienen átomos de solo dos elementos químicos diferentes, mientras que los ácidos poliatómicos contienen átomos de dos o más elementos químicos diferentes..
Lectura relacionada: Diferencia entre acetamida y benzamida.
Diferencia entre acetamida y benzamida.Un ácido es un compuesto químico inorgánico que puede neutralizar una sustancia alcalina. Los ácidos pueden disolver la mayoría de los metales. Podemos identificar fácilmente un ácido usando papel tornasol: el tornasol azul cambia de color a rojo cuando se sumerge en un ácido. Hay diferentes tipos de ácidos; Dos de estos tipos son los ácidos binarios y los ácidos poliatómicos.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los ácidos binarios?
3. ¿Qué son los ácidos poliatómicos?
4. Comparación lado a lado: ácidos binarios frente a ácidos poliatómicos en forma tabular
5. Resumen
¿Qué son los ácidos binarios?
Los ácidos binarios son sustancias inorgánicas que están unidas por hidrógeno a otro elemento químico. Este segundo elemento químico suele ser un elemento no metálico. El término "binario" se refiere a una sustancia con "dos" componentes de algo; en este contexto son dos elementos químicos diferentes. La acidez de estas sustancias surge debido a su capacidad para liberar hidrógeno como catión o protón, provocando la acidez de su solución acuosa. Los ácidos binarios más comunes son el ácido fluorhídrico (HF), el ácido clorhídrico (HCl) y el ácido bromhídrico (HBr). Además, los ácidos binarios pueden tener uno o más átomos de hidrógeno por molécula dependiendo de la valencia del no metal unido a los átomos de hidrógeno, por ejemplo, H2S.
Lectura relacionada: Diferencia entre redox intramolecular y reacción redox desproporcionada
Diferencia entre redox intramolecular y reacción redox desproporcionada
Figura 01: Cloruro de hidrógeno
Los ácidos binarios pueden ser ácidos fuertes, ácidos débiles o moderadamente ácidos. Esta fuerza ácida depende de la fuerza del enlace covalente entre un átomo de hidrógeno y un átomo no metálico. Dado que todos los ácidos binarios contienen átomos de hidrógeno, el nombre del ácido binario comienza con "hidro-".
Lectura relacionada: Diferencia entre Midol y Tylenol
Diferencia entre Midol y Tylenol¿Qué son los ácidos poliatómicos?
Los ácidos poliatómicos son compuestos inorgánicos que contienen átomos con dos o más elementos químicos diferentes. Sin embargo, los iones que se forman a partir de la disociación de un ácido poliatómico pueden ser monoatómicos o poliatómicos, ya que algunos ácidos poliatómicos tienen solo dos elementos químicos distintos y la eliminación de un átomo de hidrógeno forma un ion monoatómico.

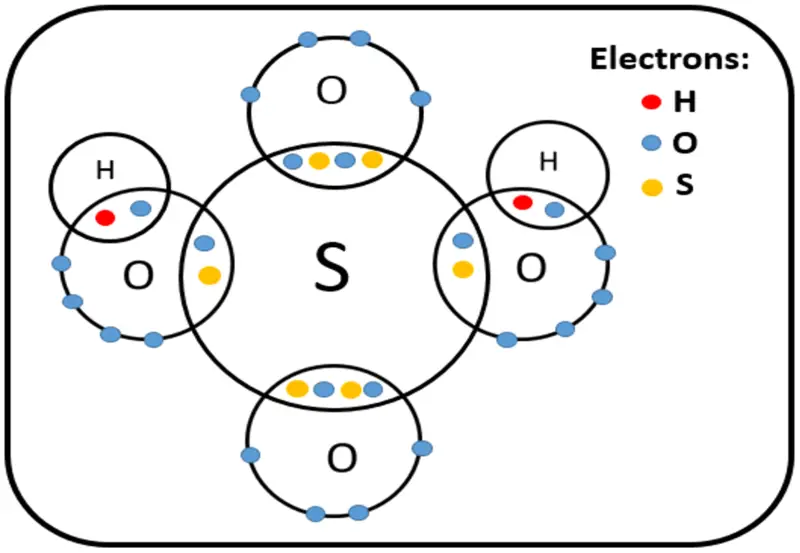
Figura 02: Estructura del ácido sulfúrico
Algunos ejemplos comunes de ácidos poliatómicos son el ácido carbónico (H2CO3), el ácido sulfúrico (H2SO4), el ácido sulfuroso (H2SO3), el ácido nítrico (HNO3), etc.
¿Cuál es la diferencia entre los ácidos binarios y los ácidos poliatómicos?
Un ácido es una sustancia que puede neutralizar una sustancia alcalina. La diferencia clave entre los ácidos binarios y los ácidos poliatómicos es que los ácidos binarios contienen átomos de solo dos elementos químicos diferentes, mientras que los ácidos poliatómicos contienen átomos de dos o más elementos químicos diferentes.
Además, los ácidos binarios siempre forman una base conjugada monoatómica, mientras que los ácidos poliatómicos pueden formar una base conjugada monoatómica o una base poliatómica. Además, los ácidos binarios suelen ser ácidos fuertes a moderadamente fuertes. El ácido fluorhídrico (HF), el ácido clorhídrico (HCl) y el ácido bromhídrico (HBr) son algunos ejemplos de ácidos binarios. Los ácidos poliatómicos, por otro lado, pueden ser ácidos fuertes, ácidos débiles o compuestos moderadamente ácidos. Algunos ejemplos son el ácido carbónico (H2CO3), el ácido sulfúrico (H2SO4) y el ácido nítrico (HNO3).
La siguiente infografía enumera, una al lado de la otra, las diferencias entre los ácidos binarios y los ácidos poliatómicos.

Resumen: ácidos binarios frente a ácidos poliatómicos
Podemos identificar fácilmente los ácidos de los papeles de tornasol; El tornasol azul se vuelve rojo cuando se sumerge en un ácido. Hay diferentes tipos de ácidos, como los ácidos binarios y los ácidos poliatómicos. La diferencia clave entre los ácidos binarios y los ácidos poliatómicos es que los ácidos binarios contienen átomos de solo dos elementos químicos diferentes, mientras que los ácidos poliatómicos contienen átomos de dos o más elementos químicos diferentes.
Relación:
1. Helmenstine, Anne Marie. "¿Qué son los ácidos y las bases?" ThoughtCo, 26 de agosto de 2020, disponible aquí.
2. "5.9: Nomenclatura de ácidos". Chemistry LibreTexts, Libretexts, 20 de noviembre de 2020, disponible aquí.
Imagen de cortesía:
1. "Dimensiones 2D de cloruro de hidrógeno" (Dominio público) a través de Commons Wikimedia
2. "Foto H2so4" por Jadder1224 - Trabajo propio (CC BY-SA 4.0) a través de Commons Wikimedia