Que diferencia principal entre calcinación y pirólisis La calcinación ocurre en presencia de una cantidad limitada de aire u oxígeno, mientras que la pirólisis ocurre en ausencia de aire.
Lectura relacionada: Diferencia entre mecanismo asociativo y disociativo.
Diferencia entre mecanismo asociativo y disociativo.La calcinación y la pirólisis son dos formas de reacciones de combustión que difieren según la cantidad de aire presente en la mezcla de reacción durante la reacción de combustión. La calcinación es un proceso químico en pirometalurgia que consiste en calentar el mineral metálico en presencia de aire u oxígeno limitados. La pirólisis, por otro lado, es una reacción de descomposición química en la que los materiales orgánicos se descomponen en ausencia de oxígeno.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la calcinación?
3. ¿Qué es la pirólisis?
4. Comparación lado a lado: calcinación y pirólisis en forma tabular
5. Resumen
que es calcinacion
La calcinación es un proceso químico en pirometalurgia que consiste en calentar el mineral metálico en presencia de aire u oxígeno limitados. Al calcinar, tenemos que calentar el mineral a una temperatura por debajo de su punto de fusión. Este es un proceso muy útil. El nombre calcinación proviene de un nombre latino debido a su aplicación principal: calentar minerales de carbonato de calcio.
Lectura relacionada: Diferencia entre complejos inertes y lábiles.
Diferencia entre complejos inertes y lábiles.
Figura 01: Calcinación
Podemos realizar el proceso de calcinación en un reactor que tenga una estructura cilíndrica; lo llamamos el calcinador. La calcinación tiene lugar en este reactor calcinador en condiciones controladas. Durante la calcinación, se forma y libera dióxido de carbono, y el carbonato de calcio se convierte en óxido de calcio. Este proceso de calcinación es importante, principalmente para eliminar las impurezas volátiles. Sin embargo, a veces tenemos que usar un horno para la calcinación porque implica calentar una sustancia a temperaturas muy altas.
Lectura relacionada: Diferencia entre espinela y estructura de espinela inversa.
Diferencia entre espinela y estructura de espinela inversa.Un buen ejemplo de calcinación es la producción de cal a partir de piedra caliza. Durante este proceso, necesitamos calentar la piedra caliza a una temperatura alta, es decir, una temperatura lo suficientemente alta como para formar y liberar gas de dióxido de carbono. La cal se forma en un estado ligeramente pulverulento.
¿Qué es la pirólisis?
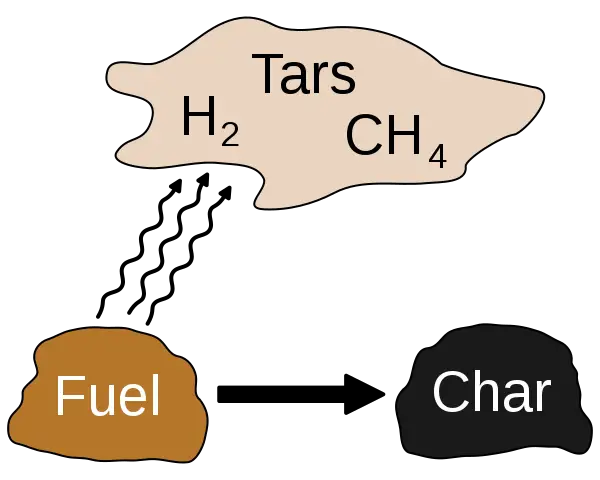
La pirólisis es una reacción de descomposición química en la que los materiales orgánicos se descomponen en ausencia de oxígeno. Debemos aplicar calor para que esta reacción progrese. Por lo tanto, podemos aumentar la velocidad de reacción aumentando la cantidad de calor proporcionada. Generalmente, la pirólisis ocurre a 430 o másOLa mayoría de las veces, sin embargo, podemos llevar a cabo estas reacciones casi sin oxígeno, ya que es muy difícil obtener una atmósfera libre de oxígeno. El producto final de esta reacción está en fase gaseosa, fase líquida o fase sólida. Normalmente se forman gases durante este proceso. Cuando se forma un líquido, lo llamamos “alquitrán”. Si es un sólido, normalmente puede ser carbón vegetal o biocarbón.

Figura 02: Pirólisis
Muy a menudo, la pirólisis convierte la materia orgánica en sus componentes gaseosos, un residuo sólido de carbón y cenizas, y un líquido llamado aceite de pirólisis. Utilizamos dos métodos principales para eliminar las impurezas de una sustancia; destrucción y remoción. El proceso de destrucción descompone los contaminantes en pequeños compuestos, mientras que el proceso de eliminación separa los contaminantes de la sustancia deseada.
Esta reacción se utiliza en diversas industrias para producir carbón vegetal, carbón activado, metanol, etc. Además, puede destruir compuestos orgánicos semivolátiles, combustibles, etc. También podemos utilizar este proceso para tratar los residuos orgánicos de las fábricas.
¿Cuál es la diferencia entre calcinación y pirólisis?
La calcinación y la pirólisis son reacciones químicas importantes. La principal diferencia entre la calcinación y la pirólisis es que la calcinación se lleva a cabo en presencia de una cantidad limitada de aire u oxígeno, mientras que la pirólisis se lleva a cabo en ausencia de aire. La calcinación se usa para producir cal a partir de piedra caliza, mientras que la pirólisis se usa para producir carbón vegetal, carbón activado, metanol, etc.
La siguiente infografía resume las diferencias entre la calcinación y la pirólisis.

Resumen: calcinación frente a pirólisis
La calcinación y la pirólisis son reacciones químicas importantes. La principal diferencia entre la calcinación y la pirólisis es que la calcinación se lleva a cabo en presencia de una cantidad limitada de aire u oxígeno, mientras que la pirólisis se lleva a cabo en ausencia de aire.
Relación:
1. Helmenstine, Annemarie. "Definición de tostado en química". ThoughtCo, 11 de febrero de 2020, disponible aquí.
Imagen de cortesía:
1. "LDLimeShaftKilnBasic" por LinguisticDemographer - Originalmente de en.wikipedia. (Dominio público) a través de Commons Wikimedia
2. "Pirólisis" por Mintrick en Wikipedia en inglés (CC BY-SA 3.0) a través de Commons Wikimedia