Que diferencia principal entre complejos planos cuadrados y tetraédricos es que los complejos planos cuadrados tienen un diagrama de campo cristalino de cuatro niveles, pero los complejos tetraédricos tienen un diagrama de campo cristalino de dos niveles.
Lectura relacionada: Diferencia entre epimerización y racemización.
Diferencia entre epimerización y racemización.La teoría del campo cristalino es una teoría de la química que describe la ruptura de los orbitales electrónicos (principalmente los orbitales d y f) debido al campo eléctrico estático creado por la carga aniónica alrededor de un átomo. La teoría es muy importante para describir las propiedades de los complejos de metales de transición. También podemos describir las estructuras de complejos cuadrados-planos y tetraédricos.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los complejos cuadrados-planares?
3. ¿Qué son los complejos tetraédricos?
4. Comparación lado a lado - complejos cuadrados-planares vs tetraédricos en forma tabular
5. Resumen
¿Qué son los complejos cuadrados-planares?
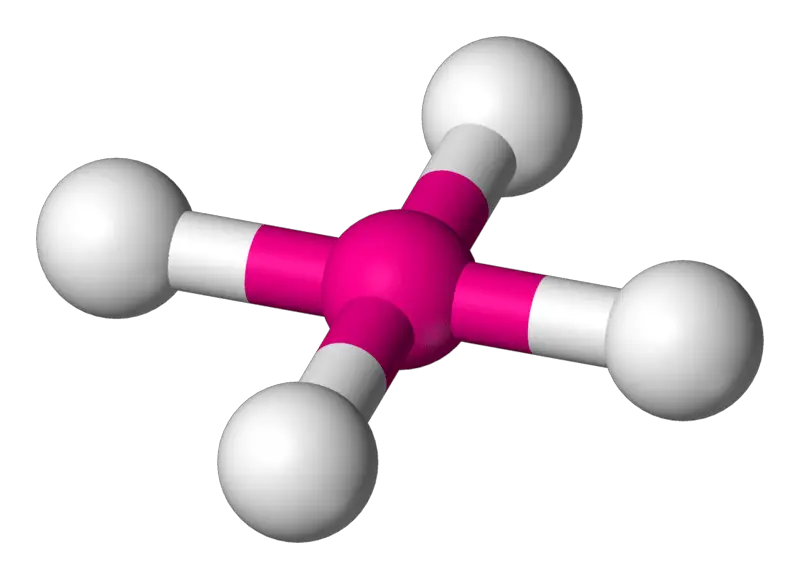
Los complejos planos cuadrados son complejos de coordinación que presentan un átomo de metal central rodeado por cuatro átomos constituyentes en las esquinas del mismo plano cuadrado. Los ángulos de enlace de los enlaces en esta estructura son 90°. Metales de transición con la configuración electrónica al final d8 formar complejos de coordinación con esta geometría molecular. Por ejemplo, Rh(I), Ir(I), Pd(II), etc. El número de coordinación para un complejo cuadrado-planar es cuatro.
 Diferencia entre cianuro y nitrilo.
Diferencia entre cianuro y nitrilo.Podemos describir la estructura de estos complejos utilizando la teoría del campo cristalino (CFT). De acuerdo con esta teoría, un complejo planar cuadrado tiene un diagrama de campo cristalino de cuatro niveles. Y esta división de cuatro niveles se llama D4 horas. Los cuatro niveles de energía resultantes se denotan por dx2-y2es decirxyes decirz2y [dxz, dyz]. Además, existe una relación específica entre la geometría plana cuadrada y la geometría tetraédrica. Podemos transformar una geometría tetraédrica en una geometría plana cuadrada aplanando el tetraedro. Y esta transformación proporciona una ruta para la isomerización de los complejos tetraédricos.
¿Qué son los complejos tetraédricos?
Los complejos tetraédricos son complejos de coordinación con un átomo central de metal rodeado por cuatro átomos constituyentes en las esquinas de un tetraedro. Los ángulos de enlace de los enlaces en esta estructura son de aproximadamente 109,5°. Sin embargo, cuando los componentes son diferentes entre sí, los ángulos de enlace varían. Hay dos tipos de metales de transición que pueden formar este tipo de complejo: metales con d0 configuración y d10 Construcción.
Además, según la teoría del campo cristalino, los complejos tetraédricos tienen un diagrama de campo cristalino de dos niveles. Los dos niveles de energía de este diagrama implican dos conjuntos de orbitales: ixyes decirxzes decirSí en un nivel de energía y dx2-y2es decirz2 en la otra oración.
Lectura relacionada: Diferencia entre alcanos de cadena lineal y de cadena ramificada
Diferencia entre alcanos de cadena lineal y de cadena ramificada¿Cuál es la diferencia entre los complejos cuadrado-planar y tetraédrico?
La teoría del campo cristalino es muy importante para describir las propiedades de los complejos de metales de transición, así como las estructuras de los complejos cuadrados-planos y tetraédricos. La principal diferencia entre los complejos planos cuadrados y tetraédricos es que los complejos planos cuadrados tienen un diagrama de campo cristalino de cuatro niveles, pero los complejos tetraédricos tienen un diagrama de campo cristalino de dos niveles.
Además, son metales de transición cuyas configuraciones electrónicas terminan en d8 configuración tienden a formar complejos planares cuadrados, mientras que los metales con d0 configuración y d10 configuración tienden a formar complejos tetraédricos.
La siguiente infografía muestra más comparaciones con respecto a la diferencia entre los complejos tetraédricos y planos cuadrados.

Resumen - Cuadrado-Planar vs. Complejos Tetraédricos
La teoría del campo cristalino es muy importante para describir las propiedades de los complejos de metales de transición. También podemos describir las estructuras de complejos cuadrados-planos y tetraédricos. La diferencia clave entre los complejos planos cuadrados y tetraédricos es que los complejos planos cuadrados exhiben un diagrama de campo cristalino de cuatro niveles, mientras que los complejos tetraédricos exhiben un diagrama de campo cristalino de dos niveles.
Relación:
1. Mott, Vallerie. "Introducción a la Química". Lúmenes, Disponible aquí.
2. "Enlace en compuestos de coordinación: teoría del campo cristalino". Química ilimitada, lúmenes, disponible aquí.
3. "Teoría del campo cristalino". LibreTexts, disponible aquí.
Imagen de cortesía:
1. "Bolas planas cuadradas en 3D" (Dominio público) a través de Commons Wikimedia
2. "Esferas 3D tetraédricas" (Dominio público) a través de Commons Wikimedia