Que diferencia principal entre complejos homolépticos y heterolépticos los complejos homolépticos tienen ligandos idénticos unidos a un centro metálico, mientras que los complejos heterolépticos tienen al menos un ligando diferente unido al centro metálico del complejo.
Lectura relacionada: Diferencia entre metil acetileno y acetileno.
Diferencia entre metil acetileno y acetileno.Los términos complejos homolépticos y heterolépticos pertenecen a la química inorgánica, donde analizamos los complejos de metales de transición. Estos dos tipos de complejos difieren entre sí según la naturaleza de los ligandos unidos al centro metálico.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los complejos homolépticos?
3. ¿Qué son los complejos heterolépticos?
4. Comparación lado a lado: complejos homolépticos frente a heterolépticos en forma tabular
5. Resumen
¿Qué son los complejos homolépticos?
Los complejos homolépticos son compuestos químicos que contienen ligandos idénticos unidos a un centro metálico. Encontramos este término en química inorgánica cuando se trata de complejos de metales de transición. El prefijo "homo-" significa "igual para todos".
Lectura relacionada: Diferencia entre reacción eutéctica y eutectoide.
Diferencia entre reacción eutéctica y eutectoide.
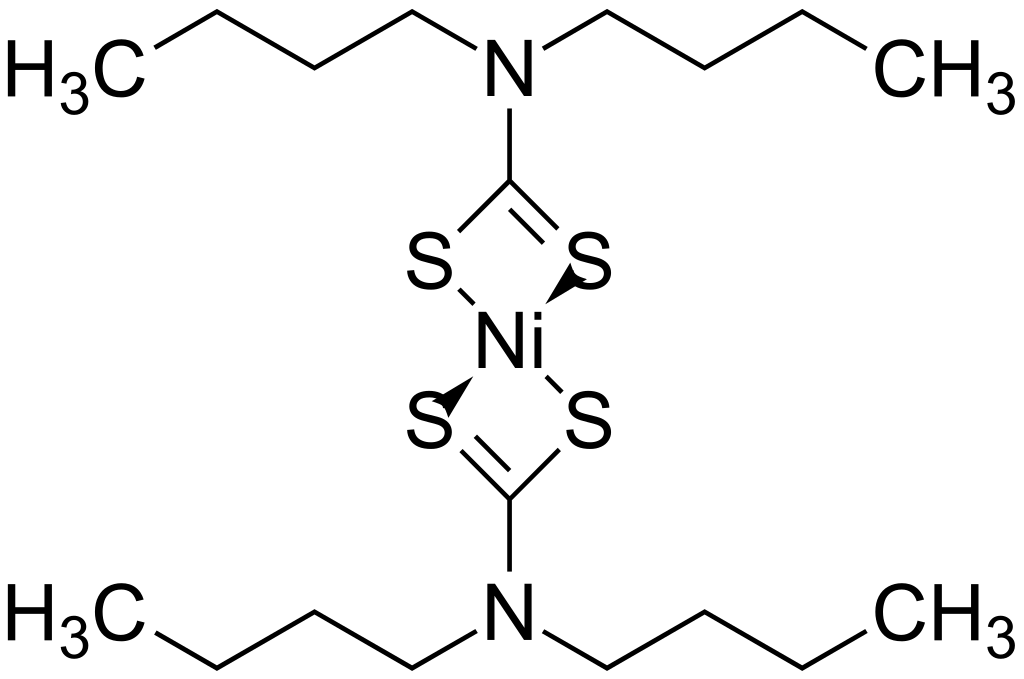
Figura 01: Un complejo homoléptico con dos ligandos similares unidos al mismo centro metálico
Un ejemplo común de tal complejo es un complejo de dialquilmagnesio presente en una solución del reactivo de Grignard en un éter, con dos ligandos de éter unidos a cada centro de magnesio. Otro ejemplo de complejo homoléptico es el trimetilaluminio en un éter como el THF. Este complejo contiene tres grupos metilo unidos a un ion metálico de aluminio central con una carga positiva +3. De manera similar, el triarilo o el trialquil borano son complejos homolépticos.
Lectura relacionada: Diferencia entre ácido oxálico y ácido acético.
Diferencia entre ácido oxálico y ácido acético.¿Qué son los complejos heterolépticos?
Los complejos heterolépticos son compuestos químicos que contienen al menos un ligando diferente unido al centro metálico. Algunos ligandos involucrados en la formación de complejos de metales de transición, como el DMSO, son capaces de unirse con dos o más modos de coordinación diferentes. En tal caso, consideramos que el complejo metálico es homoléptico, con un solo tipo de ligando con diferentes modos de coordinación.

Figura 02: Un complejo heteroléptico con cinco ligandos similares y un ligando diferente
Un ejemplo común de un complejo heteroléptico es el complejo de cobalto (III) con cuatro ligandos de amoníaco y dos ligandos de cloruro. El término complejo polinuclear, por otro lado, difiere del término complejo heteroléptico porque los complejos polinucleares son complejos de metales de transición que tienen dos o más centros metálicos con ligandos unidos. Sin embargo, también es un tipo de complejo heteroléptico cuando los ligandos unidos a los centros metálicos son diferentes entre sí.
¿Cuál es la diferencia entre los complejos homolépticos y heterolépticos?
Los términos complejos homolépticos y heterolépticos pertenecen a la química inorgánica, donde analizamos los complejos de metales de transición. Estos dos tipos de complejos difieren entre sí según la naturaleza de los ligandos unidos al centro metálico. La diferencia clave entre los complejos homolépticos y heterolépticos es que los complejos homolépticos tienen ligandos idénticos unidos a un centro metálico, mientras que los complejos heterolépticos tienen al menos un ligando diferente unido al centro metálico del complejo. Además, los complejos homolépticos son menos complejos que los complejos heterolépticos.
A continuación se muestra una tabla resumen de la diferencia entre los complejos homolépticos y heterolépticos.

Resumen: complejos homolépticos frente a heterolépticos
Los términos complejos homolépticos y heterolépticos pertenecen a la química inorgánica, donde analizamos los complejos de metales de transición. Estos dos tipos de complejos difieren entre sí según la naturaleza de los ligandos unidos al centro metálico. La diferencia clave entre los complejos homolépticos y heterolépticos es que los complejos homolépticos tienen ligandos idénticos unidos a un centro metálico, mientras que los complejos heterolépticos tienen al menos un ligando diferente unido al centro metálico del complejo.
Relación:
1. "Complejos heterolépticos". Química de coordinación de ácidos hidroxámicos, 14 de diciembre de 2014, disponible aquí.
2. "Homoléptico". Wikipedia, Fundación Wikimedia, 7 de junio de 2020, disponible aquí.
Imagen de cortesía:
1. "Dibutilcarbamoditioato de níquel (II) 200" por Emeldir (conferencia) - Trabajo propio (Dominio público) a través de Commons Wikimedia
2. "RuA5N2" de Smokefoot - Trabajo propio (Dominio público) a través de Commons Wikimedia