Que diferencia principal entre los hidruros iónicos covalentes y los metálicos es su formación. Los hidruros iónicos se forman cuando el hidrógeno reacciona con elementos de bloque s fuertemente electropositivos; Los hidruros covalentes se forman cuando los átomos de elementos químicos con valores comparables de electronegatividad reaccionan con el hidrógeno, mientras que los hidruros metálicos se forman cuando los metales de transición reaccionan con el hidrógeno.
Lectura relacionada: Diferencia entre hiperconjugación isovalente y de sacrificio.
Diferencia entre hiperconjugación isovalente y de sacrificio.Un hidruro es un compuesto químico que contiene un anión de hidrógeno, H-. Hay tres tipos principales de hidruros como hidruros iónicos, covalentes y metálicos según el tipo de elemento químico que se une al anión de hidrógeno.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los hidruros iónicos?
3. ¿Qué son los hidruros covalentes?
4. ¿Qué son los hidruros metálicos?
5. Comparación lado a lado: hidruros iónicos, covalentes y metálicos en forma tabular
6. Resumen
¿Qué son los hidruros iónicos?
Los hidruros iónicos son compuestos químicos de hidruro que contienen un anión de hidrógeno unido a un catión de bloque S fuertemente electropositivo. Estas conexiones también se denominan hidruros salinos o pseudohaluros. La combinación de hidrógeno y los metales más activos de los grupos de metales alcalinos y alcalinotérreos forma este tipo de compuesto hidruro. En estos compuestos, el hidrógeno se encuentra en un estado de oxidación negativo con el número de oxidación -1. Los hidruros iónicos suelen ser compuestos binarios, donde solo hay dos elementos químicos en una sola molécula. Además, estos compuestos suelen ser insolubles en soluciones.
Lectura relacionada: Diferencia entre galio y mercurio.
Diferencia entre galio y mercurio.¿Qué son los hidruros covalentes?
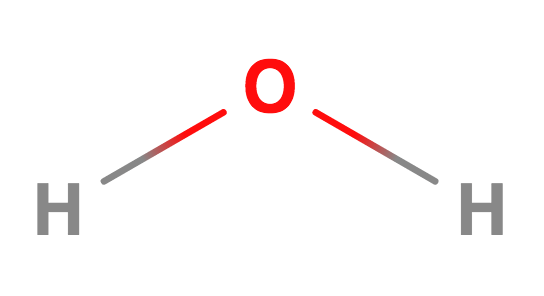
Los hidruros covalentes son compuestos químicos de hidruro que contienen un anión de hidrógeno unido a un elemento químico electronegativo similar. En estos compuestos hay un átomo de hidrógeno y uno o más átomos no metálicos que forman el compuesto.

Figura 01: La molécula de agua es un compuesto de hidruro covalente.
Lectura relacionada: Diferencia entre formaldehído y glutaraldehído
Diferencia entre formaldehído y glutaraldehídoExiste un enlace químico covalente entre el átomo de hidrógeno y el elemento químico más electropositivo. Este enlace químico se forma cuando dos átomos comparten sus electrones de valencia. Estos compuestos pueden ser volátiles o no volátiles.
Los hidruros metálicos son compuestos químicos de hidruro que contienen un anión de hidrógeno unido a elementos de metales de transición. Estas conexiones también se denominan hidruros intersticiales. Como rasgo característico de estos compuestos, podemos observar que son compuestos no estequiométricos. Es decir, la proporción de átomos de hidrógeno a átomos de metal en el compuesto no es fija. En otras palabras, estos compuestos tienen una composición atómica variable.
Un hidruro es un compuesto químico que contiene un anión de hidrógeno, H-. Podemos clasificar los hidruros en tres tipos principales según la naturaleza del elemento químico que se une al anión de hidrógeno: hidruros iónicos, covalentes y metálicos. Por lo tanto, la principal diferencia entre los hidruros iónicos covalentes y metálicos es el tipo de elemento químico unido al anión de hidrógeno. Los hidruros iónicos se forman cuando el hidrógeno reacciona con elementos de bloque s fuertemente electropositivos, y los hidruros covalentes se forman cuando átomos de elementos químicos con valores de electronegatividad comparables reaccionan con hidrógeno. Mientras tanto, los hidruros metálicos se forman cuando los metales de transición reaccionan con el hidrógeno.
Además, los hidruros iónicos son una combinación de hidrógeno con un átomo fuertemente electropositivo en un grupo alcalino o alcalinotérreo, mientras que los hidruros covalentes son una combinación de hidrógeno con un no metal electronegativo comparable. Sin embargo, los hidruros metálicos son una combinación de hidrógeno con un metal de transición.
La siguiente infografía resume las diferencias entre los hidruros iónico-covalentes y metálicos en forma tabular.

Resumen: hidruros iónicos, covalentes y metálicos
Hay tres tipos principales de hidruros: hidruros iónicos, covalentes y metálicos. los diferencia clave entre los hidruros iónicos, covalentes y metálicos es que los hidruros iónicos se forman cuando el hidrógeno reacciona con elementos de bloque s fuertemente electropositivos y los hidruros covalentes se forman cuando los átomos de elementos químicos con valores de electronegatividad comparables reaccionan con hidrógeno mientras que los hidruros metálicos se forman cuando Los metales de transición reaccionan con el hidrógeno.
Relación:
1. "Hidruros". Química LibreTextsLibretexts, 15 de agosto de 2020, disponible aquí.
Imagen de cortesía:
1. "Estructura de la molécula de agua" por AbdullahAlturki99 - Trabajo propio (CC BY-SA 4.0) a través de Commons Wikimedia