Que diferencia principal entre nitronio, nitrosonio y nitrosilo es que El ion nitronio tiene un átomo de nitrógeno unido a dos átomos de oxígeno y el ion nitrosonio tiene un átomo de nitrógeno unido a un átomo de oxígeno, mientras que el término nitrosilo se usa cuando se nombra el ligando de óxido nítrico en complejos metálicos.
Lectura relacionada: Diferencia entre ácido salicílico y ácido hialurónico
Diferencia entre ácido salicílico y ácido hialurónicoLos iones de nitronio y nitrosonio son iones inorgánicos que contienen átomos de nitrógeno y oxígeno. Ambos iones ocurren en compuestos químicos como cationes.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el nitronio?
3. ¿Qué es el nitrosonio?
4. ¿Qué es el nitrosilo?
5. ¿Cuáles son las similitudes entre nitronio, nitrosonio y nitrosilo?
6. Comparación lado a lado: nitronio frente a nitrosonio frente a nitrosilo en forma tabular
7. Resumen
¿Qué es el nitronio?
El ion nitronio es un catión con la fórmula química NO2+. Podemos llamarlo ion onio debido a su átomo de nitrógeno tetravalente y carga eléctrica +1, que es similar al ion amonio. Este catión se forma cuando se elimina un electrón de la molécula de dióxido de nitrógeno paramagnético o por la protonación del ácido nítrico.
Lectura relacionada: Diferencia entre cloroformo y diclorometano.
Diferencia entre cloroformo y diclorometano.
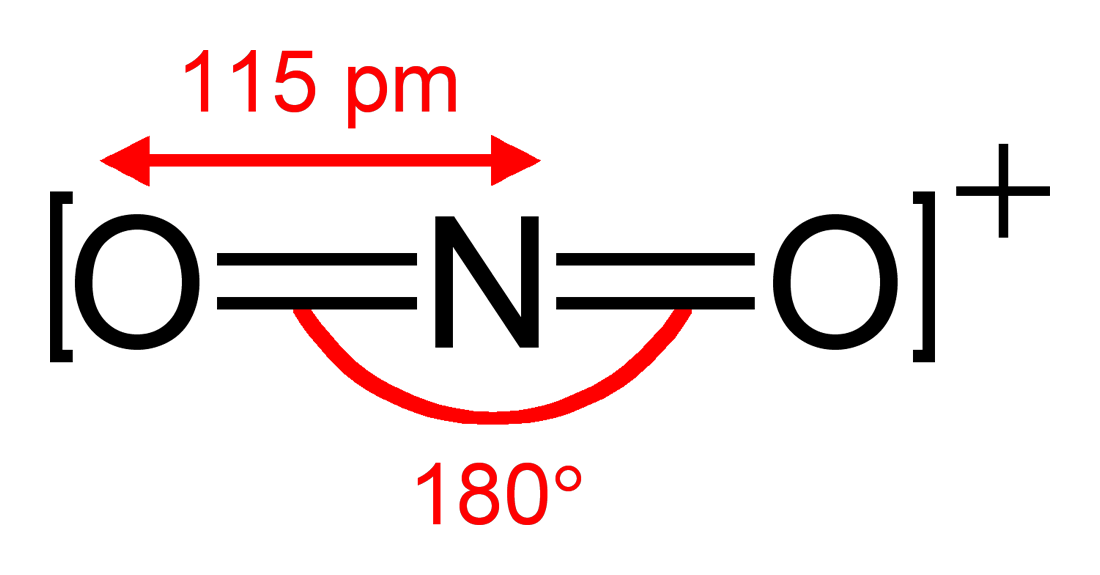
Figura 01: Estructura química de los iones de nitronio
Normalmente, el ion nitronio es lo suficientemente estable como para existir en condiciones normales. Sin embargo, este ion es generalmente reactivo y es muy útil como electrófilo para la nitración de otras sustancias. Para ello, este ion se genera in situ mezclando ácido sulfúrico concentrado y ácido nítrico concentrado.
Lectura relacionada: Diferencia entre covalente iónico e hidruros metálicos.
Diferencia entre covalente iónico e hidruros metálicos.Podemos observar que el ion nitronio es isoelectrónico con el dióxido de carbono y el óxido nitroso y tienen la misma estructura lineal y ángulo de enlace de 180 grados. Por lo tanto, este ion tiene un espectro vibratorio similar al del dióxido de carbono.
Hay pocas sales de iones de nitronio donde los aniones son débilmente nucleofílicos. Algunos ejemplos son el perclorato de nitronio (NO2+Cl O4–), tetrafluoroborato de nitronio (NO2+novio4–), hexafluorofosfato de nitronio (NO2+FP6–), hexafluoroarseniato de nitronio (NO2+AsF6–) y hexafluoroantimonato de nitronio (NO2+SbF6–).
¿Qué es el nitrosonio?
El nitrosonio es un catión con la fórmula química NO+. En este catión, el átomo de nitrógeno está unido a un átomo de oxígeno a través de un triple enlace. Por lo tanto, el orden de enlace de esta molécula es 3. Sin embargo, un átomo de oxígeno puede tener solo dos enlaces químicos según su configuración electrónica; por tanto, el otro enlace químico es un enlace coordinado. Por lo tanto, toda la especie diatómica lleva una carga positiva neta. Esto aparece como óxido nítrico con un electrón eliminado.

Figura 02: Estructura química del ion nitrosonio
Este catión es isoelectrónico con el monóxido de carbono (CO), el anión cianuro (CN-) y la molécula de nitrógeno (N2). Podemos obtener fácilmente iones de nitrosonio protonando ácido nitroso. Reacciona fácilmente con agua para formar ácido nitroso. Por lo tanto, debemos proteger este ion del agua o del aire húmedo. Cuando este ion reacciona con una base, da compuestos de nitrilo. Además, los iones de nitrosonio pueden reaccionar con las arilaminas como agentes diazotizantes. Los iones de nitrosonio también pueden actuar como un fuerte agente oxidante.
¿Qué es el nitrosilo?
El término nitrosilo se usa para nombrar el ligando de óxido nítrico en los complejos metálicos. El ligando de óxido nítrico está coordinado con un metal de transición central. Los complejos metálicos que contienen el ligando NO (óxido nitroso) en realidad tienen un catión NO+ llamado catión nitrosilo (el catión derivado del ligando nitrosilo).

Figura 03: Un complejo de metal de transición con ligandos de monóxido de carbono y nitrosilo
Este catión es isoelectrónico con el monóxido de carbono. Por lo tanto, el patrón de unión del monóxido de carbono con el metal de transición en los complejos de carbonilo es similar al de los complejos de nitrosilo.
¿Cuáles son las similitudes entre nitronio, nitrosonio y nitrosilo?
- Todos estos iones contienen átomos de nitrógeno y oxígeno.
- Estos son cationes con una carga neta positiva.
- Son óxidos de nitrógeno.
¿Cuál es la diferencia entre Nitronium Nitrosonium y Nitrosyl?
El nitronio y el nitrosonio son iones de óxido de nitrógeno. La principal diferencia entre el nitrosonio y el nitrosilo es que el ion nitronio tiene un átomo de nitrógeno unido a dos átomos de oxígeno y el ion nitrosonio tiene un átomo de nitrógeno unido a un átomo de oxígeno, mientras que el término nitrosilo se usa para nombrar el ligando de óxido nítrico en complejos metálicos. .
A continuación se muestra un resumen de la diferencia entre nitronio, nitrosonio y nitrosilo en forma tabular.

Resumen: nitronio, nitrosonio, nitrosilo
La principal diferencia entre el nitrosonio y el nitrosilo es que el ion nitronio tiene un átomo de nitrógeno unido a dos átomos de oxígeno y el ion nitrosonio tiene un átomo de nitrógeno unido a un átomo de oxígeno, mientras que el término nitrosilo se usa para nombrar el ligando de óxido nítrico en complejos metálicos. .
Relación:
1. "Ion nitronio". letras libres. (2020, 24 de agosto). Disponible aquí.
Imagen de cortesía:
1. "Dimensiones 2D de nitronio" (Dominio público) a través de Commons Wikimedia
2. "Dimensiones 2D de nitrosonio" (Dominio público) a través de Commons Wikimedia
3. "Nitroprusiato de sodio-2D" (Dominio público) a través de Commons Wikimedia