Que diferencia principal entre el estaño y el cloruro de estaño es que El cloruro de estaño tiene el estado de oxidación +4 del estaño, mientras que el cloruro de estaño tiene el estado de oxidación +2 del estaño..
Lectura relacionada: Diferencia entre alcanfor y mentol
Diferencia entre alcanfor y mentolLos nombres estaño y estaño se refieren al elemento químico estaño, que tiene dos estados de oxidación diferentes. El cloruro de estaño es cloruro de estaño (IV), mientras que el cloruro de estaño (II) es cloruro de estaño (II).
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el cloruro de estaño?
3. ¿Qué es el cloruro de estaño?
4. Comparación lado a lado: estaño y cloruro de estaño en forma tabular
5. Resumen
¿Qué es el cloruro de estaño?
El cloruro de estaño es cloruro estannoso. También se le conoce como tetracloruro de estaño, que es un compuesto inorgánico con la fórmula química SnCl4. Este compuesto es un líquido higroscópico incoloro que emite vapores al contacto con el aire. Tiene un olor fuerte. Este compuesto es importante como precursor para la fabricación de otros compuestos que contienen estaño. Fue descubierto por el científico Andreas Libavius.
Lectura relacionada: Diferencia entre las imprimaciones de óxido rojo y de cromato de zinc
Diferencia entre las imprimaciones de óxido rojo y de cromato de zinc
Figura 01: Compuesto de cloruro de estaño
Podemos producir cloruro de estaño a través de la reacción entre el cloro gaseoso y el estaño metálico a 115 grados centígrados. Además, este compuesto se solidifica alrededor de los 33 grados centígrados bajo cero. Este refuerzo da cristales monoclínicos y esta estructura es isoestructural con SnBr4. Hay varios hidratos conocidos de cloruro de estaño, como la forma pentahidratada. La estructura hidratada tiene moléculas de agua adicionales que unen con hidrógeno las moléculas de cloruro de estaño.
Lectura relacionada: Diferencia entre el ácido aminocaproico y el ácido tranexámico
Diferencia entre el ácido aminocaproico y el ácido tranexámicoTeniendo en cuenta el uso de cloruro estánnico, la principal aplicación de este compuesto es como precursor de compuestos organoestánnicos útiles como catalizadores y estabilizadores de polímeros. Podemos usar este compuesto en el proceso sol-gel para hacer recubrimientos de SnO2, nanocristales de SnO2, etc.
¿Qué es el cloruro de estaño?
El cloruro de estaño es cloruro estannoso. Aparece como un sólido cristalino blanco con la fórmula química SnCl2. La forma principal de este compuesto es la forma dihidratada, pero las soluciones acuosas de cloruro estannoso tienden a hidrolizarse cuando la solución está caliente. Además, el SnCl2 se usa a menudo como agente reductor y también es importante en los baños electrolíticos para el estañado. Este sólido blanco es inodoro, a diferencia del cloruro estannoso.
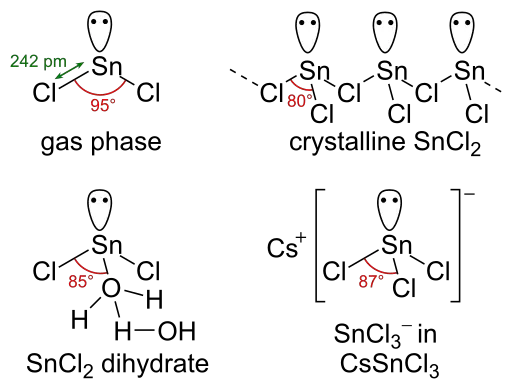
La molécula de SnCl2 tiene un par solitario de electrones; por lo tanto, esta molécula tiene una geometría doblada en su fase gaseosa. Mirando el estado sólido del cloruro estannoso, forma una estructura de cadena unida por puentes de cloruro.

Figura 02: Estructuras de cloruro de estaño en diferentes fases.
Podemos producir cloruro de estaño al exponer el metal de estaño a gas de cloruro de halógeno seco. Podemos hacer que el dihidrato se forme mediante una reacción similar usando el ácido HCl. Posteriormente, el agua presente en la solución debe eliminarse cuidadosamente por evaporación para obtener los cristales de cloruro estannoso dihidratado. Esta forma de dihidrato se puede deshidratar a la forma anhidra usando anhídrido acético.
Hay muchos usos diferentes del cloruro de estaño, incluido el estañado de acero, como mordiente en el teñido de textiles porque da colores brillantes con algunos tintes, como protector contra la erosión del esmalte en la pasta de dientes, como catalizador en la fabricación de material plástico PLA, como reductor agente, etc
¿Cuál es la diferencia entre el estaño y el cloruro de estaño?
Los nombres estaño y estaño se refieren al elemento químico estaño, que tiene dos estados de oxidación diferentes. los diferencia principal entre el estaño y el cloruro de estaño es que el cloruro de estaño tiene el estado de oxidación +4 del estaño, mientras que el cloruro de estaño tiene el estado de oxidación +2 del estaño. Teniendo en cuenta la producción de estos dos compuestos, el cloruro de estaño se puede producir mediante la reacción entre el cloro gaseoso y el estaño metálico a 115 grados centígrados. El cloruro de estaño se puede producir al exponer el metal de estaño a gas de cloruro de halógeno seco.
La siguiente infografía enumera otras diferencias entre el estaño y el cloruro de estaño.

Resumen: estaño frente a cloruro de estaño
Los nombres estaño y estaño se refieren al elemento químico estaño, que tiene dos estados de oxidación diferentes. los diferencia principal entre el estaño y el cloruro de estaño es que el cloruro de estaño tiene el estado de oxidación +4 del estaño, mientras que el cloruro de estaño tiene el estado de oxidación +2 del estaño.
Relación:
1. "Cloruro de estaño". Cloruro de estaño: una descripción general | Temas de ScienceDirect, disponibles aquí.
Imagen de cortesía:
1. "Cloruro de estaño (IV) pentahidratado" (Dominio público) a través de Commons Wikimedia
2. "Estructura SnCl2" por Hbf878 - Trabajo propio (CC0) a través de Commons Wikimedia