Que diferencia principal entre el plomo y el estaño es que El plomo es un metal gris metálico con un tinte azul, mientras que el estaño es un metal blanco plateado con un tinte amarillo tenue..
El plomo y el estaño son elementos químicos del grupo 14 en la tabla periódica de elementos. Este grupo de elementos se denomina grupo de carbono porque el primer miembro de este grupo es el elemento químico común "carbono".
Lectura relacionada: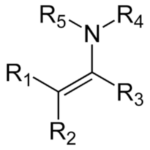 Diferencia entre imina y enamina.
Diferencia entre imina y enamina.CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el plomo?
3. ¿Qué es el estaño?
4. Comparación lado a lado: plomo frente a estaño en forma tabular
5. Resumen
que es plomo
El plomo es un elemento químico con número atómico 82 y símbolo químico Pb. Este es un elemento químico metálico y se clasifica como un metal pesado, más denso que la mayoría de los materiales que conocemos. Sin embargo, el plomo es un metal blando y maleable con un punto de fusión relativamente bajo. Podemos cortar este metal recién cortado y podemos observar un tinte azul característico junto con el aspecto metálico gris plateado. Este metal puede empañarse con el aire, lo que le da a la superficie metálica una apariencia gris opaca. Más importante aún, el plomo tiene el número atómico más alto de cualquier elemento estable.
El plomo es un metal posterior a la transición relativamente inerte. Podemos ilustrar el carácter débilmente metálico del plomo por su naturaleza anfótera. El plomo y los óxidos de plomo, por ejemplo, reaccionan con ácidos y bases y tienden a formar enlaces covalentes. Podemos encontrar compuestos de plomo que a menudo tienen un estado de oxidación de plomo +2 en lugar del estado de oxidación +4 (siendo 4 la oxidación más común para los elementos químicos del Grupo 14).
Teniendo en cuenta las propiedades a granel del plomo, debido a la pasivación, tiene alta densidad, maleabilidad, ductilidad y alta resistencia a la corrosión. El plomo tiene una estructura cúbica compacta, centrada en las caras y un alto peso atómico, lo que da como resultado una densidad mayor que las densidades de la mayoría de los metales comunes, como el hierro, el cobre y el zinc. En comparación con la mayoría de los metales, el plomo tiene un punto de fusión muy bajo y su punto de ebullición también es el más bajo entre los elementos del grupo 14.
Lectura relacionada: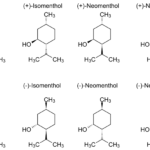 Diferencia entre alcanfor y mentol
Diferencia entre alcanfor y mentolEl plomo tiende a formar una película protectora cuando se expone al aire, que tiene una composición variable. El componente más común de esta capa es el carbonato de plomo (II). Además, pueden estar presentes componentes de sulfato y cloruro de plomo. Esta capa hace que la superficie del metal de plomo sea químicamente inerte al aire. Además, el gas flúor puede reaccionar con el plomo a temperatura ambiente para formar fluoruro de plomo (II). También hay una reacción similar con el cloro gaseoso, pero tiene que calentarse. El plomo metálico también es resistente al ácido sulfúrico y al ácido fosfórico, pero reacciona con el HCl y el ácido HNO3. Los ácidos orgánicos como el ácido acético pueden disolver el plomo en presencia de oxígeno. De manera similar, los ácidos alcalinos concentrados pueden disolver el plomo y formar plumbites.
¿Qué es el estaño?
El estaño es el elemento químico de número atómico 50 y símbolo químico Sn. Tiene una apariencia de color blanco plateado y un característico tono amarillo pálido. El estaño pertenece al grupo 14 de la tabla periódica de los elementos y, por lo tanto, al grupo del carbono. Es un metal blando que podemos cortar sin mucho esfuerzo. Sin embargo, el estaño es químicamente similar a sus dos vecinos, el plomo y el germanio.
Hay dos estados de oxidación principales del estaño; +2 y +4 estados de oxidación. El estado +4 es ligeramente más estable que el estado de oxidación +2. Podemos describir el estaño como un metal blanco plateado suave, maleable, dúctil y altamente cristalino. Hay diez isótopos estables de estaño. El isótopo más abundante es el isótopo Sn-120.

Figura 02: Superficie de metal estañado
Hay dos alótropos principales de estaño: estaño alfa y estaño beta. Entre ellos, el estaño beta es más estable a temperatura ambiente y también maleable. El estaño alfa es estable a bajas temperaturas y frágil a temperatura ambiente.
Más importante aún, el estaño es resistente a la corrosión del agua. Sin embargo, este metal puede ser atacado por ácidos y álcalis. Por lo tanto, se puede pulir mucho y podemos usarlo como capa protectora para otros metales importantes. La capa protectora de óxido que se produce sobre el estaño metálico puede prevenir aún más la oxidación de una superficie metálica, y la misma capa se puede formar sobre las aleaciones de estaño. Además, en presencia de oxígeno en la mezcla de reacción, el estaño puede actuar como catalizador, acelerando así una reacción química específica.
¿Cuál es la diferencia entre plomo y estaño?
El plomo y el estaño son elementos metálicos. El símbolo químico del plomo es Pb y el símbolo químico del estaño es Sn. La principal diferencia entre el plomo y el estaño es que el plomo aparece de color gris metálico con un tinte azul, mientras que el estaño aparece como un metal blanco plateado con un ligero tinte amarillo.
La siguiente infografía compara las propiedades principales de ambos metales y tabula lado a lado las diferencias entre el plomo y el estaño.

Resumen: plomo frente a estaño
El plomo y el estaño son elementos metálicos. La principal diferencia entre el plomo y el estaño es que el plomo aparece de color gris metálico con un tinte azul, mientras que el estaño aparece como un metal blanco plateado con un ligero tinte amarillo.
Relación:
1. "Estaño". Enciclopedia BritánicaEncyclopædia Britannica, Inc., disponible aquí.
Imagen de cortesía:
1. "Plomo electrolítico y cubo de 1 cm3" por Alchemist-hp (conferencia) (www.pse-mendelejew.de) - Trabajo propio, FAL) a través de Commons Wikimedia
2. "Dentro de una lata chapada en estaño" por Schtone - Trabajo propio (Dominio público) a través de Commons Wikimedia