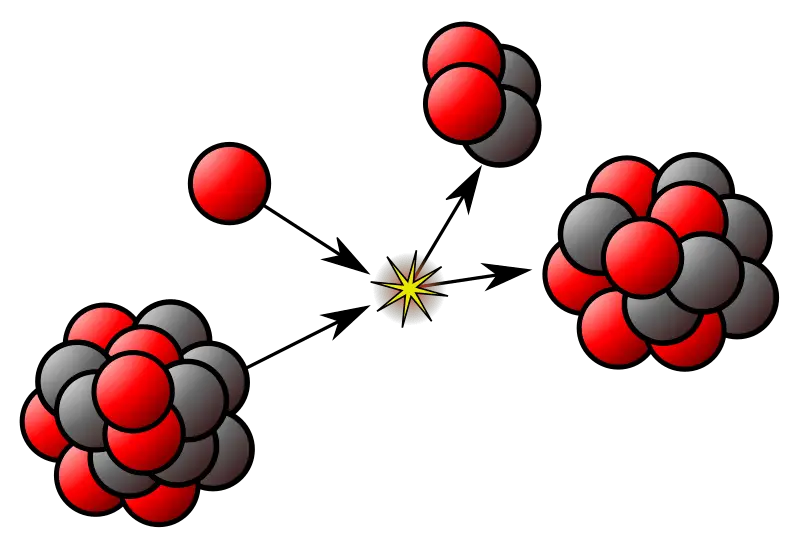
Que diferencia principal entre los isótopos padre e hijo es que un isótopo padre se desintegrará radiactivamente para formar un isótopo hijo.
Lectura relacionada: Diferencia entre anisol y éter dietílico.
Diferencia entre anisol y éter dietílico.Los términos isótopos padre e hijo pertenecen a la categoría de isótopos de elementos químicos. Los isótopos son diferentes formas de un solo elemento químico. Por lo tanto, los isótopos tienen el mismo número atómico pero diferentes números másicos porque difieren entre sí en el número de neutrones presentes en sus núcleos atómicos. Entre los isótopos de un elemento químico, algunos o todos los isótopos son radiactivos. Se descomponen radiactivamente y forman varios elementos químicos.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los isótopos originales?
3. ¿Qué son los isótopos hijos?
4. Comparación lado a lado: isótopos padre e hijo en forma tabular
5. Resumen
¿Qué son los isótopos originales?
Los isótopos originales son los isótopos de un elemento químico particular que puede sufrir una desintegración radiactiva para formar un isótopo diferente a partir de un elemento químico diferente. Durante esta desintegración radiactiva, estos isótopos liberan partículas de desintegración como rayos alfa, beta y gamma. Un isótopo padre es el comienzo de una cadena de descomposición. Una cadena de desintegración es una serie de reacciones de desintegración radiactiva que tienen lugar a partir de un solo isótopo (el isótopo principal).
Lectura relacionada: Diferencia entre nitrato de sodio y nitrito de sodio.
Diferencia entre nitrato de sodio y nitrito de sodio.
Figura 01: Desintegración radiactiva
Un ejemplo de un isótopo padre es el uranio. Puede decaer radiactivamente a través de la desintegración alfa para formar torio. El tiempo que tarda un isótopo padre en descomponerse en un isótopo hijo puede variar de un isótopo a otro; a veces, la naturaleza del isótopo padre determina el tiempo y, a veces, la naturaleza del isótopo hijo formado por el proceso de descomposición determina el tiempo.
Lectura relacionada: Diferencia entre los anómeros alfa y beta
Diferencia entre los anómeros alfa y beta¿Qué son los isótopos hijos?
Los isótopos hijos son los productos de la desintegración radiactiva de los isótopos padres. A veces, las reacciones dan isótopos hijos estables, pero la mayoría de las veces son inestables y radiactivos, lo que lleva a la propagación de cadenas de descomposición. Además, los isótopos hijos sufren una desintegración radiactiva para formar sus propios isótopos hijos. Estos se denominan isótopos nietos (isótopos hijos de isótopos hijos).

Figura 02: Una cadena de descomposición
Por ejemplo, el torio es un isótopo hijo formado en la desintegración radiactiva del uranio. Algunos otros términos que podemos usar para nombrar isótopos hijos son producto hijo, producto de desintegración, nucleido hijo, radiohijo, etc.
¿Cuál es la diferencia entre los isótopos padre e hijo?
Los términos isótopos padre e hijo pertenecen a la categoría de isótopos de elementos químicos. Los isótopos son diferentes formas de un solo elemento químico. La mayoría de los isótopos son radiactivos. La principal diferencia entre los isótopos padre e hijo es que un isótopo padre se desintegra radiactivamente para formar un isótopo hijo. Un ejemplo de un isótopo padre es el uranio. Puede sufrir una desintegración alfa y formar torio. Por lo tanto, el torio es el isótopo hijo de esta reacción. El torio puede descomponerse aún más, lo que da como resultado una cadena de descomposición.
Muy a menudo, los isótopos hijos son inestables y están sujetos a una mayor descomposición. Pero a veces son productos estables. Sin embargo, los isótopos originales son siempre isótopos inestables. Además, es importante tener en cuenta que el isótopo hijo siempre es un elemento químico diferente al isótopo padre.
La siguiente infografía resume la diferencia entre los isótopos padre e hijo.

Resumen - Isótopos padre vs. hija
Los términos isótopos padre e hijo pertenecen a la categoría de isótopos de elementos químicos. Los isótopos son diferentes formas de un solo elemento químico. La mayoría de los isótopos son radiactivos. Los isótopos originales son los isótopos de un elemento químico particular que puede sufrir una desintegración radiactiva para formar un isótopo diferente a partir de un elemento químico diferente. Los isótopos hijos, por otro lado, son los productos de la desintegración radiactiva de los isótopos padres. Entonces, esta es la diferencia clave entre los isótopos padre e hijo.
Relación:
1. Helmenstine, Annemarie. "Definición de isótopo hijo: glosario de química". ThoughtCo, 12 de enero de 2020, disponible aquí.
Imagen de cortesía:
1. "Reacción nuclear" por Kjerish - Trabajo propio (CC BY-SA 4.0) a través de Commons Wikimedia
2. "Torio de la cadena de descomposición" por BatesIsBack - (CC BY-SA 3.0) a través de Commons Wikimedia