Que diferencia principal entre isótopos y elementos es que la Los isótopos son formas diferentes de un mismo elemento químico, mientras que los elementos son tipos de átomos con el mismo número de protones en el núcleo.
Un tipo similar de átomo puede sufrir ligeros cambios para formar diferentes isótopos. Un elemento puede tener múltiples isótopos. La naturaleza de cada isótopo contribuye a la naturaleza de un elemento. Aquí discutiremos sobre los isótopos y elementos en detalle para aclarar la diferencia entre isótopos y elementos.
Lectura relacionada: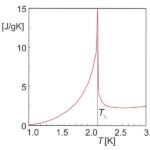 Diferencia entre capacidad calorífica y calor específico.
Diferencia entre capacidad calorífica y calor específico.CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los isótopos?
3. ¿Qué son los elementos?
4. Comparación lado a lado: isótopos frente a elementos en forma tabular
5. Resumen
¿Qué son los isótopos?
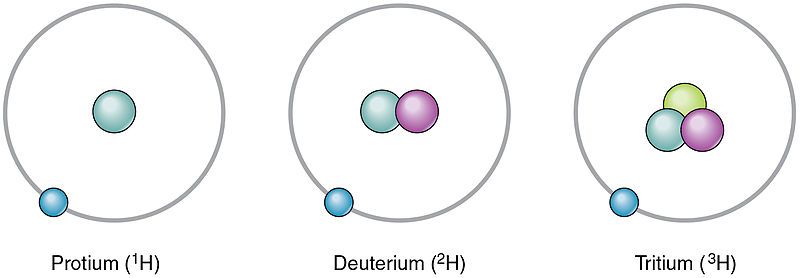
Los átomos de un mismo elemento pueden diferir entre sí. Estos diferentes átomos de un mismo elemento son isótopos. Se diferencian entre sí por un número diferente de neutrones. Dado que el número de neutrones es diferente, su número de masa también es diferente. Sin embargo, los isótopos de un mismo elemento tienen el mismo número de protones. Varios isótopos ocurren en la naturaleza en cantidades variables. Por lo tanto, podemos expresar su ocurrencia como un porcentaje, lo que se denomina frecuencia relativa. Por ejemplo, el hidrógeno tiene tres isótopos como protio, deuterio y tritio. El número de protones en sus núcleos atómicos es el mismo, pero el número de neutrones es diferente. Sus neutrones y abundancias relativas son las siguientes.
- 1H: sin neutrones, la abundancia relativa es del 99,985%
- 2H- un neutrón, la abundancia relativa es 0.015%
- 3H- dos neutrones, la abundancia relativa es 0%
El número de neutrones que puede contener un núcleo varía de un elemento a otro. Sólo unos pocos de estos isótopos son estables. Por ejemplo, el oxígeno tiene tres isótopos estables y el estaño tiene diez isótopos estables. Los elementos simples en su mayoría tienen la misma cantidad de neutrones que de protones. Pero en los elementos pesados hay más neutrones que protones.
Además, el número de neutrones es importante para equilibrar la estabilidad de los núcleos. Si los núcleos son demasiado pesados, se vuelven inestables y, por lo tanto, estos isótopos se vuelven radiactivos. Por ejemplo, 238U emite radiación y se desintegra en núcleos mucho más pequeños. Los isótopos pueden tener diferentes propiedades debido a sus diferentes masas. Por ejemplo, pueden tener diferentes giros. Por lo tanto, sus espectros de RMN difieren. Sin embargo, su cuenta de electrones es similar, lo que resulta en un comportamiento químico similar.
Lectura relacionada: diferencia entre agua y hielo
diferencia entre agua y hielo¿Qué son los elementos?
Conocemos la palabra "elemento" porque la conocemos en la tabla periódica. Hay alrededor de 118 elementos químicos en la tabla periódica, y están ordenados por su número atómico. Un elemento es una especie química que es solo un tipo de átomo. Por lo tanto, son puros. Además, los átomos de un mismo elemento tienen el mismo número de protones en sus núcleos. Sin embargo, el número de neutrones puede diferir entre sí. Por ejemplo, el elemento más pequeño es el hidrógeno. Plata, oro, platino son algunos de los elementos preciosos comúnmente conocidos.
Cada elemento tiene una masa atómica, un número atómico, un símbolo, una configuración electrónica, etc. Aunque la mayoría de los elementos se producen de forma natural, existen algunos elementos sintéticos como el californio, el americio, el einstenio y el mendelevio. Podemos dividir todos los elementos en tres grupos; como metales, semimetales y no metales.

Figura 02: Endoesqueleto
Además, podemos clasificarlos en grupos y periodos en función de características más específicas. Además, los elementos del mismo grupo o período comparten ciertas características comunes y algunas propiedades pueden cambiar secuencialmente a medida que se desplaza por un grupo o período. Además, los elementos pueden sufrir cambios químicos para formar diferentes compuestos; Sin embargo, no podemos descomponer más los elementos usando métodos químicos simples.
¿Cuál es la diferencia entre isótopos y elementos?
El término elemento químico describe un tipo de átomo, mientras que el término isótopo describe diferentes formas del mismo elemento químico. Por lo tanto, la diferencia clave entre isótopos y elementos es que los isótopos son formas diferentes del mismo elemento químico, mientras que los elementos son tipos de átomos con la misma cantidad de protones en los núcleos atómicos. Además, otra diferencia entre los isótopos y los elementos es que los isótopos tienen diferente número de neutrones, pero los elementos químicos pueden tener el mismo número de neutrones o un número diferente de neutrones; pero nunca tienen el mismo número de protones.
Como otra diferencia importante entre isótopos y elementos, podemos decir que la masa atómica de un isótopo se puede calcular simplemente sumando las masas totales de los protones y los neutrones en los núcleos atómicos, mientras que podemos calcular la masa atómica de un elemento químico usando las masas atómicas de sus isótopos y su abundancia relativa.

Resumen - Isótopos vs. Elementos
Los isótopos son diferentes formas atómicas de un mismo elemento químico. los diferencia principal entre isótopos y elementos es que los isótopos son formas diferentes del mismo elemento químico, mientras que los elementos son tipos de átomos con la misma cantidad de protones en los núcleos atómicos.
Relación:
1. "Elemento químico". Wikipedia, Fundación Wikimedia, 11 de noviembre de 2018. Disponible aquí
2. Helmenstina, Anne Marie, Ph.D. "Definición de isótopos y ejemplos en química". ThoughtCo, 22 de octubre de 2018. Disponible aquí
Imagen de cortesía:
1. "204 isótopos de hidrógeno-01" de OpenStax College - Anatomy & Physiology, sitio web de Connexions. (CC POR 3.0) a través de Commons Wikimedia
2. "Gráfico de tabla periódica simple-en" Por Offnfopt - Trabajo propio, (Dominio público) a través de Commons Wikimedia