
La principal diferencia entre los sólidos iónicos y metálicos es que el los sólidos iónicos contienen principalmente cationes y aniones, mientras que los sólidos metálicos contienen átomos metálicos y electrones libres.
Lectura relacionada: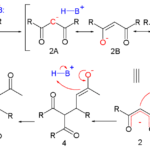 Diferencia entre la adición de Michael y la anulación de Robinson
Diferencia entre la adición de Michael y la anulación de RobinsonTanto los sólidos iónicos como los sólidos metálicos se encuentran en estado sólido. Sin embargo, difieren tanto en composición como en propiedades.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los sólidos iónicos?
3. ¿Qué son los sólidos metálicos?
4. Comparación lado a lado: sólidos iónicos y metálicos en forma tabular
5. Resumen
¿Qué son los sólidos iónicos?
Los sólidos iónicos son compuestos químicos que contienen cationes y aniones. Estos iones se mantienen unidos por fuerzas electrostáticas. Llamamos a estas fuerzas enlaces iónicos. Los iones se unen entre sí de tal manera que la conexión general es neutra (sin carga negativa o positiva). El número de cationes que rodean a un anión y viceversa puede variar de sólido a sólido, dependiendo de la carga del catión y del anión.
Lectura relacionada: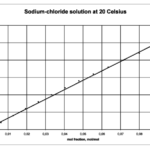 Diferencia entre fracción molar y porcentaje en peso
Diferencia entre fracción molar y porcentaje en peso
Figura 01: estructura cristalina fuerte de sólidos iónicos
Los iones en el sólido pueden ser iones simples como iones de sodio e iones de cloruro (en compuestos iónicos de cloruro de sodio o sales) o iones complejos como iones poliatómicos, es decir, iones de amonio. Estos sólidos existen como redes tridimensionales y normalmente tienen una estructura cristalina.
Lectura relacionada: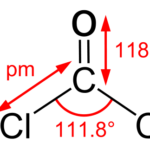 Diferencia entre fosfina y fosgeno.
Diferencia entre fosfina y fosgeno.Además, los sólidos iónicos que contienen iones de hidrógeno son ácidos y los iones de hidróxido son bases. Los sólidos iónicos que no contienen ninguno de estos iones se llaman sales. Los compuestos de sal se forman a partir de reacciones ácido-base. Además, los sólidos iónicos también se pueden formar a partir de la evaporación (retirando el solvente, los iones cristalizan en un sólido), precipitación, reacciones en estado sólido, etc.
Por lo general, los sólidos iónicos tienen puntos de fusión y ebullición muy altos porque tienen una fuerte estructura de red 3D que es muy difícil de descomponer. Estos sólidos también suelen ser duros y quebradizos. Además, estos sólidos iónicos son eléctricamente aislantes, pero cuando se derriten o disuelven se vuelven altamente conductores porque los iones se liberan.
Los sólidos metálicos son compuestos sólidos que contienen átomos de metal y electrones a su alrededor. Los metales son buenos ejemplos de sólidos metálicos. Los átomos metálicos de estos sólidos se mantienen unidos por enlaces metálicos. Los átomos de metal existen como cationes con carga eléctrica positiva, y estos átomos se encuentran inmersos en un mar de electrones. Estos electrones provienen de los átomos de metal durante la formación de cationes.

Figura 02: galio metálico en estado sólido
Es decir, los átomos metálicos forman cationes al liberar electrones de valencia, y estos electrones aparecen alrededor del ion metálico en un estado deslocalizado, y estos electrones hacen que los átomos metálicos se mantengan unidos.
Tanto los sólidos iónicos como los sólidos metálicos están presentes en el sólido pero difieren entre sí en composición y propiedades. los diferencia clave entre los sólidos iónicos y metálicos es que los sólidos iónicos contienen esencialmente cationes y aniones, mientras que los sólidos metálicos contienen átomos metálicos y electrones libres.
Además, los sólidos iónicos exhiben fuerzas de atracción electrostática entre cationes y aniones, mientras que los sólidos metálicos exhiben enlaces metálicos. Al considerar las propiedades, los sólidos iónicos son duros y quebradizos, mientras que los sólidos metálicos son duros, dúctiles y maleables.
La siguiente infografía resume la diferencia entre sólidos iónicos y metálicos.

Resumen: sólidos iónicos frente a metálicos
Tanto los sólidos iónicos como los sólidos metálicos están presentes en el sólido, pero difieren entre sí en su composición, lo que también da como resultado sus diferentes propiedades. los diferencia clave entre los sólidos iónicos y metálicos es que los sólidos iónicos contienen esencialmente cationes y aniones, mientras que los sólidos metálicos contienen átomos metálicos y electrones libres. Además, los sólidos iónicos tienen fuerzas de atracción electrostática entre cationes y aniones, pero existen enlaces metálicos en los sólidos metálicos.
Relación:
1. "Sólidos iónicos". Química LibreTextsLibretexts, 5 de junio de 2019, Disponible aquí.
Imagen de cortesía:
1. "Cristales de galio" Por en: usuario: foobar - Trabajo propio (CC BY-SA 3.0) a través de Commons Wikimedia
2. "Cloruro de potasio 3D iónico" por Benjah-bmm27 - Trabajo propio (Dominio público) a través de Commons Wikimedia











