
Diferencia clave - Cuadrícula vs Unidad célula
Una red es una estructura regular formada por muchas unidades pequeñas conocidas como celdas unitarias. Una celda unitaria es la unidad representativa más pequeña de una red compuesta por todos los componentes que se repiten a lo largo de la estructura de la red. Que diferencia principal entre la red y la celda unitaria es que Una red es una disposición tridimensional repetida regularmente de átomos, iones o moléculas en un metal u otro sólido cristalino, mientras que una celda unitaria es una disposición simple de esferas (átomos, moléculas o iones) que se asemeja al patrón repetitivo de una red. .
Lectura relacionada: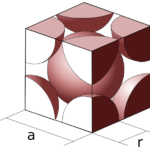 Diferencia entre BCC y FCC
Diferencia entre BCC y FCCCONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es una cuadrícula?
3. ¿Qué es una celda unitaria?
4. Relación entre celosía y celda unitaria
5. Comparación lado a lado: cuadrícula frente a celda unitaria en forma tabular
6. Resumen
¿Qué es una cuadrícula?
Una red es una disposición tridimensional repetida regularmente de átomos, iones o moléculas en un metal u otro sólido cristalino. Una celda unitaria de la red representa la disposición repetitiva de la red; La celda unitaria es la unidad más pequeña en una red que contiene todos los componentes químicos en la red.
Se puede formar una red debido a enlaces covalentes entre átomos, enlaces iónicos entre iones o fuerzas intermoleculares entre moléculas. Un ejemplo de una red de red covalente es el diamante. Allí, los átomos de carbono están conectados entre sí a través de enlaces covalentes, creando una estructura de red compleja. La red de cloruro de sodio es un ejemplo típico de una red iónica. Allí, los cationes de sodio y los aniones de cloruro se organizan en una red compleja que forma una red iónica. Las moléculas de agua también pueden formar una red; Hielo. Allí, los enlaces de hidrógeno entre las moléculas de agua pueden conducir a la formación de una red que se asemeja a la estructura del diamante. La mayoría de los metales también están dispuestos en estructuras de celosía.
Lectura relacionada: Diferencia entre empaque cerrado hexagonal y empaque cerrado cúbico
Diferencia entre empaque cerrado hexagonal y empaque cerrado cúbicoHay defectos de red en casi todas las redes. Un defecto es una irregularidad en el sistema reticular. Hay dos tipos principales de defectos de red; Defecto de Frenkel y defecto de Schottky. En los defectos de Frenkel, un átomo o ion en la red deja su ubicación original y ocupa una ubicación diferente en la misma red. Un defecto de Schottky ocurre cuando los iones con carga opuesta abandonan su ubicación original.
Al considerar la termodinámica de una red, la energía de la red es una medida de la energía contenida en la red cristalina de un compuesto, igual a la energía que se liberaría si los iones de los componentes del infinito se juntaran.
 Lectura relacionada:
Lectura relacionada: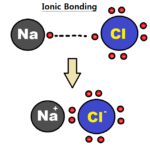 Diferencia entre sólidos iónicos y moleculares.
Diferencia entre sólidos iónicos y moleculares.Figura 01: una red es una disposición regular de átomos, moléculas o iones
Hay 14 tipos de rejillas. Estas formas se clasifican en función de la disposición de los átomos, moléculas o iones en la celda unitaria. Los tipos de cuadrícula se dan en la siguiente tabla junto con la categoría.
¿Qué es una celda unitaria?
Una celda unitaria es un arreglo simple de esferas (átomos, moléculas o iones) que se asemejan al patrón repetitivo de una red. Una celda unitaria se considera como una estructura de caja. Esta caja contiene todos los componentes químicos presentes en toda la red. Una celda unitaria es una estructura 3D y se describe mediante parámetros de red. Los parámetros de celosía son las longitudes entre los bordes y los ángulos de la celda unitaria.
- Las longitudes entre los bordes de la celda unitaria se indican con los símbolos a, b y c
- Los ángulos de las celdas unitarias se denotan con los símbolos alfa(α), beta(β) y gamma(γ).

Figura 02: Parámetros de celosía
Una celda unitaria puede tener diferentes formas según los ángulos y las longitudes entre los bordes de la celda. Es el bloque de construcción de una red. Hay 7 tipos de celdas unitarias cúbicas. Los nombres de estas formas de celdas unitarias y sus dimensiones se dan en la siguiente tabla.
¿Cuál es la relación entre la red y la celda unitaria?
- Una celda unitaria es la unidad representativa más pequeña de una red. Están todos los componentes y su disposición, que se repite a lo largo de la estructura reticular.
¿Cuál es la diferencia entre celosía y celda unitaria?
Lattice vs celda unitaria |
|
| Una red es una disposición tridimensional repetida regularmente de átomos, iones o moléculas en un metal u otro sólido cristalino. | Una celda unitaria es un arreglo simple de esferas (átomos, moléculas o iones) que se asemejan al patrón repetitivo de una red. |
| Naturaleza | |
| La red es una estructura muy grande y compleja. | La celda unitaria es la unidad repetitiva más simple y pequeña de una red. |
| número de átomos | |
| Una red tiene una gran cantidad de componentes (átomos, moléculas o iones). | Una celda unitaria tiene un pequeño número de componentes. |
Resumen - rejilla contra Unidad célula
Una red es una estructura de red compleja con pequeñas unidades que están conectadas entre sí. Estas pequeñas unidades se llaman celdas unitarias. La diferencia entre la red y la celda unitaria es que una red es una disposición tridimensional repetida regularmente de átomos, iones o moléculas en un metal u otro sólido cristalino, mientras que una celda unitaria es una disposición simple de esferas (átomos, moléculas o iones). que se asemejan al patrón repetitivo de una cuadrícula.
Relación:
1. “Célula unitaria”. Química LibreTexts, Libretexts, 31 de enero de 2017. Disponible aquí
2. "Simetría, sistemas cristalinos y celosías de Bravais". Simetría, sistemas cristalinos y redes de Bravais | La física en breve. Disponible aquí
3. "12.1 Red cristalina y celdas unitarias". Química LibreTexts, Libretexts, 30 de enero de 2018. Disponible aquí
4. "Cuadrícula". Merriam Webster, Merriam Webster. Disponible aquí
Imagen de cortesía:
1.'2790370' de DavidZydd (dominio público) a través de pixabay
2. 'UnitCell' por Mcpazzo - Trabajo propio, (Dominio público) a través de Commons Wikimedia











