Diferencia clave: ligando fuerte contra ligando débil
Un ligando es un átomo, ion o molécula que dona o comparte dos de sus electrones a través de un enlace covalente coordinado con un átomo o ion central. El concepto de ligandos se analiza en química de coordinación. Los ligandos son especies químicas involucradas en la formación de complejos con iones metálicos. Por lo tanto, también se denominan agentes complejantes. Los ligandos pueden ser monodentados, bidentados, tridentados, etc. en base a la denticidad del ligando. La denticidad es el número de grupos donantes presentes en un ligando. Monodentado significa que el ligando tiene solo un grupo donante. Bidentado significa que tiene dos grupos donantes por molécula de ligando. Hay dos tipos principales de ligandos clasificados según la teoría del campo cristalino; ligandos fuertes (o ligandos de campo fuerte) y ligandos débiles (o ligandos de campo débil). Que diferencia principal entre ligandos fuertes y ligandos débiles es que La división de los orbitales después de unirse a un ligando de campo fuerte provoca una diferencia mayor entre los orbitales de mayor y menor nivel de energía, mientras que la división de los orbitales después de unirse a un ligando de campo débil provoca una diferencia menor entre el nivel de energía de los orbitales de mayor y menor nivel de energía. causado
Lectura relacionada: Diferencia entre CO2 y CO2e
Diferencia entre CO2 y CO2eCONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la teoría del campo cristalino?
3. ¿Qué es un ligando fuerte?
4. ¿Qué es un ligando débil?
5. Comparación lado a lado: ligando fuerte frente a ligando débil en forma tabular
6. Resumen
¿Qué es la teoría del campo cristalino?
La teoría del campo cristalino se puede describir como un modelo que tiene como objetivo explicar la ruptura de la degeneración (capas de electrones de la misma energía) de los orbitales de electrones (generalmente orbitales d o f) debido al campo eléctrico estático creado por un anión o aniones circundantes (o ligandos). Esta teoría se usa a menudo para demostrar el comportamiento de los complejos de iones de metales de transición. Esta teoría puede explicar las propiedades magnéticas, los colores de los complejos de coordinación, las entalpías de hidratación, etc.
Teoría:
La interacción entre el ion metálico y el ligando resulta de la atracción entre el ion metálico cargado positivamente y la carga negativa de los electrones desapareados del ligando. Esta teoría se basa principalmente en los cambios que ocurren en cinco orbitales electrónicos degenerados (un átomo de metal tiene cinco orbitales d). Cuando un ligando se acerca al ion metálico, los electrones desapareados están más cerca de algunos orbitales d que de otros orbitales d del ion metálico. Esto provoca una pérdida de degeneración. Además, los electrones en los orbitales d repelen los electrones del ligando (porque ambos tienen carga negativa). Por lo tanto, los orbitales d más cercanos al ligando tienen mayor energía que otros orbitales d. Esto conduce a la división de los orbitales d en orbitales d de alta energía y orbitales d de baja energía en función de la energía.
Lectura relacionada: Diferencia entre ácido concentrado y ácido fuerte.
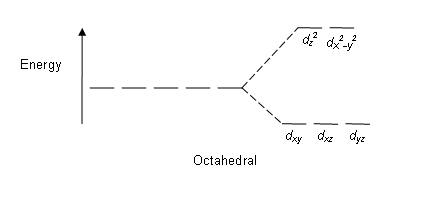
Diferencia entre ácido concentrado y ácido fuerte.Algunos factores que afectan esta partición son: la naturaleza del ion metálico, el estado de oxidación del ion metálico, la disposición de los ligandos alrededor del ion metálico central y la naturaleza de los ligandos. Después de la división energética de estos orbitales d, la diferencia entre los orbitales d de alta y baja energía se da como el parámetro de división del campo cristalino (∆Oct para complejos octaédricos).

Figura 01: patrón de división en complejos octaédricos
Lectura relacionada: Diferencia entre cavidades tetraédricas y octaédricas
Diferencia entre cavidades tetraédricas y octaédricasPatrón de brecha: Dado que hay cinco orbitales d, la división se produce en una proporción de 2:3. En los complejos octaédricos hay dos orbitales en el nivel de alta energía (denominados colectivamente como "p.ej'), y tres orbitales están en el nivel de energía más bajo (conocidos colectivamente como t2g). En los complejos tetraédricos ocurre lo contrario; tres orbitales están en el nivel de energía más alto y dos están en el nivel de energía más bajo.
¿Qué es un ligando fuerte?
Un ligando fuerte o ligando de campo fuerte es un ligando que puede conducir a una mayor división del campo cristalino. Esto significa que la unión de un ligando de campo fuerte provoca una mayor diferencia entre los orbitales de mayor y menor nivel de energía. Los ejemplos incluyen CN– (ligandos de cianuro), NO2– (ligando nitro) y CO (ligandos carbonilo).

Figura 02: división de giro bajo
En la formación de complejos con estos ligandos, los orbitales de menor energía (t2g) primero se llenan por completo con electrones antes de llenarse con cualquier otro orbital de alto nivel de energía (p. ej.). Los complejos formados de esta manera se denominan "complejos de espín bajo".
¿Qué es un ligando débil?
Un ligando débil o un ligando de campo débil es un ligando que puede conducir a una menor división del campo cristalino. Esto significa que la unión de un ligando de campo débil causa menos diferencia entre los orbitales de mayor y menor nivel de energía.

Figura 3: división de alto giro
En este caso, dado que la pequeña diferencia entre los dos niveles orbitales provoca repulsiones entre los electrones en estos niveles de energía, los orbitales de mayor energía pueden llenarse fácilmente con electrones en comparación con los orbitales de baja energía. Los complejos formados con estos ligandos se denominan "complejos de alto espín". Ejemplos de ligandos de campo débil son I– (ligando yoduro), Br– (ligando bromuro), etc.
¿Cuál es la diferencia entre ligando fuerte y ligando débil?
Ligando fuerte frente a ligando débil |
|
| Un ligando fuerte o ligando de campo fuerte es un ligando que puede conducir a una mayor división del campo cristalino. | Un ligando débil o un ligando de campo débil es un ligando que puede conducir a una menor división del campo cristalino. |
| teoría | |
| La división tras la unión de un ligando de campo fuerte provoca una mayor diferencia entre los orbitales de mayor y menor nivel de energía. | La división de los orbitales tras la unión de un ligando de campo débil provoca una diferencia menor entre los orbitales de mayor y menor nivel de energía. |
| categoría | |
| Los complejos formados con ligandos de campo fuerte se denominan “complejos de espín bajo”. | Los complejos formados con ligandos de campo débil se denominan "complejos de alto espín". |
Resumen - Ligando fuerte contra ligando débil
Los ligandos fuertes y los ligandos débiles son aniones o moléculas que hacen que los orbitales d de un ion metálico se dividan en dos niveles de energía. La diferencia entre los ligandos fuertes y los ligandos débiles es que la división después de unirse a un ligando de campo fuerte provoca una mayor diferencia entre los orbitales de mayor y menor nivel de energía, mientras que la división de los orbitales después de unirse a un ligando de campo débil provoca una diferencia menor entre el de mayor nivel. y menor causa orbitales de nivel de energía.
Relación:
1. Helmenstine, Anne Marie, D. "Definición de ligando". ThoughtCo, 11 de febrero de 2017. Disponible aquí
2. "Ligandos". Química LibreTexts, Libretexts, 19 de enero de 2018. Disponible aquí
3. Los editores de la Encyclopædia Britannica. "Ligand." Encyclopædia Britannica, Encyclopædia Britannica, Inc., 12 de agosto de 2010. Disponible aquí
Imagen de cortesía:
1. "División del campo de cristal octaédrico" por el usuario de Wikipedia en inglés YanA, (CC BY-SA 3.0) a través de Commons Wikimedia
2. 'CFT-Low Spin Splitting Diagram-Vector' por Offnfopt, (Dominio público) a través de Commons Wikimedia
3. 'CFT-High Spin Splitting Diagram-Vector' Por Offnfopt, imagen de referencia creada por YanA - Trabajo propio (Dominio público) a través de Commons Wikimedia