Que diferencia principal entre el cloroformo y el diclorometano es que El cloroformo contiene tres átomos de cloro por molécula, mientras que el diclorometano contiene dos átomos de cloro por molécula..
El cloroformo y el diclorometano son moléculas organocloradas con atomicidad similar y geometría o forma molecular similar.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el cloroformo?
3. ¿Qué es el diclorometano?
4. Comparación lado a lado: cloroformo frente a diclorometano en forma tabular
5. Resumen
 Diferencia entre covalente iónico e hidruros metálicos.
Diferencia entre covalente iónico e hidruros metálicos.¿Qué es el cloroformo?
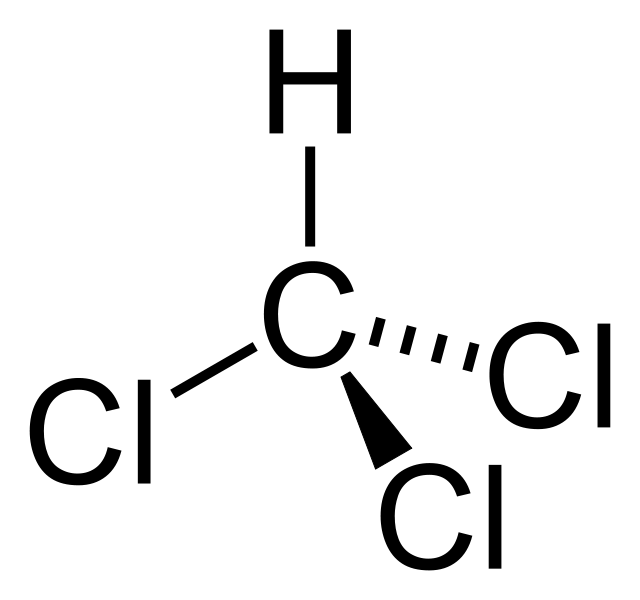
El cloroformo es un compuesto orgánico con la fórmula química CHCl3. Es útil como un poderoso anestésico. El nombre IUPAC para este compuesto es triclorometano. Es un líquido incoloro y denso que tiene un olor dulce. El cloroformo se produce a gran escala como precursor de la fabricación de PTFE. Además, la mayor parte del cloroformo en el medio ambiente (alrededor del 90%) se debe a emisiones de origen natural. Por ejemplo, muchos tipos de algas y hongos producen este compuesto y lo liberan a la atmósfera.
La masa molar del cloroformo es 119,37 g/mol y aparece como un líquido incoloro a temperatura ambiente. Este líquido tiene un fuerte olor etéreo. Su punto de fusión es de -63,5 °C y su punto de ebullición es de 61,15 °C. Además, el cloroformo se descompone a 450 °C. Esta molécula tiene una geometría tetraédrica.

 Diferencia entre hiperconjugación isovalente y de sacrificio.
Diferencia entre hiperconjugación isovalente y de sacrificio.Figura 01: Estructura química del cloroformo
A escala industrial, podemos hacer este compuesto calentando una mezcla de cloro y clorometano (a veces también usamos metano). Al calentar, la halogenación radical tiene lugar a 400–500 °C. Esto produce compuestos clorados de clorometano (o metano), que producen cloroformo. Este compuesto puede someterse a una cloración adicional para formar tetracloruro de carbono. Sin embargo, el producto final de esta reacción es una mezcla de clorometanos, que podemos separar por destilación para obtener cloroformo.
Hay muchos usos del cloroformo. Es útil como solvente porque el átomo de hidrógeno en esta molécula puede formar un enlace de hidrógeno. También podemos usarlo como reactivo para muchas reacciones químicas. Ej: como fuente del grupo diclorocarbeno. Más importante aún, el cloroformo es conocido por sus propiedades anestésicas.
Lectura relacionada: Diferencia entre galio y mercurio.
Diferencia entre galio y mercurio.¿Qué es el diclorometano?
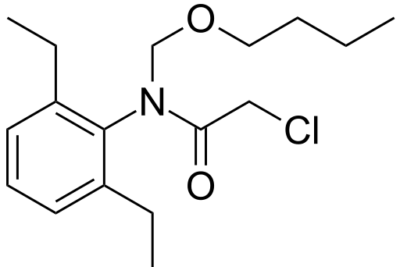
El diclorometano es un compuesto orgánico con la fórmula química CH2clase2. Es un compuesto organoclorado y podemos referirnos a él como DCM. Este compuesto se presenta como un líquido volátil e incoloro con un olor dulce similar al cloroformo. El diclorometano es principalmente adecuado como disolvente. Este líquido es inmiscible con agua, aunque es un compuesto polar. Sin embargo, puede mezclarse con muchos otros disolventes orgánicos.

Figura 02: Estructura química del diclorometano
Hay algunas fuentes naturales de diclorometano, incluidos los respiraderos oceánicos, las macroalgas, los humedales y los volcanes. Sin embargo, podemos observar que la mayor parte del diclorometano en el medio ambiente se debe a las emisiones industriales. Podemos producir diclorometano tratando clorometano o metano con cloro gaseoso a altas temperaturas.
¿Cuál es la diferencia entre el cloroformo y el diclorometano?
El cloroformo y el diclorometano son moléculas organocloradas. La principal diferencia entre el cloroformo y el diclorometano es que el cloroformo contiene tres átomos de cloro por molécula, mientras que el diclorometano contiene dos átomos de cloro por molécula. Además, el cloroformo se puede producir calentando una mezcla de cloro y clorometano, mientras que el diclorometano se puede producir tratando el clorometano o el metano con cloro gaseoso a altas temperaturas.
Resumen - Cloroformo vs Diclorometano
En resumen, el cloroformo y el diclorometano son moléculas organocloradas. La principal diferencia entre el cloroformo y el diclorometano es que el cloroformo contiene tres átomos de cloro por molécula, mientras que el diclorometano contiene dos átomos de cloro por molécula.
Relación:
1. "Cloroformo". Centro Nacional de Información Biotecnológica. Base de datos de conexión de PubChemBiblioteca Nacional de Medicina de EE. UU., disponible aquí.
Imagen de cortesía:
1. "Cloroformo mostrado" Por Benjah-bmm27, Vectorización: Fvasconcellos - convertido de Fvasconcellos (dominio público) a través de Commons Wikimedia
2. "Estructura molecular del diclorometano" por Ohnodoctor - Dibujado con ChemDraw (CC BY-SA 4.0) a través de Commons Wikimedia