
Que diferencia principal entre el zinc y el óxido de zinc es que el El zinc es un elemento químico, mientras que el óxido de zinc es un compuesto químico.
Lectura relacionada: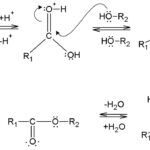 Diferencia entre esterificación y transesterificación.
Diferencia entre esterificación y transesterificación.El zinc es un elemento químico metálico en el bloque d de la tabla periódica de elementos. Forma muchos compuestos como óxidos, sulfuros, etc. El óxido de zinc es uno de esos compuestos químicos que contiene átomos de zinc y oxígeno. Está presente como un sólido blanco. Analicemos más detalles sobre el zinc y su óxido a continuación.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el zinc?
3. ¿Qué es el óxido de zinc?
4. Comparación lado a lado: zinc frente a óxido de zinc en forma tabular
5. Resumen
¿Qué es el zinc?
El zinc es un elemento químico con número atómico 30 y símbolo químico Zn. Este elemento químico es similar al magnesio cuando observamos sus propiedades químicas. Esto se debe principalmente a que estos dos elementos tienen el estado de oxidación +2 como estado de oxidación estable y también el Mg+2 y zinc+2 Los cationes son de tamaño similar. Además, este es el 24el elemento químico más común en la corteza terrestre. Algunos datos químicos sobre el zinc son los siguientes:
Lectura relacionada: Diferencia entre imán de neodimio e imán normal
Diferencia entre imán de neodimio e imán normal- Símbolo químico - Zn
- Número atómico – 30
- Peso atómico estándar - 65,38
- Apariencia - sólido gris plateado
- grupo – 12
- Período – 4to
- bloque - bloque d
- Categoría de elemento: metal después de la transición
- configuración electronica - [Ar] 3d10 4s2
- Fase a temperatura y presión estándar - fase sólida
- Punto de fusión - 419,53°C
- Punto de ebullición - 907 °C
- Estructura cristalina - hcp (empaquetado cerrado hexagonal)
Mirando el metal de zinc, es un metal diamagnético y tiene una apariencia brillante de color blanco azulado. A la mayoría de las temperaturas, este metal es duro y quebradizo. Sin embargo, se vuelve maleable entre 100 y 150 °C. Además, este es un buen conductor de electricidad. Sin embargo, tiene puntos de fusión y ebullición bajos en comparación con la mayoría de los otros metales.
En cuanto a la aparición de este metal, la corteza terrestre tiene alrededor de 0,0075% de zinc. Encontramos este elemento en el suelo, agua de mar, minerales de cobre y plomo, etc. Además, es más probable que este elemento se encuentre en combinación con azufre.
¿Qué es el óxido de zinc?
El óxido de zinc es un compuesto químico con la fórmula química ZnO. Es un compuesto inorgánico. El estado de oxidación del zinc en este compuesto es +2, y para el oxígeno -2. Aparece como un sólido blanco que es insoluble en agua. En la naturaleza, sin embargo, se presenta como el mineral zincita; un mineral raro. Este mineral contiene manganeso y algunas otras impurezas. Por lo tanto, aparece como un color amarillo o rojo. Aparte de eso, el óxido de zinc cristalino es termocrómico. Esto significa que su color blanco se vuelve amarillo cuando se calienta en el aire y puede volverse blanco cuando se enfría. Algunos datos químicos sobre el óxido de zinc son los siguientes:
- Fórmula química - ZnO
- Masa molar - 81,38 g/mol
- Apariencia - sólido blanco
- Fase a temperatura y presión estándar - fase sólida
- Punto de fusión - 1.975°C
- Punto de ebullición: se descompone por encima de 1975 °C
- Estructura de Cristal – Wurtzita

Figura 02: Óxido de zinc
Utilizamos este compuesto como aditivo en la fabricación de caucho, plásticos, cerámica, vidrio, cemento, lubricantes, etc. Además, tiene propiedades semiconductoras. Las propiedades favorables que tiene este compuesto para ser utilizado como semiconductor son la transparencia, alta movilidad de electrones, gran banda prohibida, etc.
¿Cuál es la diferencia entre el zinc y el óxido de zinc?
El zinc es un elemento químico con número atómico 30 y símbolo químico Zn, mientras que el óxido de zinc es un compuesto químico con fórmula química ZnO. Esta es la diferencia clave entre el zinc y el óxido de zinc. Es decir, el óxido de zinc es un compuesto inorgánico derivado del elemento químico zinc. Está asociado con el oxígeno. Dado que el zinc es un elemento químico, podemos dar su peso atómico (el peso atómico estándar es 65,38 para el zinc), mientras que podemos dar su masa molar o peso molecular para el óxido de zinc (la masa molar es 81,38 g/mol) porque es un compuesto químico.
Además, también existe una diferencia de apariencia entre el zinc y el óxido de zinc. El zinc aparece como un sólido gris plateado brillante, mientras que el óxido de zinc aparece como un sólido blanco a temperatura y presión estándar. Aparte de eso, otra diferencia entre el zinc y el óxido de zinc es que podemos usar el óxido de zinc para fabricar semiconductores, pero el zinc por sí solo no tiene propiedades semiconductoras.
La siguiente infografía presenta más detalles sobre la diferencia entre el zinc y el óxido de zinc en forma tabular.

Resumen: zinc frente a óxido de zinc
El zinc es un elemento químico que conocemos muy bien como metal. El óxido de zinc es un compuesto inorgánico que contiene zinc y oxígeno en combinación. Entonces, la diferencia clave entre el zinc y el óxido de zinc es que el zinc es un elemento químico, mientras que el óxido de zinc es un compuesto químico.
Relación:
1. "Zinc" Wikipedia, Fundación Wikimedia, 4 de septiembre de 2018. Disponible aquí
2. "Óxido de zinc". Wikipedia, Fundación Wikimedia, 30 de agosto de 2018. Disponible aquí
Imagen de cortesía:
1. "Fragmento de zinc sublimado y cubo de 1 cm3" Por Alchemist-hp - Trabajo propio, (FAL) a través de Commons Wikimedia
2. "Óxido de zinc" Por w: Usuario: Walkerma - Trabajo propio, (Dominio público) a través de Commons Wikimedia













