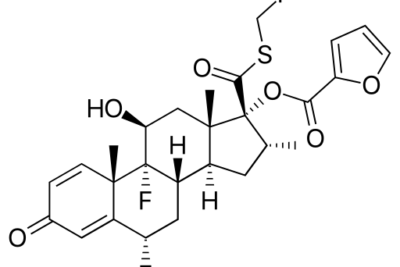
La oximercuración es una reacción química que implica un mecanismo de adición electrofílico que convierte un alqueno en un alcohol neutro. La demercuración u oximercuración-desmercuración es una reacción en la que un alqueno se convierte en una sal de Hg2+ y un nucleófilo de oxígeno, formando un intermedio de organomercurio.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la Oximercuración?
3. ¿Qué es la demercuración?
4. Oximercuración vs. demercuración en forma tabular
5. Resumen: oximercuración frente a demercuración
 ¿Cuál es la diferencia entre el carbonato de cobre y el carbonato de cobre básico?
¿Cuál es la diferencia entre el carbonato de cobre y el carbonato de cobre básico?¿Qué es la oximercuración?
La oximercuración es una reacción química que implica un mecanismo de adición electrofílico que convierte un alqueno en un alcohol neutro. En este proceso, podemos observar la reacción entre un alqueno y acetato de mercurio en una solución acuosa. Esto da la adición de un acetoximercurio grupo y un grupo OH a través del doble enlace.

Figura 01: Un mecanismo de reacción de oximercuración en orden secuencial
Lectura relacionada: ¿Cuál es la diferencia entre la cafeína, la teobromina y la teofilina?
¿Cuál es la diferencia entre la cafeína, la teobromina y la teofilina?Los carbocationes no se forman durante el proceso de oximercuración. Por lo tanto, también hay pasos de reordenamiento. Esta reacción sigue la regla de Markonikov, que establece que la adición de un ácido protónico de fórmula HX (donde X = halógeno) o H2O (considerado H-OH) a un alqueno, el hidrógeno se une al carbono de doble enlace con el mayor número de átomos de hidrógeno, mientras que el halógeno (X) se une al otro carbono.
Además, la oximercuración es una reacción anti-adición. Esto significa que el grupo OH siempre se agrega al átomo de carbono más sustituido y los dos grupos tienden a ser trans entre sí.

 ¿Cuál es la diferencia entre el zinc y el magnesio?
¿Cuál es la diferencia entre el zinc y el magnesio?Figura 02: Una aplicación de Oximercuración
Usualmente, una reacción de oximercuración es seguida por una reacción de demercuración reductora; por lo tanto, lo llamamos una reacción de reducción de oximercuración. En la práctica, esta reacción de reducción es más común que la reacción de oximercuración.
¿Qué es la demercuración?
La demercuración u oximercuración-desmercuración es la reacción en la que un alqueno se convierte en una sal de Hg2+ y un nucleófilo de oxígeno, formando un intermedio de organomercurio. El nucleófilo de oxígeno usado aquí puede ser agua o un alcohol. En otras palabras, en la demercuración, un átomo de hidrógeno en el sitio CH2 y un grupo hidroxilo en el átomo de carbono del anillo reaccionan entre sí. Da el producto de Markovnikov predicho a través de la hidratación indirecta de un alqueno.
¿Cuál es la diferencia entre oximercuración y desmercuración?
La oximercuración es una reacción química que implica un mecanismo de adición electrofílico que convierte un alqueno en un alcohol neutro. Por el contrario, la desmercurización es la reacción en la que un alqueno se convierte en una sal de Hg2+ y un nucleófilo de oxígeno, formando así un intermedio de organomercurio. Por lo tanto, la diferencia clave entre la oximercuración y la demercuración es que la oximercuración implica una adición electrófila en la que un alqueno se convierte en un alcohol neutro, mientras que la demercuración implica la conversión de un alqueno en una sal de Hg2+ y un organomercurio intermedio.
Resumen - Oximercuración vs Desmercuración
La oximercuración es una reacción química que implica un mecanismo de adición electrofílico que convierte un alqueno en un alcohol neutro. La demercuración u oximercuración-desmercuración es la reacción en la que un alqueno se convierte en una sal de Hg2+ y un nucleófilo de oxígeno, formando un intermedio de organomercurio. Por lo tanto, la diferencia clave entre la oximercuración y la demercuración es que la oximercuración implica una adición electrófila en la que un alqueno se convierte en alcohol neutro, mientras que la demercuración implica la conversión de un alqueno en una sal de Hg2+ y un organomercurio intermedio.
Relación:
1. "Demercuración por oximercuración". Una visión general | Temas de ScienceDirect.
2. "Hidratación: Oximercuración-Desmercuración". Química - Texto libre
Imagen de cortesía:
1. "Oximercuración paso a paso" por The Jackal en Wikipedia en inglés - Transferido de en.wikipedia a Commons por Ronhjones usando Commons Helper. (Dominio público) a través de Commons Wikimedia
2. "Oxymerc otro" Por Vkk0000 - Trabajo propio (CC BY-SA 3.0) a través de Commons Wikimedia