El ácido tartárico y el ácido cítrico son compuestos ácidos porque sus grupos carboxilo pueden donar los átomos de hidrógeno que contienen al medio, haciendo que el medio se vuelva ácido. Ambos compuestos están presentes en las plantas, especialmente en las frutas. El ácido tartárico se encuentra en las uvas, mientras que el ácido cítrico se encuentra en los limones.
Lectura relacionada:
 Diferencia entre éter y cetona.
Diferencia entre éter y cetona.CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el ácido tartárico?
3. ¿Qué es el ácido cítrico?
4. Comparación lado a lado: ácido tartárico frente a ácido cítrico en forma tabular
5. Resumen
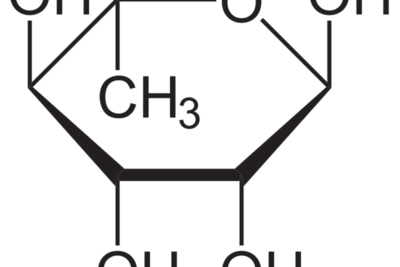
¿Qué es el ácido tartárico?
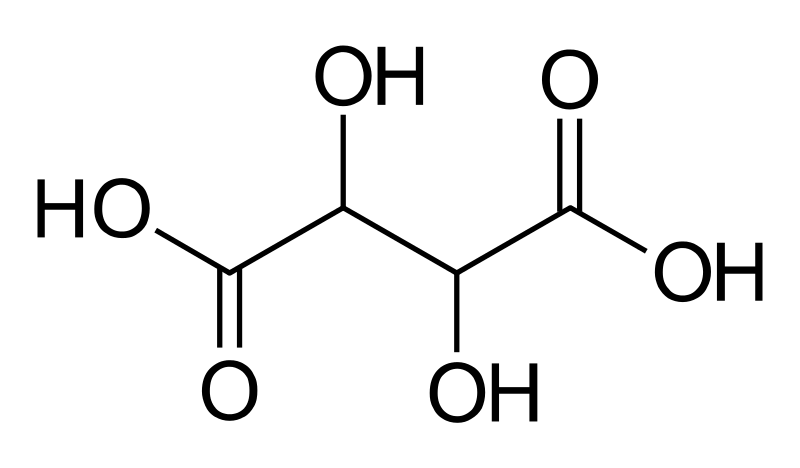
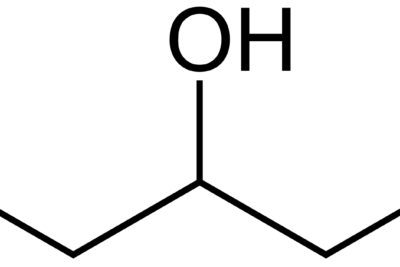
Ácido tartárico, comúnmente conocido como cremor tártaro, es un compuesto orgánico con la fórmula química C4H6O6. El nombre IUPAC de este ácido es ácido 2,3-dihidroxibutanodioico. La masa molar de este ácido es de 150,08 g/mol y es muy poco soluble en agua. El compuesto está disponible como un polvo blanco y es irritante en forma concentrada.
El ácido tartárico está presente de forma natural en las uvas y se forma espontáneamente durante el proceso de vinificación utilizando uvas. Además, es común en su forma de sal de potasio: bitartrato de potasio. El bicarbonato de sodio, un agente leudante común en la producción de alimentos, es una mezcla de bicarbonato de sodio y bitartrato de potasio. Además, el ácido tartárico actúa como antioxidante en algunos alimentos.
Lectura relacionada: Diferencia entre el óxido de zinc y el dióxido de titanio.
Diferencia entre el óxido de zinc y el dióxido de titanio.El ácido tartárico es un ácido alfa-hidroxicarboxílico. Esta categorización se basa en los dos grupos de ácido carboxílico en esta molécula y estos dos grupos tienen un grupo hidroxilo en su posición de carbono alfa. Además, la molécula es diprótica ya que es posible eliminar los átomos de hidrógeno en los dos grupos carboxilo como protones.
La molécula de ácido tartárico de origen natural es un compuesto quiral. Es decir, esta molécula tiene enantiómeros; tiene enantiómeros L y D. El enantiómero natural es el ácido L-(+)-tartárico. Estos enantiómeros son ópticamente activos porque pueden rotar la luz polarizada linealmente.
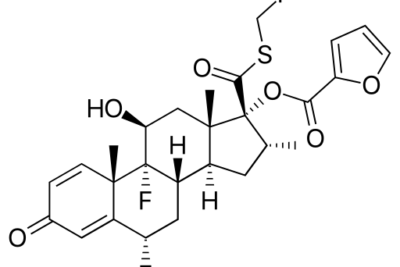
¿Qué es el ácido cítrico?
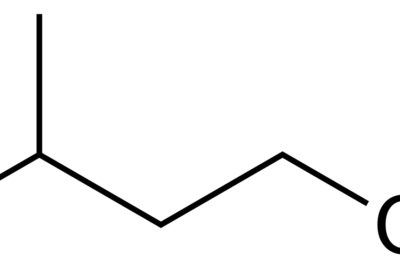
El ácido cítrico es un compuesto orgánico con la fórmula química C6H8O7. El nombre IUPAC de este compuesto es Ácido 2-hidroxipropano-1,2,3-tricarboxílico. Su masa molar es de 192,12 g/mol y su punto de fusión es de 156 °C. Es un compuesto inodoro y está disponible como un compuesto cristalino sólido.
La molécula de ácido cítrico tiene tres grupos de ácido carboxílico, lo que indica que es tribásico o triprótico, pero solo tiene un grupo hidroxilo. El ácido es triprótico porque la molécula de ácido puede liberar tres protones por molécula (los tres grupos de ácido carboxílico pueden liberar los átomos de hidrógeno que contienen como protones).

Figura 2: Molécula de ácido cítrico
El ácido cítrico está presente de forma natural en el limón y otras frutas de la familia Rutaceae, es decir, los cítricos. Es un irritante para la piel y los ojos. Este compuesto tiene varios usos, como aditivo alimentario, bebida, agente quelante, ingrediente en ciertos cosméticos, etc.
¿Cuál es la diferencia entre el ácido tartárico y el ácido cítrico?
Ácido tartárico versus ácido cítrico |
|
| ácido tartárico es un compuesto orgánico con la fórmula química C4H6O6. | ácido cítrico es un compuesto orgánico con la fórmula química C6H8O7. |
| nombre de la IUPAC | |
| ácido 2,3-dihidroxibutanodioico | Ácido 2-hidroxipropano-1,2,3-tricarboxílico |
| masa molar | |
| 150,08 g/mol | 192,12 g/mol |
| punto de fusion | |
| 206 °C (en mezcla racémica de enantiómeros D y L) | 153 grados |
| punto de ebullición | |
| 275 grados | 310 grados |
| Número de grupos de ácido carboxílico |
|
| Tiene dos grupos de ácido carboxílico. | Tiene tres grupos de ácido carboxílico. |
| presencia de enantiómeros | |
| Dos formas enantioméricas: ácido L-tartárico y ácido D-tartárico | Sin enantiómeros |
| presencia de un grupo hidroxilo | |
| Tiene dos grupos hidroxilo | Tiene un grupo hidroxilo |
| fuente natural |
|
| Se encuentra naturalmente en frutas como las uvas. | Naturalmente disponible en cítricos |
| Producto comercial | |
| Se vende como polvo de hornear | Se vende como un sólido blanco cristalino |
| aplicaciones | |
| Utilizado en la industria farmacéutica y como agente quelante de calcio y magnesio. | Se utiliza como ingrediente en alimentos y bebidas, como agente quelante, en la fabricación de medicamentos y cosméticos, etc. |
Resumen: ácido tartárico frente a ácido cítrico
La diferencia clave entre el ácido tartárico y el ácido cítrico es que el ácido tartárico es diprótico, mientras que el ácido cítrico es triprótico. Es decir, la molécula de ácido tartárico tiene dos átomos de hidrógeno que se liberan como protones, mientras que la molécula de ácido cítrico tiene tres átomos de hidrógeno que se liberan como protones. Ambos compuestos ácidos están comúnmente disponibles en las plantas, especialmente en las frutas; Sin embargo, las uvas son la fuente más común de ácido tartárico, mientras que los cítricos son la fuente más común de ácido cítrico.
Relación:
1. “ácido tartárico”. Wikipedia, Fundación Wikimedia, 22 de abril de 2018, disponible aquí.
2. "Ácido cítrico". Wikipedia, Fundación Wikimedia, 17 de abril de 2018, disponible aquí.
3. Brown, William H. "Ácido tartárico". Encyclopædia Britannica, Inc., 17 de abril de 2016, disponible aquí.
Imagen de cortesía:
1. "Ácido tartárico" de JaGa: hecho a sí mismo con BKChem e Inkscape (CC BY-SA 3.0) a través de Commons Wikimedia
2. "Ácido cítrico" por NEUROtiker - Trabajo propio (Dominio público) a través de Commons Wikimedia