Que diferencia principal entre aldehído y cetona que es El grupo funcional de un aldehído siempre se encuentra en un extremo, mientras que el grupo funcional de una cetona siempre se encuentra en el medio de una molécula.
Los aldehídos y las cetonas son moléculas orgánicas con un grupo carbonilo. En un grupo carbonilo, un átomo de carbono tiene un doble enlace con el oxígeno. El átomo de carbono del carbonilo es sp2 hibridado. Por lo tanto, los aldehídos y las cetonas tienen una disposición plana trigonal alrededor del átomo de carbono del carbonilo. El grupo carbonilo es un grupo polar; por lo tanto, los aldehídos y las cetonas tienen puntos de ebullición más altos en comparación con los hidrocarburos del mismo peso. Sin embargo, estos no pueden formar enlaces de hidrógeno más fuertes que los alcoholes; por lo tanto, tienen puntos de ebullición más bajos que los alcoholes correspondientes. Debido a la capacidad de formar enlaces de hidrógeno, los aldehídos y cetonas de bajo peso molecular son solubles en agua. Pero a medida que aumenta el peso molecular, se vuelven hidrofóbicos.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el aldehído?
3. ¿Qué es la cetona?
4. Comparación lado a lado: aldehído frente a cetona en forma tabular
5. Resumen
 Diferencia entre níquel cepillado y níquel satinado
Diferencia entre níquel cepillado y níquel satinado¿Qué es el aldehído?
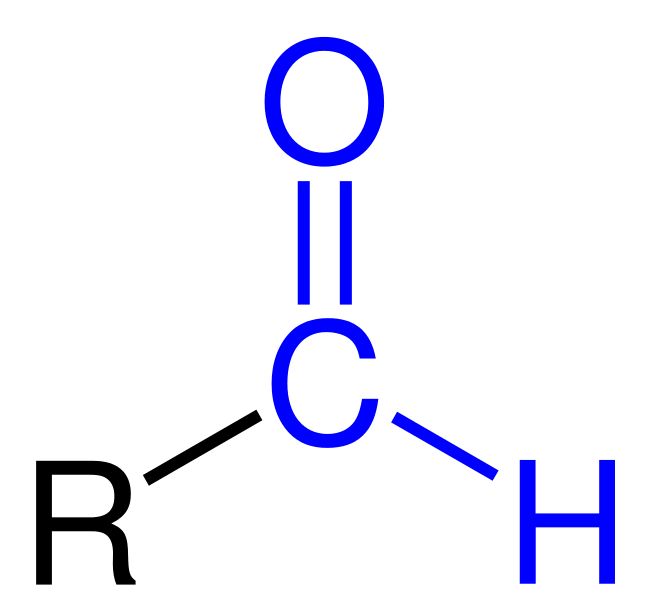
El aldehído tiene un grupo carbonilo. Este grupo carbonilo se une a otro carbono de un lado y se une a un átomo de hidrógeno en el otro extremo. Por lo tanto, podemos caracterizar los aldehídos con el grupo -CHO. El aldehído más simple es el formaldehído. Sin embargo, esta molécula se desvía de la fórmula general al tener un átomo de hidrógeno en lugar del grupo R.
En la nomenclatura de aldehídos, según el sistema IUPAC, usamos el término "al" para denotar un aldehído. En el caso de los aldehídos alifáticos, la "e" del alcano correspondiente se sustituye por "al". Por ejemplo, llamamos CH3CHO como etanal y CH3CH2CHO se conoce como propanal.

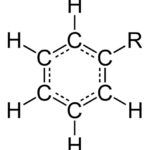 Diferencia entre fenol y fenilo.
Diferencia entre fenol y fenilo.Figura 01: Estructura química de los aldehídos.
Para los aldehídos con sistemas de anillos donde el grupo aldehído está unido directamente al anillo, usamos el término "carbaldehído" como sufijo para nombrarlos. Sin embargo, llamamos al compuesto C6H6CHO se usa comúnmente como benzaldehído en lugar de bencenocarbaldehído. Podemos sintetizar aldehídos por diferentes métodos. Un método es a través de la oxidación de alcoholes primarios. Además, podemos sintetizar aldehídos mediante la reducción de ésteres, nitrilos y cloruros de acilo.
¿Qué es la cetona?
En una cetona, el grupo carbonilo se encuentra entre dos átomos de carbono. Usamos el sufijo "uno" en la nomenclatura de cetonas. En lugar de "-e" del alcano correspondiente, usamos el término "uno". Además, numeramos la cadena alifática para que el carbono carbonilo tenga el número más bajo posible. Por ejemplo, llamamos al compuesto CH3COCH2CH2CH3 como 2-pentanona.
Lectura relacionada: Diferencia entre molécula de elemento y molécula de compuesto.
Diferencia entre molécula de elemento y molécula de compuesto.
Figura 02: Estructura química de las cetonas
Además, podemos sintetizar cetonas por oxidación de alcoholes secundarios, por ozonólisis de alquenos, etc. Aparte de eso, las cetonas tienen la capacidad de tautomerismo ceto-enol. Este proceso ocurre cuando una base fuerte acepta el hidrógeno α (hidrógeno unido al carbono adyacente al grupo carbonilo). La capacidad de liberar el hidrógeno α hace que las cetonas sean más ácidas que los alcanos correspondientes.
¿Cuál es la diferencia entre aldehído y cetona?
El aldehído es un compuesto orgánico con la fórmula química general R-CHO, mientras que la cetona es un compuesto orgánico con la fórmula química general R-CO-R'. La diferencia clave entre el aldehído y la cetona es que el grupo funcional de un aldehído siempre se encuentra en un extremo, mientras que el grupo funcional de una cetona siempre se encuentra en el medio de una molécula. Además, los aldehídos suelen ser más reactivos que las cetonas.
Como otra diferencia importante entre el aldehído y la cetona, podemos decir que los aldehídos se pueden oxidar para formar ácidos carboxílicos, pero las cetonas no se pueden oxidar a menos que rompamos sus cadenas de carbono.
Resumen: aldehído frente a cetona
Tanto los aldehídos como las cetonas son compuestos orgánicos. La diferencia clave entre el aldehído y la cetona es que el grupo funcional de un aldehído siempre se encuentra en un extremo, mientras que el grupo funcional de una cetona siempre se encuentra en el medio de una molécula.
Relación:
1. Letras libres. "Nomenclatura de Aldehídos y Cetonas". Química LibreTexts, Fundación Nacional de Ciencias, 2 de octubre de 2018. Disponible aquí
2. "Cetona". Wikipedia, Fundación Wikimedia, 7 de noviembre de 2018. Disponible aquí
Imagen de cortesía:
1. "Aldehídos de grupo funcional" por MaChe (Conferencia) - Trabajo propio, (Dominio público) a través de Commons Wikimedia
2. "Cetona-general" (dominio público) a través de Commons Wikimedia