Que diferencia principal entre haloalcanos primarios secundarios y terciarios es la posición del átomo de carbono que lleva el átomo de halógeno. En los haloalcanos primarios, el átomo de carbono que lleva el átomo de halógeno está unido a un solo grupo alquilo. Sin embargo, en los haloalcanos secundarios, este átomo de carbono está unido a dos grupos alquilo. Mientras que en los haloalcanos terciarios, este átomo de carbono está unido a tres grupos alquilo.
Los haloalcanos o haloalcanos son alcanos que contienen halógenos. Los halógenos son elementos químicos del grupo 17 de la tabla periódica. Incluye flúor (F), cloro (Cl), bromo (Br), yodo (I) y astato (At). Uno o más halógenos pueden estar presentes en el mismo haloalcano. Hay muchos usos importantes de los haloalcanos como retardantes de llama, extintores de incendios, refrigerantes, propulsores, etc. Sin embargo, muchos haloalcanos se consideran compuestos tóxicos y contaminantes.
Lectura relacionada: Diferencia entre arsénico y arsina
Diferencia entre arsénico y arsinaCONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los haloalcanos primarios?
3. ¿Qué son los haloalcanos secundarios?
4. ¿Qué son los haloalcanos terciarios?
5. Comparación lado a lado: haloalcanos primarios, secundarios y terciarios en forma tabular
6. Resumen
¿Qué son los haloalcanos primarios?
Los haloalcanos primarios son compuestos orgánicos en los que un átomo de carbono está unido a un grupo alquilo y un átomo de halógeno. Por lo tanto, la estructura general de un haloalcano primario es R-CH2-X; R es un grupo alquilo mientras que X es un halógeno. Podemos llamarlos 10 haloalcanos. Un ejemplo común es un halotano que contiene un grupo etilo como grupo R y un átomo de cloro como grupo X o halógeno. Sin embargo, los haluros de metilo son una excepción a estas estructuras primarias de haloalcano porque tienen tres átomos de hidrógeno en el átomo de carbono que lleva el átomo de halógeno. Esto significa que no hay grupos alquilo unidos a estos compuestos. Sin embargo, se consideran haloalcanos primarios.
Además, si consideramos la reactividad de los haloalcanos primarios, el átomo de carbono unido al átomo de halógeno es un centro reactivo porque el halógeno es más electronegativo que el carbono; Por lo tanto, imparte una carga positiva parcial al átomo de carbono al atraer los electrones de enlace hacia sí mismo. Además, estos compuestos pueden ser atacados por reactivos nucleófilos que buscan cargas positivas. Esto conduce a una reacción de sustitución nucleófila. Y esta reacción tiene una alta barrera de energía de activación. Es una reacción de tipo SN2 y la llamamos reacción bimolecular.
Lectura relacionada: Diferencia entre éteres corona y criptandos
Diferencia entre éteres corona y criptandos¿Qué son los haloalcanos secundarios?
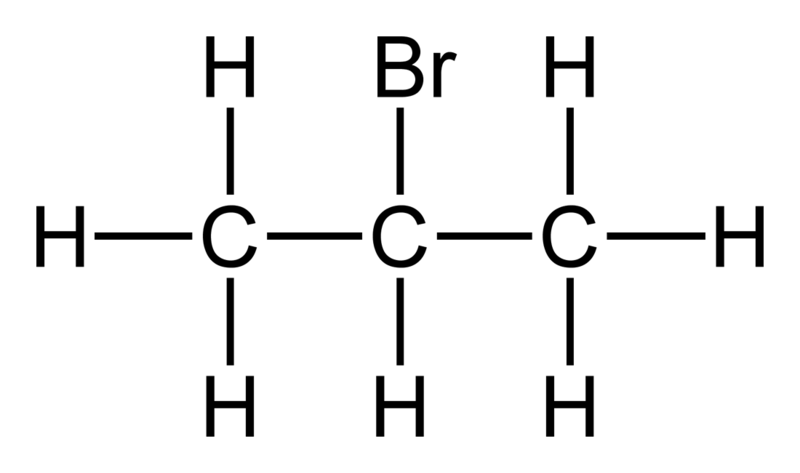
Los haloalcanos secundarios son compuestos orgánicos que tienen un átomo de carbono unido a dos grupos alquilo y un átomo de halógeno. La estructura general de un haloalcano secundario es R2-C(-H)-X. Los dos grupos alquilo (grupo R) pueden ser grupos iguales o diferentes. Podemos denotar estas conexiones como 20 haloalcanos. Además, los haloalcanos secundarios experimentan reacciones de sustitución nucleófila SN2. Por lo tanto, son reacciones bimoleculares.
La reactividad de los haloalcanos secundarios se encuentra entre las reactividades de los haloalcanos primarios y terciarios porque la presencia de dos grupos alquilo reduce la carga positiva en el átomo de carbono ya que los grupos alquilo son especies atractoras de electrones.
¿Qué son los haloalcanos terciarios?
Los haloalcanos terciarios son compuestos orgánicos que tienen un átomo de carbono unido a tres grupos alquilo (sin átomos de hidrógeno unidos directamente a ese átomo de carbono) y un átomo de halógeno. La estructura general de un haloalcano terciario es R3-CX, donde tres grupos R (grupos alquilo) pueden ser grupos iguales o diferentes. Podemos denotar estas conexiones como 30 haloalcanos. Además, estos compuestos experimentan reacciones de sustitución nucleófila SN1. Sin embargo, este mecanismo difiere de las reacciones de sustitución nucleófila de los haloalcanos primarios y secundarios.
El átomo de carbono que lleva el átomo de halógeno tiene una carga positiva muy débil porque tres grupos atractores de electrones están unidos a este átomo de carbono. Por lo tanto, no se requiere la formación de intermediarios de alta energía y el nucleófilo puede atacar directamente al ion carbonio una vez que se forma. Por eso la llamamos reacción unimolecular.
¿Cuál es la diferencia entre los haloalcanos primarios, secundarios y terciarios?
Dependiendo de la estructura, los haloalcanos son de tres tipos; haloalcanos primarios, secundarios y terciarios. En los haloalcanos primarios, el átomo de carbono que lleva el átomo de halógeno está unido a un solo grupo alquilo, y en los haloalcanos secundarios, ese átomo de carbono está unido a dos grupos alquilo, mientras que en los haloalcanos terciarios, ese átomo de carbono está unido a tres grupos alquilo. Entonces, esta es la diferencia clave entre los haloalcanos primarios secundarios y terciarios.
Resumen: haloalcanos primarios, secundarios y terciarios
Dependiendo de la estructura, existen tres tipos de haloalcanos; haloalcanos primarios, secundarios y terciarios. La principal diferencia entre los haloalcanos primarios, secundarios y terciarios es que en los haloalcanos primarios, el átomo de carbono que lleva el átomo de halógeno está unido a un solo grupo alquilo. Y en los haloalcanos secundarios, ese átomo de carbono está unido a dos grupos alquilo. Por el contrario, en los haloalcanos terciarios, este átomo de carbono está unido a tres grupos alquilo.
Relación:
1. "10.34 - Haloalcanos". Química OrgánicaDisponible aquí.
Imagen de cortesía:
1. "2-bromopropano-2D-flat" por Ben Mills - Trabajo propio (Dominio público) a través de Commons Wikimedia