Puede dar por sentado que la materia está formada por átomos, pero lo que consideramos conocimiento común era desconocido hasta hace relativamente poco tiempo en la historia humana. La mayoría de los historiadores de la ciencia atribuyen a John Dalton, físico, químico y meteorólogo británico, el desarrollo de la teoría atómica moderna.
Teorías Tempranas
Si bien los antiguos griegos creían que los átomos formaban la materia, no estaban de acuerdo sobre qué eran los átomos. Demócrito registró que Leucipo creía que los átomos eran cuerpos pequeños e indestructibles que podían combinarse para cambiar las propiedades de la materia. Aristóteles creía que cada elemento tenía su propia "esencia" especial, pero no creía que las propiedades se extendieran hasta partículas diminutas e invisibles. Nadie cuestionó realmente la teoría de Aristóteles, ya que no existían herramientas para examinar la materia en detalle.
Lectura relacionada: Diagrama de Flujo del Método Científico
Diagrama de Flujo del Método Científico
A Lo Largo viene Dalton
Por lo tanto, no fue hasta el siglo XIX que los científicos realizaron experimentos sobre la naturaleza de la materia. Los experimentos de Dalton se centraron en los gases: sus propiedades, lo que sucedía cuando se combinaban y las similitudes y diferencias entre los diferentes tipos de gases. Lo que aprendió lo llevó a proponer varias leyes, que se conocen colectivamente como Teoría Atómica de Dalton o Leyes de Dalton:
- Los átomos son partículas de materia pequeñas y químicamente indestructibles. Los elementos consisten en átomos.
- Los átomos de un elemento comparten propiedades comunes.
- Los átomos de diferentes elementos tienen diferentes propiedades y diferentes pesos atómicos.
- Los átomos que interactúan entre sí obedecen la Ley de Conservación de la Masa. Esencialmente, esta ley establece que el número y los tipos de átomos que reaccionan son iguales al número y los tipos de átomos en los productos de una reacción química.
- Los átomos que se combinan entre sí obedecen la Ley de las Proporciones Múltiples. En otras palabras, cuando los elementos se combinan, la relación en la que se combinan los átomos se puede expresar como una relación de números enteros.
Dalton también es conocido por proponer leyes de gases (Ley de Presiones Parciales de Dalton) y explicar el daltonismo. No todos sus experimentos científicos podrían considerarse exitosos. Por ejemplo, algunos creen que el derrame cerebral que sufrió podría haber resultado de una investigación en la que se usó a sí mismo como sujeto, en la que se pinchó en la oreja con un palo afilado para "investigar los humores que se mueven dentro de mi cráneo.”
Lectura relacionada: Cómo Hacer una Rosa Arcoíris Real
Cómo Hacer una Rosa Arcoíris Real
Fuentes
- Grossman, M. I. (2014). "John Dalton y los atomistas de Londres: William y Bryan Higgins, William Austin y las nuevas dudas daltónicas sobre el origen de la teoría atómica." Notas y Registros. 68 (4): 339–356. doi:10.1098/rsnr.2014.0025
- Levere, Trevor (2001). Transformando la Materia: Una Historia de la Química de la Alquimia al Buckyball. Baltimore, Maryland: Prensa de la Universidad Johns Hopkins. pp.84-86. ISBN 978-0-8018-6610-4.
- Rocke, Alan J. (2005). "En busca de El Dorado: John Dalton y los orígenes de la Teoría Atómica."Investigación Social. 72 (1): 125–158. JSTOR 40972005
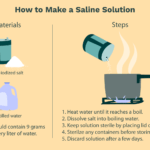 Cómo hacer Solución Salina en Casa
Cómo hacer Solución Salina en Casa