
Que diferencia principal entre compuestos iónicos y moleculares es que la Los compuestos iónicos tienen fuerzas de atracción electrostática entre cationes y aniones, mientras que los compuestos moleculares solo tienen enlaces químicos covalentes entre átomos.
Lectura relacionada: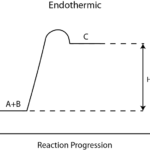 Diferencia entre reacciones endotérmicas y exotérmicas.
Diferencia entre reacciones endotérmicas y exotérmicas.Los elementos químicos pueden combinarse para formar compuestos químicos. Los elementos se conectan a través de enlaces químicos que tienen propiedades iónicas o covalentes. Si los compuestos tienen enlaces iónicos los llamamos compuestos iónicos y si tienen enlaces covalentes entonces son compuestos moleculares. Por lo tanto, la principal diferencia entre los compuestos iónicos y moleculares radica en el enlace químico entre los átomos.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué son los compuestos iónicos?
3. ¿Qué son los compuestos moleculares?
4. Comparación lado a lado: compuestos iónicos y moleculares en forma tabular
5. Resumen
¿Qué son los compuestos iónicos?
Los compuestos iónicos son los compuestos químicos que tienen cationes y aniones que se unen entre sí a través de enlaces iónicos. Por lo tanto, existen fuerzas de atracción electrostática entre cationes y aniones. Sin embargo, el compuesto tiene una carga global neutra porque la carga global de los cationes es neutralizada por la carga global de los aniones. Estos iones pueden ser monoatómicos o poliatómicos.
Lectura relacionada: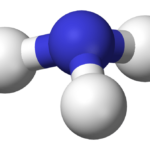 Diferencia entre amoníaco y amonio.
Diferencia entre amoníaco y amonio.Por lo general, los compuestos iónicos que contienen iones de hidrógeno (H+) como catión son “ácidos”. Por el contrario, los iones básicos como los iones de hidróxido (OH–) está presente en las bases. Si no hay iones de hidrógeno o iones de hidróxido presentes en el compuesto iónico, lo llamamos "sal".

Figura 01: Compuesto iónico de cloruro de sodio que es una sal.
Lectura relacionada: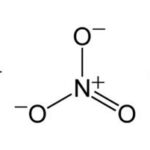 Diferencia entre nitrato y nitrito.
Diferencia entre nitrato y nitrito.Algunos compuestos iónicos, como las sales, se forman a partir de reacciones de neutralización ácido-base. Algunos compuestos se forman a partir de la evaporación de solventes, reacciones de precipitación, reacciones de estado sólido, congelación, reacciones de transferencia de electrones entre metales y no metales, etc. Por lo general, estos compuestos tienen puntos de fusión y ebullición altos. En su mayoría son duros y quebradizos. Casi todos los compuestos iónicos son aislantes eléctricos en su estado sólido y pueden volverse altamente conductores cuando se disuelven en un solvente como el agua porque los cationes y aniones pueden moverse libremente.
¿Qué son los compuestos moleculares?
Los compuestos moleculares son compuestos químicos que contienen átomos unidos por enlaces químicos covalentes. Por lo tanto, estos compuestos se forman cuando los átomos comparten sus electrones desapareados entre sí. Los átomos involucrados en este intercambio de electrones tienen valores de electronegatividad similares.

Figura 02: diagrama de una molécula triatómica que muestra enlaces covalentes entre los tres átomos
Por lo general, los compuestos moleculares tienen puntos de fusión y ebullición relativamente bajos porque los átomos no están fuertemente unidos entre sí. De manera similar, estos compuestos son blandos y relativamente flexibles. En comparación con los compuestos iónicos, estos compuestos moleculares son altamente inflamables. Porque casi todas las sustancias combustibles son compuestos moleculares formados por átomos de carbono e hidrógeno. A diferencia de los compuestos iónicos, no pueden conducir electricidad cuando se disuelven en un solvente porque no hay iones disponibles para la separación una vez disueltos.
¿Cuál es la diferencia entre compuestos iónicos y moleculares?
Los compuestos iónicos son compuestos químicos con cationes y aniones que se unen entre sí mediante enlaces iónicos, mientras que los compuestos moleculares son compuestos químicos que contienen átomos unidos entre sí mediante enlaces químicos covalentes. Por lo tanto, la diferencia entre los compuestos iónicos y moleculares radica en el tipo de enlace químico. Eso es; los diferencia clave entre los compuestos iónicos y moleculares es que los compuestos iónicos tienen fuerzas de atracción electrostática entre cationes y aniones, mientras que los compuestos moleculares solo tienen enlaces químicos covalentes entre los átomos.
Como otra diferencia importante entre los compuestos iónicos y moleculares, los compuestos iónicos son duros y quebradizos, mientras que los compuestos moleculares son blandos y relativamente flexibles. Esto se debe principalmente a que los átomos de los compuestos iónicos se mantienen unidos entre sí mediante enlaces iónicos, mientras que los átomos de los compuestos moleculares están relativamente poco unidos entre sí. Además, los puntos de fusión y ebullición de los compuestos iónicos son muy altos en comparación con los compuestos moleculares.

Resumen: compuestos iónicos y moleculares
Los compuestos iónicos tienen enlaces iónicos, mientras que los compuestos moleculares tienen enlaces covalentes. Por lo tanto, la diferencia clave entre los compuestos iónicos y moleculares es que los compuestos iónicos tienen fuerzas de atracción electrostática entre cationes y aniones, mientras que los compuestos moleculares solo tienen enlaces químicos covalentes entre los átomos.
Relación:
1. Helmenstina, Anne Marie, Ph.D. "Propiedades de los compuestos covalentes o moleculares". ThoughtCo, 7 de junio de 2018. Disponible aquí
2. "Compuesto iónico". Wikipedia, Fundación Wikimedia, 20 de octubre de 2018. Disponible aquí
Imagen de cortesía:
1. "Iones 3D de cloruro de sodio" Por Benjah-bmm27 - Trabajo propio, (Dominio público) a través de Commons Wikimedia
2. "Dióxido de carbono-3D-vdW" Por Jacek FH - Trabajo propio (CC BY-SA 3.0) a través de Commons Wikimedia











