Diferencia principal - isomorfismo contra polimorfismo
Los compuestos pueden ocurrir en la naturaleza en diferentes formas. Estas diferentes formas pueden ser diferentes morfologías o diferentes estructuras. La estructura de un compuesto químico determina las propiedades físicas de ese compuesto. A veces, las propiedades químicas también están determinadas por la estructura. "Morfismo" es un término utilizado para denotar el término "morfología". Describe la apariencia externa de una conexión. Los términos isomorfismo y polimorfismo se utilizan para describir estos fenómenos externos. Polimorfismo significa la presencia de un compuesto en más de una forma cristalina. El isomorfismo es la presencia de dos o más compuestos con la misma morfología. Que diferencia principal entre isomorfismo y polimorfismo es que El isomorfismo se refiere a la presencia de dos o más compuestos con morfologías idénticas, mientras que el polimorfismo se refiere a la presencia de diferentes morfologías de la misma sustancia.
Lectura relacionada: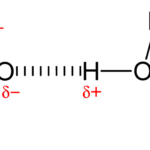 Diferencia entre enlaces de hidrógeno intermoleculares e intramoleculares.
Diferencia entre enlaces de hidrógeno intermoleculares e intramoleculares.CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el isomorfismo?
3. ¿Qué es el polimorfismo?
4. Comparación lado a lado: isomorfismo frente a polimorfismo en forma tabular
5. Resumen
¿Qué es el isomorfismo?
El isomorfismo se refiere a la presencia de dos o más compuestos con morfologías idénticas. Esto significa la presencia de la misma estructura cristalina en diferentes compuestos. Estos compuestos se denominan isomorfos. Las sustancias isomórficas tienen casi la misma forma y estructura.
Estos compuestos tienen la misma proporción entre los átomos presentes en estos compuestos. Esto indica que las fórmulas empíricas de las sustancias isomórficas son idénticas. Sin embargo, las propiedades físicas de las sustancias isomórficas son diferentes entre sí porque tienen diferentes combinaciones de átomos. Ej: masa, densidad, reactividad química son algunas de las propiedades físicas que difieren entre las sustancias isomórficas. Veamos algunos ejemplos para entender qué es el isomorfismo en química.
Lectura relacionada: Diferencia entre las fuerzas ion dipolo y dipolo dipolo
Diferencia entre las fuerzas ion dipolo y dipolo dipolo- Carbonato de calcio (CaCO3) y nitrato de sodio (NaNO3).

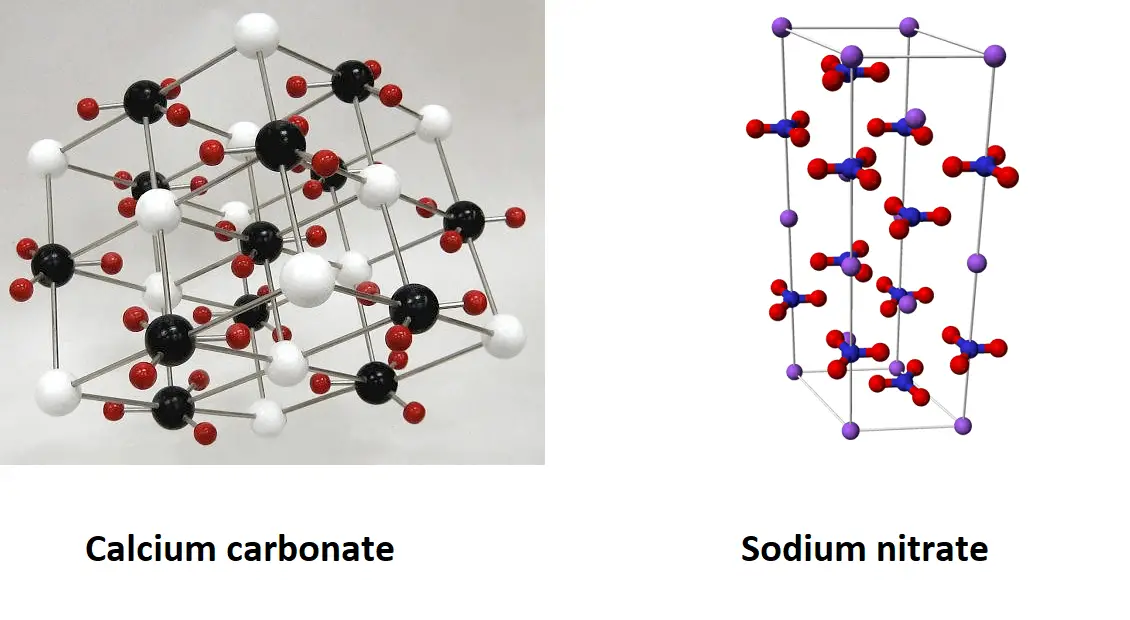
Figura 01: La comparación de carbonato de calcio y nitrato de sodio como isomorfos
Tanto el carbonato de calcio como el nitrato de sodio tienen forma trigonal. La relación atómica de los átomos presentes en cada compuesto es 1:1:3. Pero estos compuestos tienen diferentes propiedades físicas y químicas. Sus masas molares también son diferentes (carbonato de calcio = 100 g/mol y nitrato de sodio = 85 g/mol).
Lectura relacionada: Diferencia entre blindaje y efecto de blindaje.
Diferencia entre blindaje y efecto de blindaje.- Fosfato de sodio (Na3correos4) y arseniato de sodio ( Na3ComoO4).
Estos compuestos existen en forma tetraédrica y la fórmula empírica de estos compuestos tiene la relación atómica 3:1:4. Pero tienen diferentes propiedades químicas y físicas.
¿Qué es el polimorfismo?
El polimorfismo se refiere a la presencia de diferentes morfologías de la misma sustancia. La sustancia que muestra polimorfismo se denomina sustancias polimórficas. Aquí existe un determinado compuesto en diferentes formas y formas cristalinas.
Los polimorfos muestran similitudes y diferencias basadas en la estructura. Pero la mayoría de las propiedades químicas son las mismas ya que es el mismo compuesto que viene en diferentes formas. Pero las propiedades físicas son diferentes. , CaCO3 (carbonato de calcio) existen en forma ortorrómbica o en forma hexagonal.

Figura 02: alótropos de carbono
La alotropía es un término relacionado con el polimorfismo. La alotropía se refiere al polimorfismo de un elemento en particular. Los compuestos que muestran alotropía se conocen como alótropos. Los alótropos ocurren cuando un elemento forma una estructura cristalina con diferentes arreglos. Por ejemplo, el carbono forma alótropos como el diamante o el grafito. Estos alótropos tienen diferentes propiedades químicas y físicas.
¿Cuál es la diferencia entre isomorfismo y polimorfismo?
Isomorfismo versus polimorfismo |
|
| El isomorfismo se refiere a la presencia de dos o más compuestos con morfologías idénticas. | El polimorfismo se refiere a la presencia de diferentes morfologías de la misma sustancia. |
| forma | |
| Las sustancias isomórficas tienen formas idénticas. | Las sustancias polimórficas tienen diferentes formas. |
| conexión | |
| El isomorfismo se refiere a dos o más compuestos diferentes. | El polimorfismo describe las diferentes formas de un mismo compuesto o elemento. |
| con elementos | |
| El isomorfismo está ausente en los elementos. | El polimorfismo está presente en los elementos. |
| relación atómica | |
| Las sustancias isomórficas tienen la misma proporción atómica en la fórmula molecular. | Los polimorfos tienen proporciones atómicas similares o diferentes. |
Resumen - isomorfismo contra polimorfismo
El isomorfismo y el polimorfismo expresan dos ideas opuestas. La diferencia entre isomorfismo y polimorfismo es que el isomorfismo se refiere a la presencia de dos o más compuestos con morfologías idénticas, mientras que el polimorfismo se refiere a la presencia de diferentes morfologías de la misma sustancia.
Relación:
1. "Cristalización y polimorfismo". Sociedad Química Americana. Disponible aquí
2. "Isomorfismo (cristalografía)". Wikipedia, Fundación Wikimedia, 17 de febrero de 2018. Disponible aquí
3. "Alotropía". Wikipedia, Fundación Wikimedia, 3 de marzo de 2018. Disponible aquí
Imagen de cortesía:
1. 'Estructura de calcita CaCO3' por Tem5psu - Trabajo propio, (CC BY-SA 4.0) a través de Commons Wikimedia (Modificado)
2. "Esferas 3D de celdas unitarias de nitrato de sodio" por Ben Mills - Trabajo propio, (Dominio público) a través de Commons Wikimedia (Modificado)
3. 'Alótropos de carbono' por Mstroeck (conferencia) (Cargas) - Trabajo propio, (CC BY-SA 3.0) a través de Commons Wikimedia