En química, precipitar es formar un compuesto insoluble haciendo reaccionar dos sales o cambiando la temperatura para afectar la solubilidad del compuesto. Además, "precipitado" es el nombre dado al sólido que se forma como resultado de una reacción de precipitación.
La precipitación puede indicar que se ha producido una reacción química, pero también puede ocurrir si una concentración de soluto excede su solubilidad. La precipitación está precedida por un evento llamado nucleación, que es cuando pequeñas partículas insolubles se agregan entre sí o forman una interfaz con una superficie, como la pared de un recipiente o un cristal de siembra.
Conclusiones Clave: Definición de Precipitado en Química
- En química, precipitado es tanto un verbo como un sustantivo.
- Precipitar es formar un compuesto insoluble, ya sea disminuyendo la solubilidad de un compuesto o haciendo reaccionar dos soluciones salinas.
- El sólido que se forma a través de una reacción de precipitación se llama precipitado.
- Las reacciones de precipitación cumplen funciones importantes. Se utilizan para la purificación, eliminación o recuperación de sales, para la fabricación de pigmentos y para identificar sustancias en análisis cualitativos.
Lectura relacionada:
 Qué significan los Números de la Tabla Periódica
Qué significan los Números de la Tabla PeriódicaPrecipitado vs Precipitante
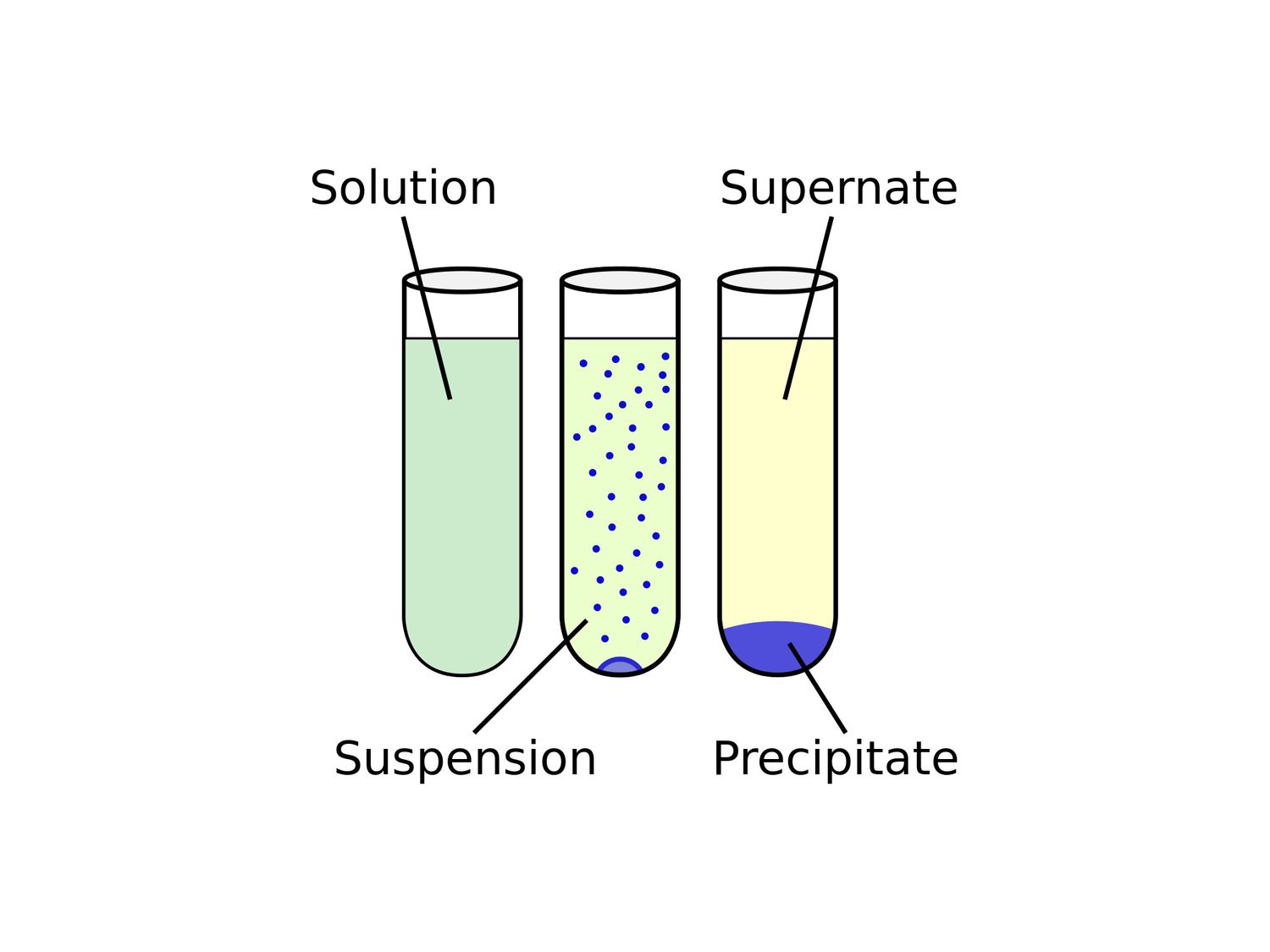
La terminología puede parecer un poco confusa. Así es como funciona: la formación de un sólido a partir de una solución se llama precipitación. Una sustancia química que hace que se forme un sólido en una solución líquida se llama precipitante. El sólido que se forma se llama precipitado. Si el tamaño de partícula del compuesto insoluble es muy pequeño o no hay suficiente gravedad para llevar el sólido al fondo del recipiente, el precipitado puede distribuirse uniformemente por todo el líquido, formando un suspensión. Sedimentación se refiere a cualquier procedimiento que separa el precipitado de la porción líquida de la solución, que se denomina sobrenadante. Una técnica de sedimentación común es la centrifugación. Una vez que se ha recuperado el precipitado, el polvo resultante puede denominarse "flor"."
Ejemplo de Precipitación
Mezclar nitrato de plata y cloruro de sodio en agua hará que el cloruro de plata precipite de la solución en forma de un sólido. En este ejemplo, el precipitado es cloruro de plata.
Lectura relacionada: Nomenclatura y Numeración de Alcanos
Nomenclatura y Numeración de Alcanos
Al escribir una reacción química, la presencia de un precipitado puede indicarse siguiendo la fórmula química con una flecha apuntando hacia abajo:
Ag+ + Cl- → AgCl↓
Lectura relacionada:
 Tabla Periódica de Colores de los Elementos Con Cargas
Tabla Periódica de Colores de los Elementos Con CargasUsos de los Precipitados
Los precipitados se pueden usar para identificar el catión o anión en una sal como parte del análisis cualitativo. Se sabe que los metales de transición, en particular, forman diferentes colores de precipitados dependiendo de su identidad elemental y estado de oxidación. Las reacciones de precipitación se utilizan para eliminar sales del agua, aislar productos y preparar pigmentos. En condiciones controladas, una reacción de precipitación produce cristales puros de precipitado. En metalurgia, la precipitación se utiliza para fortalecer las aleaciones.
Cómo Recuperar un Precipitado
Existen varios métodos utilizados para recuperar un precipitado:
Filtración: En la filtración, la solución que contiene el precipitado se vierte sobre un filtro. Idealmente, el precipitado permanece en el filtro, mientras que el líquido pasa a través de él. El recipiente puede enjuagarse y verterse sobre el filtro para ayudar a la recuperación. Siempre hay alguna pérdida del precipitado que puede ser causada por la disolución en el líquido, el paso a través del filtro o la adhesión al medio filtrante.
Centrifugación: En la centrifugación, la solución se hace girar rápidamente. Para que la técnica funcione, el precipitado sólido debe ser más denso que el líquido. El precipitado compactado, denominado gránulo, se puede obtener vertiendo el líquido. Típicamente, hay menos pérdida con la centrifugación que con la filtración. La centrifugación funciona bien con tamaños de muestra pequeños.
Decantación: En la decantación, la capa líquida se vierte o se succiona del precipitado. En algunos casos, se añade un disolvente adicional para separar la solución del precipitado. La decantación se puede usar con la solución completa o después de la centrifugación.
Envejecimiento o Digestión Precipitados
Un proceso llamado envejecimiento o digestión del precipitado ocurre cuando se deja que un precipitado nuevo permanezca en su solución. Típicamente, se aumenta la temperatura de la solución. La digestión puede producir partículas más grandes con una pureza más alta. El proceso que conduce a este resultado se conoce como maduración de Ostwald.
Fuentes
- Adler, Alan D.; Longo, Frederick R.; Kampas, Frank; Kim, Jean (1970). "Sobre la preparación de metaloporfirinas". Revista de Química Inorgánica y Nuclear. 32 (7): 2443. doi:10.1016/0022-1902 (70) 80535-8
- Dhara, S. (2007). "Formación, Dinámica y Caracterización de Nanoestructuras mediante Irradiación con Haz de Iones". Revisiones Críticas en Ciencias del Estado Sólido y de los Materiales. 32 (1): 1-50. doi:10.1080/10408430601187624
- Zumdahl, Steven S. (2005). Principios Químicos (5ª ed.). Nueva York: Houghton Mifflin. ISBN 0-618-37206-7.