Que diferencia principal entre 1 propanol y 2 propanol que es El 1-propanol tiene su grupo hidroxilo unido al final de la cadena de carbono, mientras que el 2-propanol tiene el grupo hidroxilo unido al átomo de carbono medio de la cadena de carbono.
Tanto el 1-propanol como el 2-propanol son dos formas isoméricas de la molécula de propanol. El propanol es un alcohol que contiene tres átomos de carbono en una estructura de cadena de carbono y hay un grupo hidroxilo (-OH) como grupo funcional de la molécula. Además, la diferencia fundamental entre el 1-propanol y el 2-propanol es dónde se une este grupo hidroxilo a la cadena de carbono.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es 1 propanol?
3. ¿Qué es el 2-propanol?
4. Comparación lado a lado: 1 propanol frente a 2 propanol en forma tabular
5. Resumen
 Diferencia entre actividad y volatilidad
Diferencia entre actividad y volatilidad¿Qué es el 1-propanol?
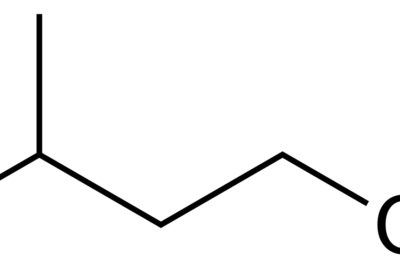
1 El propanol es el compuesto orgánico con la fórmula química C3H8O. Es un alcohol primario porque el grupo hidroxilo está unido al átomo de carbono al final de la cadena de carbono. Dado que solo hay otro átomo de carbono unido a este átomo de carbono, es un alcohol primario. También es un isómero de 2-propanol.

Figura 01: Estructura de 1 propanol
Lectura relacionada: Diferencia entre oxicloruro de cobre y sulfato de cobre.
Diferencia entre oxicloruro de cobre y sulfato de cobre.Este compuesto se forma naturalmente en pequeñas cantidades en muchos procesos de fermentación. La masa molar es 60,09 g/mol. También aparece como un líquido incoloro con un olor alcohólico suave. Además, este compuesto es importante como disolvente en la industria farmacéutica. Debido al alto octanaje, también es adecuado como combustible para motores.
¿Qué es el 2-propanol?
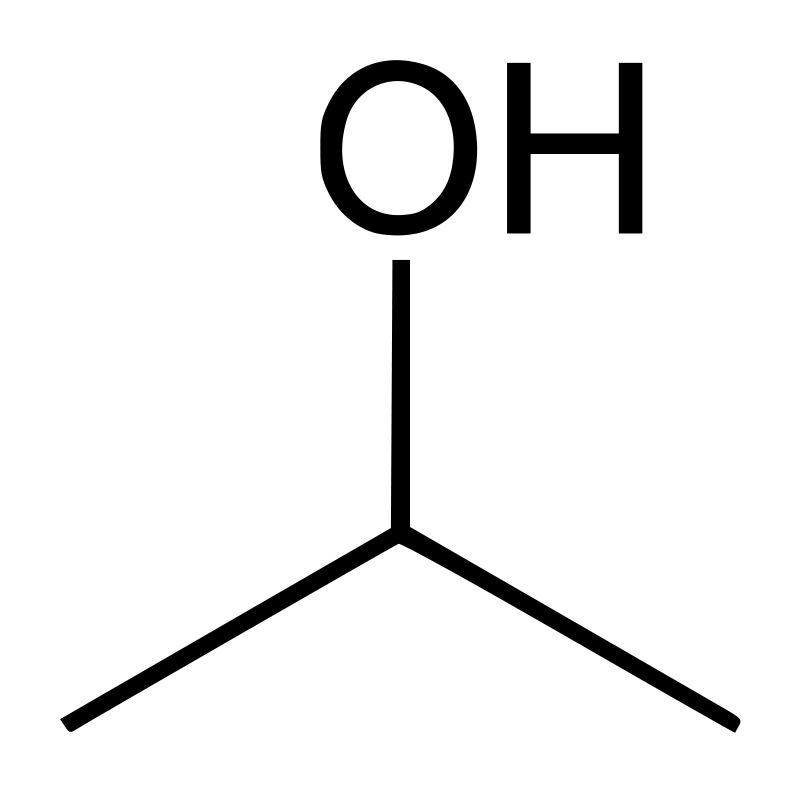
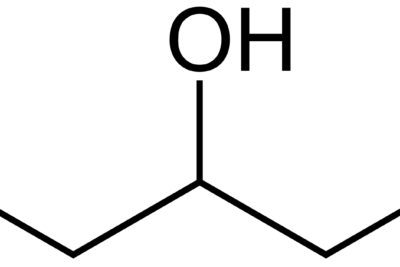
El 2-propanol es el compuesto orgánico de fórmula química C3H8O, y es un isómero de 1-propanol. Como nombre común, lo llamamos alcohol isopropílico. Se presenta como un líquido incoloro e inflamable. Además, tiene un olor fuerte. El grupo hidroxilo en este compuesto está unido al átomo de carbono medio de la cadena de carbono. Por lo tanto, es un alcohol secundario. También es un isómero estructural de 1-propanol.

 Diferencia entre la reacción de Sandmeyer y la reacción de Gattermann
Diferencia entre la reacción de Sandmeyer y la reacción de GattermannFigura 02: Estructura de 2-Propanol
Además, esta sustancia es miscible con agua, etanol, éter y cloroformo. Con la disminución de la temperatura, la viscosidad de este líquido aumenta bruscamente. Se puede oxidar a acetona. Además, el principal método de producción de 2-propanol es la hidratación indirecta; La reacción de propeno con ácido sulfúrico forma una mezcla de ésteres de sulfato y la posterior hidrólisis de estos ésteres da alcohol isopropílico.
En términos de utilidad, es útil como solvente para disolver una variedad de compuestos no polares. Ej: limpieza de vidrios, electrónica, etc. También es importante como intermediario químico en la fabricación de acetato de isopropilo. Además, la producción de alcohol para fricciones a partir de alcohol isopropílico es importante para aplicaciones médicas.
¿Cuál es la diferencia entre 1 propanol y 2 propanol?
1 El propanol es el compuesto orgánico con la fórmula química C3H8O, mientras que el 2-propanol es el compuesto orgánico con fórmula química C3H8O y es un isómero de 1-propanol. Entonces, la diferencia clave entre el 1-propanol y el 2-propanol es que el grupo hidroxilo del 1-propanol está unido al final de la cadena de carbono, mientras que el grupo hidroxilo del 2-propanol está unido al átomo de carbono medio de la cadena de carbono. .
Resumen: 1 propanol frente a 2 propanol
1 El propanol es el compuesto orgánico con la fórmula química C3H8O, mientras que el 2-propanol es el compuesto orgánico con fórmula química C3H8O y es n-isómero de 1-propanol. En resumen, la principal diferencia entre el 1-propanol y el 2-propanol es que el grupo hidroxilo del 1-propanol está unido al final de la cadena de carbono, mientras que el grupo hidroxilo del 2-propanol está unido al átomo de carbono central del carbono. cadena.
Relación:
1. “Propanol”. Centro Nacional de Información Biotecnológica. Base de datos compuesta de PubChem, Biblioteca Nacional de Medicina de EE. UU., disponible aquí.
Imagen de cortesía:
1. "Propan-1-ol" por Usuario: Bryan Derksen - Trabajo propio (Dominio público) a través de Commons Wikimedia
2. "2-Propanol" por Yikrazuul - Trabajo propio (Dominio público) a través de Commons Wikimedia