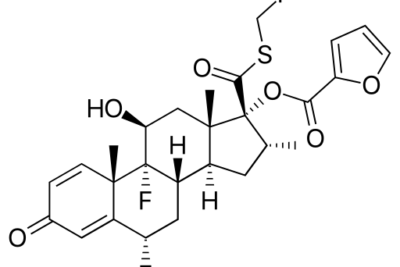
La diferencia principal se encuentra entre la O-acilación y la N-acilación La O-acilación forma un producto final oxigenado mientras que la N-acilación forma un producto final nitrogenado..
La acilación es el proceso químico que agrega un grupo acilo a un compuesto químico. En este método, el compuesto que proporciona el grupo acilo se denomina agente acilante. Un grupo acilo tiene la fórmula química RC(=O)-, donde R es un grupo arilo o alquilo. De acuerdo con el producto final de la acilación, existen tres procesos principales de acilación como C-acilación, O-acilación y N-acilación. Este artículo analiza las reacciones de O-acilación y N-acilación.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la O-Acilación?
3. ¿Qué es la N-acilación?
4. Comparación lado a lado: O-acilación frente a N-acilación en forma tabular
5. Resumen
 Diferencia entre monovalente y bivalente
Diferencia entre monovalente y bivalente¿Qué es la O-Acilación?
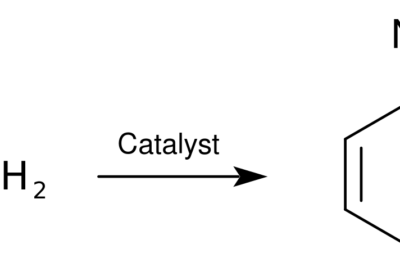
La O-acilación es un tipo de proceso de acilación en el que el producto final contiene un átomo de oxígeno que conecta el grupo acilo con el compuesto reactivo. En otras palabras, hay un átomo de oxígeno entre el grupo acilo y el resto del compuesto reactivo. La O-acilación es un tipo de reacción de sustitución de acilo nucleofílica. Para este proceso, el agente acilante suele ser cloruro de acilo o anhídrido de acilo. Este tipo de acilación ocurre con las moléculas de reactivo que contienen grupos -OH, como los alcoholes arílicos o alquílicos.

Figura 01: Un proceso de acilación típico
Lectura relacionada: Diferencia entre la condensación de Claisen y Dieckmann
Diferencia entre la condensación de Claisen y Dieckmann¿Qué es la N-acilación?
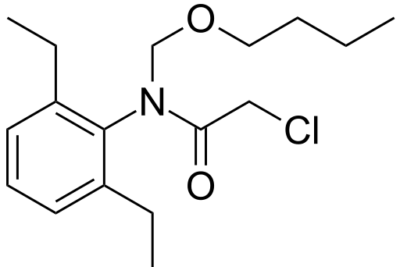
La N-acilación es un tipo de acilación en la que el producto final contiene un átomo de nitrógeno que conecta el grupo acilo con el compuesto reactivo. En otras palabras, hay un átomo de nitrógeno entre el grupo acilo y el resto del compuesto reactivo.

Figura 02: Mecanismo de una reacción de N-acilación
Lectura relacionada: Diferencia entre cloruro de etilo y cloruro de vinilo.
Diferencia entre cloruro de etilo y cloruro de vinilo.La N-acilación es un tipo de reacción de acilación electrofílica. Para este proceso, el agente acilante suele ser cloruro de acilo o anhídrido de acilo. Este tipo de reacciones ocurre con las moléculas reactivas que contienen grupos -NH como la anilina. Por ejemplo, la N-acilación de la anilina es una vía eficaz cuando se utiliza anhídrido acético como agente acilante.
¿Cuál es la diferencia entre O-acilación y N-acilación?
De acuerdo con el producto final del proceso de acilación, existen tres procesos principales de acilación como C-acilación, O-acilación y N-acilación. La O-acilación es un tipo de proceso de acilación en el que el producto final contiene un átomo de oxígeno que conecta el grupo acilo con el compuesto reactivo, mientras que la N-acilación es un tipo de acilación en el que el producto final contiene un átomo de nitrógeno que conecta el grupo acilo con el reactivo. compuesto
Por lo tanto, la principal diferencia entre la O-acilación y la N-acilación es que la O-acilación forma un producto final oxigenado, mientras que la N-acilación forma un producto final nitrogenado. Los reactivos que experimentan reacciones de O-acilación son compuestos que contienen grupos -OH, como los fenoles. Los reactivos que experimentan N-acilación son compuestos con grupos -NH como la anilina. Además, la O-acilación es un tipo de reacción de sustitución de acilo nucleofílica, mientras que la N-acilación es un tipo de reacción de cambio de acilación electrófila.
Resumen: O-acilación frente a N-acilación
De acuerdo con el producto final del proceso de acilación, existen tres procesos principales de acilación como C-acilación, O-acilación y N-acilación. La diferencia clave entre la O-acilación y la N-acilación es que la O-acilación forma un producto final oxigenado, mientras que la N-acilación forma un producto final nitrogenado.
Relación:
1. Ouarna, Souad, et al. "Una ruta altamente eficiente y respetuosa con el medio ambiente para la N-acilación en condiciones sin catalizador". Revista oriental de química20 de junio de 2015, disponible aquí.
2. Caza, Ian. "Ch24 - Acilación de fenoles". Instituto de QuímicaUniversidad de Calgary, disponible aquí.
Imagen de cortesía:
1. "Acylation Friedel-Crafts" por Prepapc - Trabajo propio, CC BY-SA 3.0) a través de Commons Wikimedia
2. "Mecanismo de N-acilación usando HATU" por Dar58 en Wikipedia en inglés, CC BY-SA 3.0) a través de Commons Wikimedia