Que Diferencia clave entre la sustitución de radicales y la adición de radicales es que la sustitución radical implica el reemplazo de un grupo funcional con otro grupo funcional, mientras que la adición radical implica la adición de un nuevo grupo funcional a una molécula.
Un radical libre puede ser un átomo, una molécula o un ion compuesto por un electrón de valencia desapareado. Hay dos tipos principales de reacciones de radicales libres: sustitución de radicales libres y reacciones de adición de radicales libres.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es un radical libre?
3. ¿Qué es la sustitución de radicales libres?
4. ¿Qué es la adición de radicales libres?
5. Sustitución de radicales libres frente a adición de radicales libres en forma tabular
6. Resumen: sustitución de radicales libres frente a adición de radicales libres
 Diferencia entre mica y pigmento.
Diferencia entre mica y pigmento.¿Qué es un radical libre?
Un radical libre puede ser un átomo, una molécula o un ion compuesto por un electrón de valencia desapareado. Normalmente, estos electrones desapareados pueden hacer que los radicales libres sean altamente reactivos químicamente; sin embargo, puede haber algunas excepciones. Debido a su alta reactividad, la mayoría de los radicales libres tienden a dimerizarse espontáneamente. Por lo tanto, tienen una vida útil muy corta.
¿Qué es la sustitución de radicales libres?
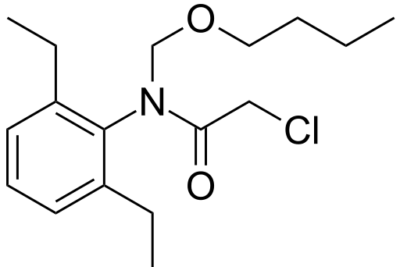
La sustitución por radicales libres es un tipo de reacción de sustitución en la que intervienen radicales libres como intermedio reactivo. Los intermedios reactivos son moléculas de vida corta, de alta energía y altamente reactivas. Estas moléculas se forman durante una reacción química que tiende a transformarse rápidamente en moléculas más estables. Además, una reacción de sustitución es un tipo de reacción química en la que un grupo funcional de un compuesto químico tiende a ser reemplazado por otro grupo funcional.

 Diferencia entre PFOA y PFOS
Diferencia entre PFOA y PFOSFigura 01: Diferentes pasos en las reacciones de radicales libres.
La imagen de arriba muestra los pasos de las reacciones radicales en general; Los pasos 2 y 3 se denominan reacciones de iniciación, donde se forman radicales libres a través de la homólisis. La homólisis se puede llevar a cabo usando calor o luz ultravioleta y usando iniciadores de radicales libres, p. B. Se pueden lograr peróxidos orgánicos, compuestos azoicos, etc. Los pasos finales 6 y 7 se denominan colectivamente terminación; aquí el radical tiende a recombinarse con otra especie de radical. Sin embargo, el radical a veces continúa reaccionando donde ocurre la propagación. La propagación resulta de los pasos 4 y 5 en la imagen de arriba.
Algunos ejemplos de reacciones de sustitución de radicales incluyen la desoxigenación de Barton-McCombie, la reacción de Wohl-Ziegler, la reacción de Dowd-Beckwith, etc.
Lectura relacionada: Diferencia entre sal compleja y sal doble.
Diferencia entre sal compleja y sal doble.¿Qué es la adición de radicales libres?
La adición de radicales libres es un tipo de reacción de adición en la que se agrega un grupo funcional a un compuesto a través de un intermedio radicalmente reactivo. Este tipo de adición puede tener lugar entre una especie radical y una no radical o entre dos especies radicales. Los pasos básicos de la adición de radicales libres incluyen la iniciación, la propagación de la cadena y la terminación de la cadena.

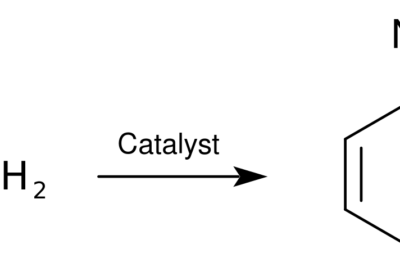
Figura 02: Adición radical de HBr a alquenos.
Durante el proceso de iniciación, se usa un iniciador de radicales libres para la iniciación, formando una especie de radicales libres a partir de un precursor que no es de radicales libres. Durante el proceso de propagación de la cadena, un radical libre tiende a reaccionar con una especie no radical para crear una nueva especie radical. El paso final es la terminación de la cadena, donde los dos radicales reaccionan entre sí, creando una especie no radical. Un ejemplo común de este tipo de reacción es la arilación de Meerwein.
Por lo general, las reacciones de adición de radicales libres se basan en reactivos débilmente enlazados para que puedan someterse a homólisis para formar especies de radicales. Cuando hay enlaces fuertes, el mecanismo de reacción difiere de las reacciones habituales de adición de radicales libres.
¿Cuál es la diferencia entre la sustitución de radicales libres y la adición de radicales libres?
Un radical libre puede ser un átomo, una molécula o un ion compuesto por un electrón de valencia desapareado. La diferencia clave entre la sustitución de radicales y la adición de radicales es que la sustitución de radicales implica reemplazar un grupo funcional con otro grupo funcional, mientras que la adición de radicales implica agregar un nuevo grupo funcional a una molécula.
Resumen: sustitución de radicales libres frente a adición de radicales libres
Un radical libre puede ser un átomo, una molécula o un ion compuesto por un electrón de valencia desapareado. La diferencia clave entre la sustitución de radicales y la adición de radicales es que la sustitución de radicales implica reemplazar un grupo funcional con otro grupo funcional, mientras que la adición de radicales implica agregar un nuevo grupo funcional a una molécula.
Relación:
1. "¿Qué es la sustitución de radicales libres?" Química LibreTextsLibretexts, 13 de septiembre de 2020, disponible aquí.
Imagen de cortesía:
1. "FreeRadicalSubstitutionGeneralDescr (1)" por V8rik en Wikipedia en inglés (CC BY-SA 3.0) a través de Commons Wikimedia
2. “Adición de radicales libres de peróxido” por Bryn C - Transferido de en (Dominio público) a través de Commons Wikimedia