Como sabemos, los tampones se utilizan habitualmente en fases móviles de HPLC para mantener el pH estable. Están compuestas por una base o ácido débil, combinada con su ácido o base conjugada. Dado que la retención, la forma del pico, la estabilidad de la columna, la reproducibilidad y la selectividad de los analitos ionizables es muy sensible al pH de la fase móvil, por tanto, es necesario controlar el pH añadiendo un tampón a la fase móvil.
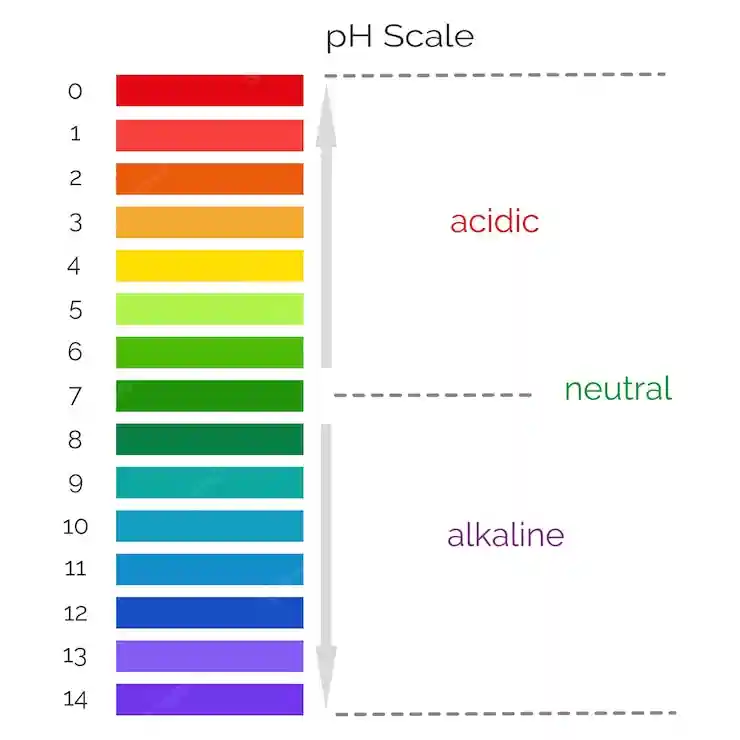
Mantener el pH de la fase móvil es una herramienta importante para conseguir una adecuada separación de los analitos en la cromatografía líquida de alto rendimiento (HPLC), pero si el pH se mantiene mal se producen varios problemas con las separaciones. Cuando un ácido supera las 2 unidades de pH o por debajo de su pKa será superior al 99% ionizado o no ionizado, correspondientemente. Los compuestos básicos están ionizados por debajo de su pKa y no ionizados por encima de su pKa. Los compuestos no ionizados que se forman serán menos polares y, por tanto, se conservarán con mayor fuerza en la cromatografía de fase inversa. En consecuencia, a pH bajo, las moléculas ácidas se retendrán más, mientras que las moléculas básicas se retendrán más a pH más alto. Si el pH de la fase móvil está cercano al valor de pKa, estos pequeños cambios de pH conducen a grandes cambios en el tiempo de retención de los analitos. La resolución, la forma del pico y los parámetros de idoneidad del sistema también cambian cambiando las unidades de pH: éste es el error común en la modificación del pH para muchos análisis.
 ¿Por qué necesitamos una solución tampón en HPLC?
¿Por qué necesitamos una solución tampón en HPLC?