
Las separaciones de fase inversa de compuestos polares e ionizables requieren un control preciso del pH utilizando tampones. Esto asegura tiempos de retención reproducibles y ausencia de retrasos máximos, tiempos de retención y ausencia de retrasos máximos. La amortiguación también evita las interacciones entre los analitos y los silanoles residuales en la fase estacionaria.
Las separaciones de fase inversa se pueden realizar fácilmente en el rango de pH de 2,0 a 7,5. Sin embargo, la reproducibilidad de los resultados se logra si el pH se mantiene dentro de +/- 1 unidad de pH del valor pka del ion tamponador. Como referencia, aquí están los rangos útiles de los puffers de uso común:
| Buffer | caballos de fuerza a los 250C | rango de pH: |
| Fosfato | 2.1 | 1.1-3.1 |
| 7.2 | 6.2 – 8.2 | |
| 12.3 | 11.3 – 13.3 | |
| Acetato | 4.8 | 3.8-5.8 |
| borato | 9.2 | 8.2-10.2 |
| trietilamina | 10.8 | 9.8-11.8 |
Factores que determinan la elección de los tampones
Valores límite UV
Lectura relacionada: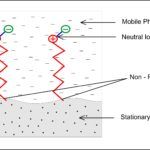 HPLC de cromatografía de par de iones de fase inversa
HPLC de cromatografía de par de iones de fase inversaLa selección del tampón debe basarse en la transparencia en la longitud de onda de detección. El límite UV de los tampones de uso común es de aproximadamente 230 nm a menos de 200 nm.
Compatibilidad de fase móvil
Los tampones deben ser compatibles con la fase móvil. Estos no deben precipitar, ya que la formación de precipitados puede causar daños irreparables a la bomba y la columna de cromatografía.
Lectura relacionada: Avances en Fases Estacionarias de HPLC en Columnas de HPLC Monolíticas
Avances en Fases Estacionarias de HPLC en Columnas de HPLC MonolíticasSelección de tampones para los sistemas LC – MS
La elección de tampones está limitada para aplicaciones LC-MS, ya que el tampón debe tener una alta volatilidad. Los tampones de fosfato no son adecuados para esto. Comúnmente se usan sales de amonio tales como acetato de amonio pH 2.0 - 3.8, formiato de amonio pH 2.7 a 3.7 y carbonato de amonio pH 6.6 a 8.6.
Concentración de tampón
Lectura relacionada: Avances en Fases Estacionarias de HPLC en Columnas HPLC de Circonio
Avances en Fases Estacionarias de HPLC en Columnas HPLC de CirconioEl aumento de la concentración de tampón conduce a una elución más rápida de las moléculas polares. Esto se puede usar para resolver los picos de coelución, pero las concentraciones más altas aumentan la viscosidad, lo que da como resultado una alta contrapresión de la columna.
Las columnas a base de sílice tienden a disolverse incluso por debajo de un pH de 7,0 y la solubilidad se convierte en un problema cuando se mezclan con un disolvente orgánico en altas concentraciones. Las concentraciones por debajo de 0,005 M generalmente hacen que el tampón sea ineficaz. Un rango de concentración de 10 a 50 mM normalmente es suficiente para la mayoría de las aplicaciones. Como regla general, no debe usarse más del 50% en volumen de disolvente orgánico.
Secuencia recomendada para la preparación del tampón
- Disolver el polvo y maquillar hasta la marca.
- El ajuste del pH debe realizarse antes de mezclar con el medio orgánico.
- Filtrar a través de un filtro de 0,45 m para HPLC analítica y de 0,22 µm para las aplicaciones de UHPLC
Precauciones esenciales al usar soluciones tampón
- Los tampones son un buen medio para el crecimiento de microorganismos. Prepare tantas soluciones frescas como sea posible y establezca tiempos de vida útil cortos.
- Después de usar tampones, enjuague el sistema con la misma cantidad de mezcla de agua y solvente orgánico, seguido de agua pura y luego el solvente de almacenamiento. Esto es necesario para evitar que las sales tampón se depositen en los componentes de la bomba y en las columnas si el sistema no se utiliza durante un período de tiempo prolongado.
Ahora que ha comprendido la importancia del control del tampón en las separaciones de fase inversa, deje sus preguntas y comentarios sobre el contenido de este artículo.












