
Diferencia clave: energía de la solución contra energía reticular
La energía de solvatación es el cambio en la energía de Gibbs de un solvente cuando un soluto se disuelve en ese solvente. La energía de red es la cantidad de energía liberada en la formación de una red a partir de iones o la cantidad de energía requerida para romper una red. Que diferencia principal entre la energía de solvatación y la energía de red es que La energía de solvatación da el cambio de entalpía cuando un soluto se disuelve en un solvente, mientras que la energía de red da el cambio de entalpía cuando se forma (o colapsa) una red.
Lectura relacionada: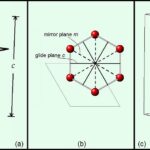 Diferencia entre grupo puntual y grupo espacial
Diferencia entre grupo puntual y grupo espacialCONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la energía de solvatación?
3. ¿Qué es la energía de red?
4. Comparación lado a lado: energía de solvatación frente a energía de red en forma tabular
5. Resumen
¿Qué es la energía de solvatación?
La energía de solvatación es el cambio en la energía de Gibbs cuando un ion o una molécula se transfiere desde el vacío (o la fase gaseosa) a un solvente. La solvatación es la interacción entre un solvente y las moléculas o iones de un soluto. El soluto es el compuesto que se va a disolver en el disolvente. Algunos solutos están formados por moléculas, mientras que otros contienen iones.
La interacción entre las partículas de disolvente y soluto determina muchas de las propiedades de un soluto. Ej: solubilidad, reactividad, color, etc. Durante el proceso de solvatación, las partículas de soluto están rodeadas por moléculas de solvente que forman complejos de solvatación. Cuando el disolvente que interviene en esta solvatación es agua, el proceso se denomina hidratación.
Lectura relacionada: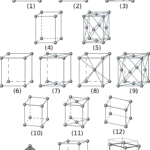 Diferencia entre celda unitaria y celda primitiva.
Diferencia entre celda unitaria y celda primitiva.Durante el proceso de solvatación se forman varios tipos de enlaces químicos e interacciones; Puentes de hidrógeno, interacciones ion-dipolo y fuerzas de van der Waal. Las propiedades complementarias del solvente y el soluto determinan la solubilidad de un soluto en un solvente. Por ejemplo, la polaridad es un factor importante que determina la solubilidad de un soluto en un solvente. Los solutos polares se disuelven bien en disolventes polares. Los solutos no polares se disuelven bien en solventes no polares. Pero la solubilidad de los solutos polares en solventes no polares (y viceversa) es pobre.

Figura 01: Solvatación de un catión de sodio en agua.
Lectura relacionada: Diferencia entre celosía y celda unitaria.
Diferencia entre celosía y celda unitaria.Desde un punto de vista termodinámico, la solvatación (espontánea) solo es posible si la energía libre de Gibbs de la solución final es menor que las energías libres individuales del solvente y el soluto. Por lo tanto, la energía libre de Gibbs debería ser un valor negativo (la energía libre de Gibbs del sistema debería disminuir después de la formación de la solución). La solvatación implica diferentes pasos con diferentes energías.
- Formación de una cavidad de disolvente para dejar espacio a los solutos. Esto es termodinámicamente desfavorable porque a medida que se reducen las interacciones entre las moléculas de disolvente, también se reduce la entropía.
- La separación del soluto de la masa también es termodinámicamente desfavorable. Esto se debe a que se reducen las interacciones entre los solutos.
- Las interacciones entre el solvente y el soluto tienen lugar cuando el soluto ingresa a la cavidad del solvente de una manera termodinámicamente favorable.
La energía de solvatación también se llama entalpía de solvatación. Es útil para explicar la resolución de algunos retículos en solventes mientras que algunos retículos no lo hacen. El cambio en la entalpía de la solución es la diferencia entre las energías de liberar un soluto del volumen y combinar el soluto con el solvente. Si un ion tiene un valor negativo para el cambio de entalpía de la solución, esto indica que es más probable que el ion se disuelva en ese solvente. Un valor positivo alto indica que es menos probable que el ion se disuelva.
¿Qué es la energía reticular?
La energía de red es una medida de la energía contenida en la red cristalina de un compuesto, igual a la energía que se liberaría si se juntaran los iones de los componentes del infinito. La energía reticular de un compuesto también se puede definir como la cantidad de energía requerida para descomponer un sólido iónico en sus átomos en la fase gaseosa.
Los sólidos iónicos son compuestos muy estables debido a las entalpías de formación de las moléculas iónicas junto con la estabilidad debida a la energía reticular de la estructura sólida. Pero la energía de la red no se puede medir experimentalmente. Por lo tanto un Ciclo de Born-Haber se utiliza para determinar la energía de red de los sólidos iónicos. Antes de dibujar un ciclo de Born-Haber, es necesario comprender algunos términos.
- Energía de ionización: la cantidad de energía necesaria para eliminar un electrón de un átomo neutro en forma de gas.
- Afinidad electrónica: la cantidad de energía liberada cuando se agrega un electrón a un átomo neutro en el gas.
- Energía de disociación: la cantidad de energía necesaria para romper un compuesto en átomos o iones.
- Energía de sublimación: la cantidad de energía necesaria para transformar un sólido en su vapor.
- El calor de formación: el cambio de energía cuando se forma un compuesto a partir de sus elementos.
- Ley de Hess: una ley que establece que el cambio total de energía de un proceso dado se puede determinar dividiendo el proceso en diferentes pasos.

Figura 02: El ciclo de Born-Haber para la formación de fluoruro de litio (LiF)
El ciclo de Born-Haber se puede dar mediante la siguiente ecuación.
Calor de formación = calor de atomización + energía de disociación + suma de energías de ionización + suma de afinidades electrónicas + energía de red
Entonces, la energía reticular de un compuesto se puede obtener reorganizando esta ecuación de la siguiente manera.
Energía reticular = Calor de formación - {Calor de atomización + Energía de disociación + Suma de energías de ionización + Suma de afinidades electrónicas}
¿Cuál es la diferencia entre la energía de solvatación y la energía de red?
Energía de solvatación frente a energía de red |
|
| La energía de solvatación es el cambio en la energía de Gibbs cuando un ion o una molécula se transfiere desde el vacío (o la fase gaseosa) a un solvente. | La energía de red es una medida de la energía contenida en la red cristalina de un compuesto, igual a la energía que se liberaría si se juntaran los iones de los componentes del infinito. |
| principio | |
| La energía de solvatación da el cambio de entalpía cuando un soluto se disuelve en un solvente. | La energía de la red proporciona el cambio de entalpía tras la formación (o colapso) de una red. |
Resumen - energía de solvatación contra energía reticular
La energía de solvatación es el cambio de entalpía de un sistema durante la solvatación de un soluto en un solvente. La energía de red es la cantidad de energía liberada durante la formación de una red, o la cantidad de energía requerida para romper una red. La diferencia entre la energía de solvatación y la energía de red es que la energía de solvatación da el cambio de entalpía al disolver un soluto en un solvente, mientras que la energía de red da el cambio de entalpía en la formación (o colapso) de una red.
Relación:
1. "Energía de la red". chem.purdue.edu. Disponible aquí
2. Unión Internacional de Química Pura y Aplicada. “Energía de solución.” Libro de oro de la IUPAC - Energía de solvatación. Disponible aquí
3. "Solución" Wikipedia, Fundación Wikimedia, 5 de marzo de 2018. Disponible aquí
Imagen de cortesía:
1. 'Na+H2O' de Taxman (Dominio público) a través de Commons Wikimedia
2. "Born-Haber Cycle LiF" por Jkwchui - Trabajo propio, (CC BY-SA 3.0) a través de Commons Wikimedia











