Diferencia clave: ácido acético frente a acetato
La principal diferencia entre el ácido acético y el acetato es esta. El ácido acético es un compuesto neutro, mientras que el acetato es un anión con una carga eléctrica neta negativa..
El ácido acético es un compuesto orgánico que ayuda en la producción de vinagre, mientras que el ion acetato es la base conjugada del ácido acético. Lo más importante es que la formación del ion acetato se produce mediante la eliminación de el átomo de hidrógeno en el grupo carboxilo del ácido acético.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el ácido acético?
3. ¿Qué es el acetato?
4. Comparación lado a lado: ácido acético frente a acetato en forma tabular
5. Resumen
 Diferencia entre litio y otros metales alcalinos
Diferencia entre litio y otros metales alcalinos¿Qué es el ácido acético?
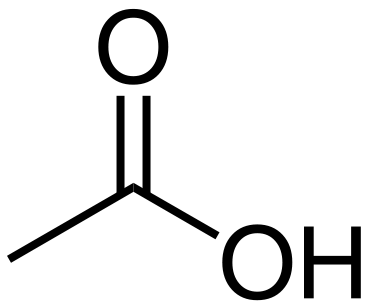
El ácido acético es un compuesto orgánico con la fórmula química CH3COH. La masa molar de este compuesto es 60 g/mol mientras que el nombre IUPAC de este compuesto es ácido acético. Además, a temperatura ambiente, el ácido acético es un líquido incoloro con sabor agrio. AEl ácido acético se clasifica como ácido carboxílico debido a la presencia de un grupo de ácido carboxílico (-COOH).

Figura 1: Molécula de ácido acético
Lectura relacionada: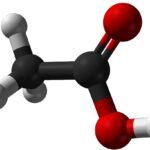 Diferencia entre ácido fórmico y ácido acético.
Diferencia entre ácido fórmico y ácido acético.El ácido acético glacial es la forma concentrada de ácido acético. Además, el ácido acético tiene un olor acre similar al olor del vinagre, así como un sabor agrio característico. También es un ácido débil ya que se disocia parcialmente en solución acuosa, liberando anión acetato y un protón. El ácido acético tiene un protón disociable por molécula. Sin embargo, el ácido glacial es un irritante altamente corrosivo.
El ácido acético es un ácido carboxílico simple; De hecho, es el segundo ácido carboxílico más simple. En el estado sólido del ácido acético, las moléculas forman cadenas moleculares a través de enlaces de hidrógeno. Sin embargo, en la fase de vapor del ácido acético, forma dímeros (dos moléculas unidas por puentes de hidrógeno). Debido a que el ácido acético líquido es un solvente prótico polar, es miscible con muchos solventes polares y no polares.
¿Qué es el acetato?
El acetato es un anión formado por la eliminación de un átomo de hidrógeno del ácido acético. Este anión tiene una carga negativa neta (la carga es -1 como resultado de la liberación de un protón). ion acetato no puede persistir como un solo compuesto debido a su carga altamente reactiva. Por lo tanto, existe principalmente como una sal de un metal alcalino. El ion acetato es la base conjugada del ácido acético, que en consecuencia se forma a partir de la disociación del ácido acético.
Lectura relacionada: Diferencia entre óxidos metálicos y no metálicos.
Diferencia entre óxidos metálicos y no metálicos.
Figura 2: anión acetato
La fórmula química de este anión es C2H3O2− tiempo su nombre IUPAC es etanoato. Además, la masa molar del acetato es de 59 g/mol. En particular, a valores de pH superiores a 5,5, el ácido acético está presente como anión acetato, que libera espontáneamente un protón. Esto se debe a que los iones de acetato son más estables que el ácido acético a un pH elevado.
¿Cuál es la diferencia entre el ácido acético y el acetato?
ácido acético vs acetato |
|
| El ácido acético es un compuesto orgánico con la fórmula química CH3COH. | El acetato es un anión formado por la eliminación de un átomo de hidrógeno del ácido acético. |
| masa molar | |
| La masa molar del ácido acético es de 60 g/mol. | Pero la masa molar del acetato es de 59 g/mol. |
| Carga eléctrica | |
| El ácido acético no tiene carga neta. | El acetato tiene carga negativa. |
| categoría | |
| El ácido acético es una molécula orgánica. | El acetato es un anión orgánico. |
| valor de pH | |
| Las moléculas de ácido acético son estables a pH bajo (alrededor de pH 5). | Los iones de acetato son estables a valores de pH elevados (superiores a pH 5,5). |
Resumen: ácido acético frente a acetato
El ácido acético es el segundo ácido carboxílico más simple. El acetato, por otro lado, es un anión derivado del ácido acético. La diferencia clave entre el ácido acético y el acetato es que el ácido acético es un compuesto neutro, mientras que el acetato es un anión con una carga eléctrica neta negativa.
Relación:
1. "Ácido acético". Wikipedia, 18 de abril de 2018, disponible aquí.
2. "Ácido acético". Centro Nacional de Información Biotecnológica. Base de datos compuesta de PubChem, Biblioteca Nacional de Medicina de EE. UU., disponible aquí.
3. "Acetato". Wikipedia, 10 de abril de 2018, disponible aquí.
Imagen de cortesía:
1. "Esqueleto 2D de ácido acético" (Dominio público) a través de Commons Wikimedia
2. "Acetato-anión-canónico-forma-2D-esquelético" (Dominio público) a través de Commons Wikimedia