La principal diferencia entre el etanol y el dimetil éter es que el A temperatura ambiente, el etanol es un líquido incoloro con alta volatilidad, mientras que el éter dimetílico es un gas incoloro a temperatura ambiente. Además, el etanol (el nombre común es alcohol etílico) es un alcohol, mientras que el éter dimetílico es un éter.
Un alcohol es un compuesto orgánico compuesto por un grupo hidroxilo (-OH) como grupo funcional. Un éter también es un compuesto orgánico pero tiene dos grupos alquilo unidos al mismo átomo de oxígeno.

 Diferencia entre SiO2 y CO2
Diferencia entre SiO2 y CO2CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es el etanol?
3. ¿Qué es el éter dimetílico?
4. Similitudes entre el etanol y el dimetil éter
5. Comparación lado a lado: etanol frente a dimetil éter en forma tabular
6. Resumen
¿Qué es el etanol?
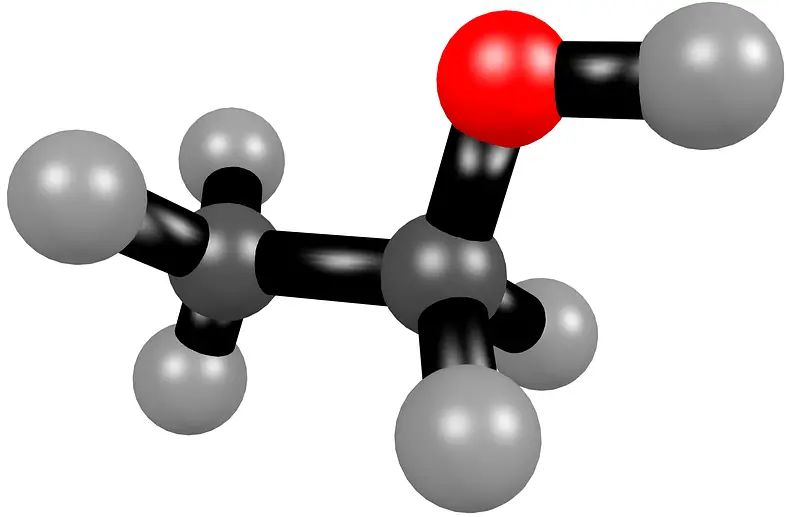
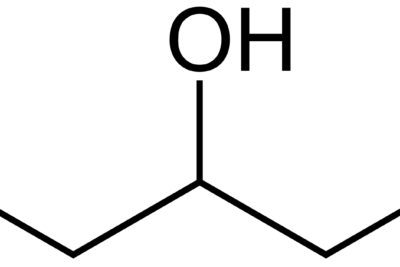
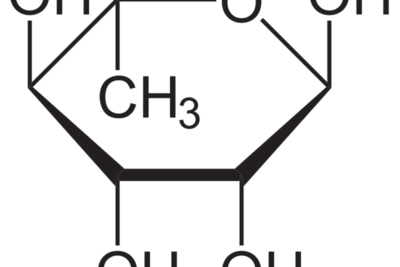
El etanol es un alcohol con la fórmula química C2H5OH. El nombre común de este compuesto es alcohol etílico. El grupo funcional de este compuesto es un grupo hidroxilo (-OH). El etanol es altamente inflamable; por lo tanto, también se utiliza como combustible. Además, es un compuesto muy volátil. Sin embargo, a temperatura ambiente es un líquido incoloro con un olor característico.

 Diferencia entre destilación y condensación.
Diferencia entre destilación y condensación.Figura 1: Estructura química del etanol
Algunos datos químicos sobre el etanol
- Fórmula química = C2H6O
- masa molar = 0,7 g/mol
- Punto de fusión = -114,1°C
- Punto de ebullición = 78,37°C
- Estado físico = a temperatura ambiente es un líquido incoloro
- Olor = olor alcohólico característico
- Solubilidad en agua = miscible con agua
El etanol es miscible con agua porque puede formar enlaces de hidrógeno con moléculas de agua (los grupos -OH pueden formar enlaces de hidrógeno con H2moléculas de O). Por lo tanto, las soluciones utilizadas tienen una alta viscosidad. Además, la volatilidad disminuye cuando el etanol se mezcla con agua.
El etanol es un compuesto polar porque tiene un grupo hidroxilo terminal. Hace que el etanol sea un buen solvente para los compuestos polares. Hay dos formas de producir etanol: procesos químicos y procesos biológicos. El proceso químico más común es la hidratación del etileno. La ruta biológica más común es la fermentación de azúcares por microorganismos.
Lectura relacionada: Diferencia entre etano eteno y etino.
Diferencia entre etano eteno y etino.Los usos del etanol incluyen usos industriales, usos médicos, como combustible, como solvente, etc. El etanol también tiene otro uso como antiséptico, ya que puede matar algunos microorganismos. Además, el etanol es un antídoto para el metanol. El etanol se puede utilizar directamente como combustible o como aditivo de combustible.
¿Qué es el éter dimetílico?
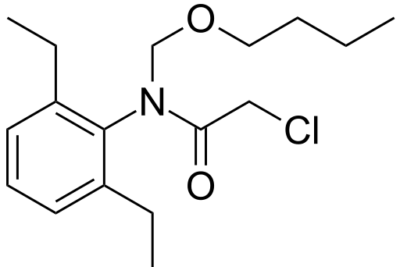
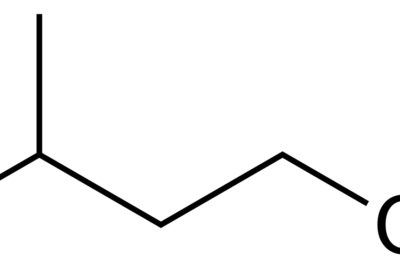
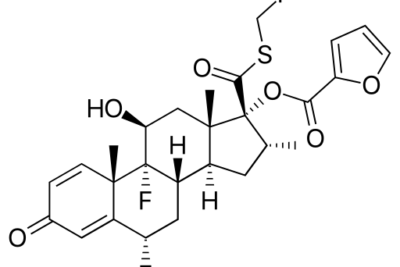
dimetil éter es un compuesto de éter con la fórmula química C2H6O. El nombre IUPAC de este compuesto es metoximetano. Este compuesto es conocido por sus propiedades disolventes. Tiene dos grupos metilo unidos a través de un átomo de oxígeno; los dos grupos metilo están unidos al mismo átomo de oxígeno.

Figura 2: estructura esquelética de dimetil éter
Algunos datos químicos sobre el éter dimetílico
- Fórmula química = C2H6O
- masa molar = 46,07 g/mol
- Punto de fusión = -141°C
- Punto de ebullición = -24°C
- Estado físico = a temperatura ambiente es un gas incoloro
- Olor = olor etéreo
- Solubilidad en agua = no soluble en agua
el éter dimetílico es un compuesto no polar. Esto significa que el dimetil éter no tiene polaridad. Esto se debe a su estructura molecular simétrica. Por lo tanto, es un buen disolvente para compuestos no polares. Sin embargo, no es químicamente reactivo en comparación con otros compuestos orgánicos.
¿Cuáles son las similitudes entre el etanol y el dimetil éter?
- El etanol y el éter dimetílico son compuestos orgánicos.
- Tanto el etanol como el éter dimetílico tienen la misma masa molar.
- Ambos son buenos disolventes.
- El etanol y el éter dimetílico consisten en átomos de C, H y O.
¿Cuál es la diferencia entre el etanol y el dimetil éter?
etanol versus éter dimetílico |
|
| El etanol es un alcohol con la fórmula química C2H5OH. | El dimetil éter es un compuesto de éter con la fórmula química C2H6o |
| categoría | |
| El etanol es un alcohol. | el éter dimetílico es un éter. |
| punto de fusion | |
| El punto de fusión del etanol es -114,1 °C. | El punto de fusión del éter dimetílico es -141 °C. |
| punto de ebullición | |
| El punto de ebullición del etanol es 78,37 °C. | El punto de ebullición del éter dimetílico es -24°C |
| estado físico | |
| A temperatura ambiente, el etanol es un líquido incoloro con alta volatilidad. | El dimetil éter es un gas incoloro a temperatura ambiente. |
| Olor | |
| El etanol tiene un olor alcohólico característico. | El dimetil éter tiene un olor etéreo típico. |
| presencia de un grupo hidroxilo | |
| El etanol tiene un grupo hidroxilo (-OH). | el éter dimetílico no tiene grupos hidroxilo. |
Resumen: etanol frente a dimetil éter
El etanol y el éter dimetílico son compuestos orgánicos con la misma masa molar pero estructuras químicas diferentes. La diferencia clave entre el etanol y el dimetiléter es que el etanol es un líquido incoloro a temperatura ambiente, mientras que el dimetiléter es un gas incoloro a temperatura ambiente.
Relación:
1. "Etanol" Wikipedia, Fundación Wikimedia, 18 de abril de 2018, disponible aquí.
2. "Éter". Centro Nacional de Información Biotecnológica. Base de datos compuesta de PubChem, Biblioteca Nacional de Medicina de EE. UU., disponible aquí.
3. "éter dietílico". Éter dietílico - Enciclopedia del Nuevo Mundo, disponible aquí.
Imagen de cortesía:
1. "1094992" (CC0) a través de Pixabay
2. "Fórmulas estructurales de dimetiléter" por Jü - Trabajo propio (Dominio público) a través de Commons Wikimedia