Hay cuatro niveles de estructura encontrados en polipéptidos y proteínas. La estructura primaria de una proteína polipeptídica determina sus estructuras secundaria, terciaria y cuaternaria.
Estructura Primaria
La estructura primaria de polipéptidos y proteínas es la secuencia de aminoácidos en la cadena polipeptídica con referencia a las ubicaciones de cualquier enlace disulfuro. La estructura primaria puede considerarse como una descripción completa de todos los enlaces covalentes en una cadena polipeptídica o proteína.
Lectura relacionada: Ideas para Proyectos de Ciencias Químicas de Plantas y Suelos
Ideas para Proyectos de Ciencias Químicas de Plantas y Suelos
La forma más común de denotar una estructura primaria es escribir la secuencia de aminoácidos usando las abreviaturas estándar de tres letras para los aminoácidos. Por ejemplo, gly-gly-ser-ala es la estructura primaria para un polipéptido compuesto de glicina, glicina, serina y alanina, en ese orden, desde el aminoácido N-terminal (glicina) hasta el aminoácido C-terminal (alanina).
Estructura Secundaria
La estructura secundaria es la disposición o conformación ordenada de aminoácidos en regiones localizadas de un polipéptido o molécula de proteína. Los enlaces de hidrógeno juegan un papel importante en la estabilización de estos patrones de plegado. Las dos estructuras secundarias principales son la hélice alfa y la lámina plisada beta antiparalela. Existen otras conformaciones periódicas, pero la hélice α y la lámina plisada β son las más estables. Un único polipéptido o proteína puede contener múltiples estructuras secundarias.
Lectura relacionada: pH, pKa y la ecuación de Henderson-Hasselbalch
pH, pKa y la ecuación de Henderson-Hasselbalch
Una hélice α es una espiral hacia la derecha o en el sentido de las agujas del reloj en la que cada enlace peptídico está en el trans conformación y es plano. El grupo amina de cada enlace peptídico discurre generalmente hacia arriba y paralelo al eje de la hélice; el grupo carbonilo apunta generalmente hacia abajo.
La lámina plisada β consiste en cadenas polipeptídicas extendidas con cadenas vecinas que se extienden antiparalelas entre sí. Al igual que con la hélice α, cada enlace peptídico es trans y plano. Los grupos amina y carbonilo de los enlaces peptídicos apuntan uno hacia el otro y en el mismo plano, por lo que pueden producirse enlaces de hidrógeno entre cadenas polipeptídicas adyacentes.
La hélice se estabiliza mediante enlaces de hidrógeno entre grupos amina y carbonilo de la misma cadena polipeptídica. La lámina plisada se estabiliza mediante enlaces de hidrógeno entre los grupos amina de una cadena y los grupos carbonilo de una cadena adyacente.
Lectura relacionada: Bioquímica Enzimática: Qué Son y Cómo Funcionan
Bioquímica Enzimática: Qué Son y Cómo Funcionan
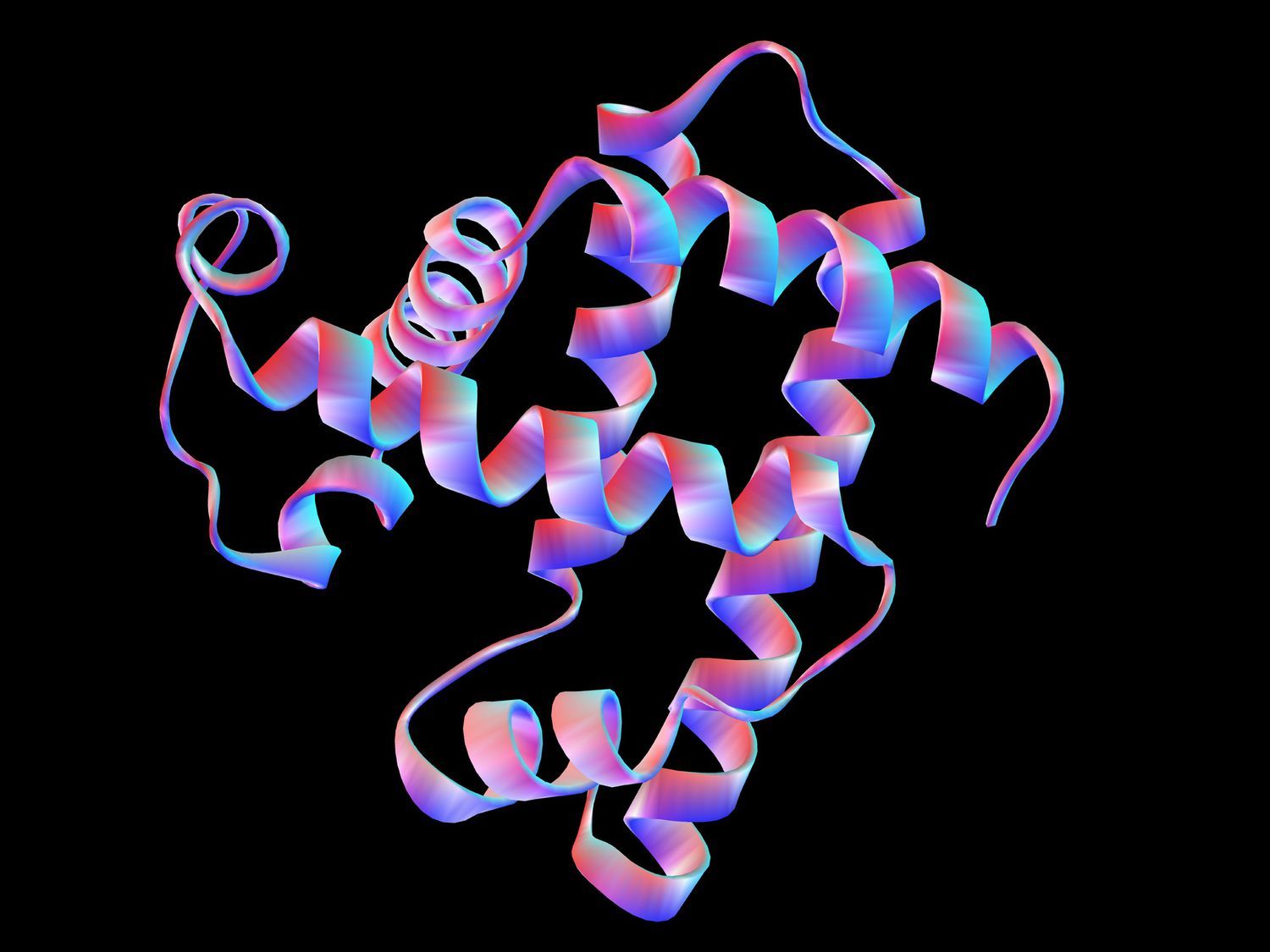
Estructura Terciaria
La estructura terciaria de un polipéptido o proteína es la disposición tridimensional de los átomos dentro de una única cadena polipeptídica. Para un polipéptido que consiste en un único patrón de plegamiento conformacional (por ejemplo, solo una hélice alfa), la estructura secundaria y terciaria puede ser una y la misma. Además, para una proteína compuesta de una única molécula polipeptídica, la estructura terciaria es el nivel más alto de estructura que se alcanza.
La estructura terciaria se mantiene en gran medida mediante enlaces disulfuro. Los enlaces disulfuro se forman entre las cadenas laterales de la cisteína por oxidación de dos grupos tiol (SH) para formar un enlace disulfuro (S-S), también llamado a veces puente disulfuro.
Estructura Cuaternaria
La estructura cuaternaria se usa para describir proteínas compuestas de múltiples subunidades (múltiples moléculas polipeptídicas, cada una llamada "monómero"). La mayoría de las proteínas con un peso molecular superior a 50.000 consisten en dos o más monómeros unidos de forma no covalente. La disposición de los monómeros en la proteína tridimensional es la estructura cuaternaria. El ejemplo más común usado para ilustrar la estructura cuaternaria es la proteína hemoglobina. La estructura cuaternaria de la hemoglobina es el paquete de sus subunidades monoméricas. La hemoglobina se compone de cuatro monómeros. Hay dos cadenas α, cada una con 141 aminoácidos, y dos cadenas β, cada una con 146 aminoácidos. Debido a que hay dos subunidades diferentes, la hemoglobina exhibe una estructura heterocuaternaria. Si todos los monómeros de una proteína son idénticos, existe una estructura homocuaternaria.
La interacción hidrófoba es la principal fuerza estabilizadora para las subunidades en la estructura cuaternaria. Cuando un monómero individual se pliega en una forma tridimensional para exponer sus cadenas laterales polares a un entorno acuoso y para proteger sus cadenas laterales no polares, todavía hay algunas secciones hidrófobas en la superficie expuesta. Dos o más monómeros se ensamblarán de modo que sus secciones hidrófobas expuestas estén en contacto.
Más Información
¿Quieres más información sobre aminoácidos y proteínas? Aquí hay algunos recursos adicionales en línea sobre aminoácidos y quiralidad de aminoácidos. Además de los textos de química general, se puede encontrar información sobre la estructura de las proteínas en textos de bioquímica, química orgánica, biología general, genética y biología molecular. Los textos de biología suelen incluir información sobre los procesos de transcripción y traducción, a través de los cuales se utiliza el código genético de un organismo para producir proteínas.