Las proteínas son polímeros biológicos construidos a partir de aminoácidos unidos entre sí para formar péptidos. Estas subunidades peptídicas pueden unirse con otros péptidos para formar estructuras más complejas. Múltiples tipos de enlaces químicos mantienen unidas a las proteínas y las unen a otras moléculas. Eche un vistazo más de cerca a los enlaces químicos responsables de la estructura de las proteínas.
Enlaces Peptídicos
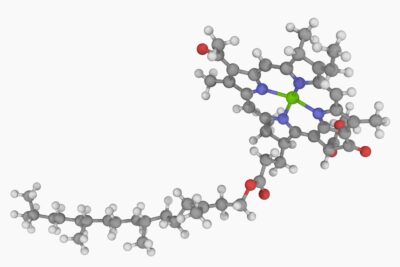
La estructura primaria de una proteína consiste en aminoácidos encadenados entre sí. Los aminoácidos están unidos por enlaces peptídicos. Un enlace peptídico es un tipo de enlace covalente entre el grupo carboxilo de un aminoácido y el grupo amino de otro aminoácido. Los aminoácidos en sí mismos están hechos de átomos unidos por enlaces covalentes.
Lectura relacionada: Experimento Científico de Hueso de Pollo de Goma
Experimento Científico de Hueso de Pollo de Goma
Enlaces de Hidrógeno
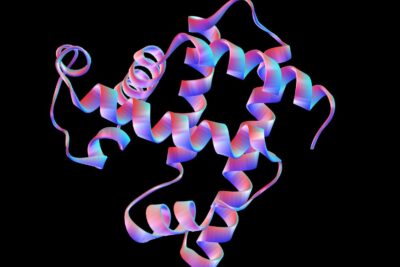
La estructura secundaria describe el plegamiento o enrollamiento tridimensional de una cadena de aminoácidos (por ejemplo, lámina plegada en beta, hélice alfa). Esta forma tridimensional se mantiene en su lugar mediante enlaces de hidrógeno. Un enlace de hidrógeno es una interacción dipolo-dipolo entre un átomo de hidrógeno y un átomo electronegativo, tal como nitrógeno u oxígeno. Una única cadena polipeptídica puede contener múltiples regiones de lámina plegada alfa-hélice y beta.
Cada hélice alfa se estabiliza mediante enlaces de hidrógeno entre los grupos amina y carbonilo en la misma cadena polipeptídica. La lámina plegada en beta se estabiliza mediante enlaces de hidrógeno entre los grupos amina de una cadena polipeptídica y los grupos carbonilo de una segunda cadena adyacente.
Lectura relacionada: Cómo Calcular la Normalidad de una Solución
Cómo Calcular la Normalidad de una Solución
Enlaces de Hidrógeno, Enlaces Iónicos, Puentes Disulfuro
Mientras que la estructura secundaria describe la forma de las cadenas de aminoácidos en el espacio, la estructura terciaria es la forma general asumida por la molécula completa, que puede contener regiones de láminas y bobinas. Si una proteína consiste en una cadena polipeptídica, una estructura terciaria es el nivel más alto de estructura. Los enlaces de hidrógeno afectan la estructura terciaria de una proteína. Además, el grupo R de cada aminoácido puede ser hidrófobo o hidrófilo.
Lectura relacionada:
 Aprende a Calcular la Molaridad de una Solución
Aprende a Calcular la Molaridad de una SoluciónInteracciones Hidrófobas e Hidrófilas
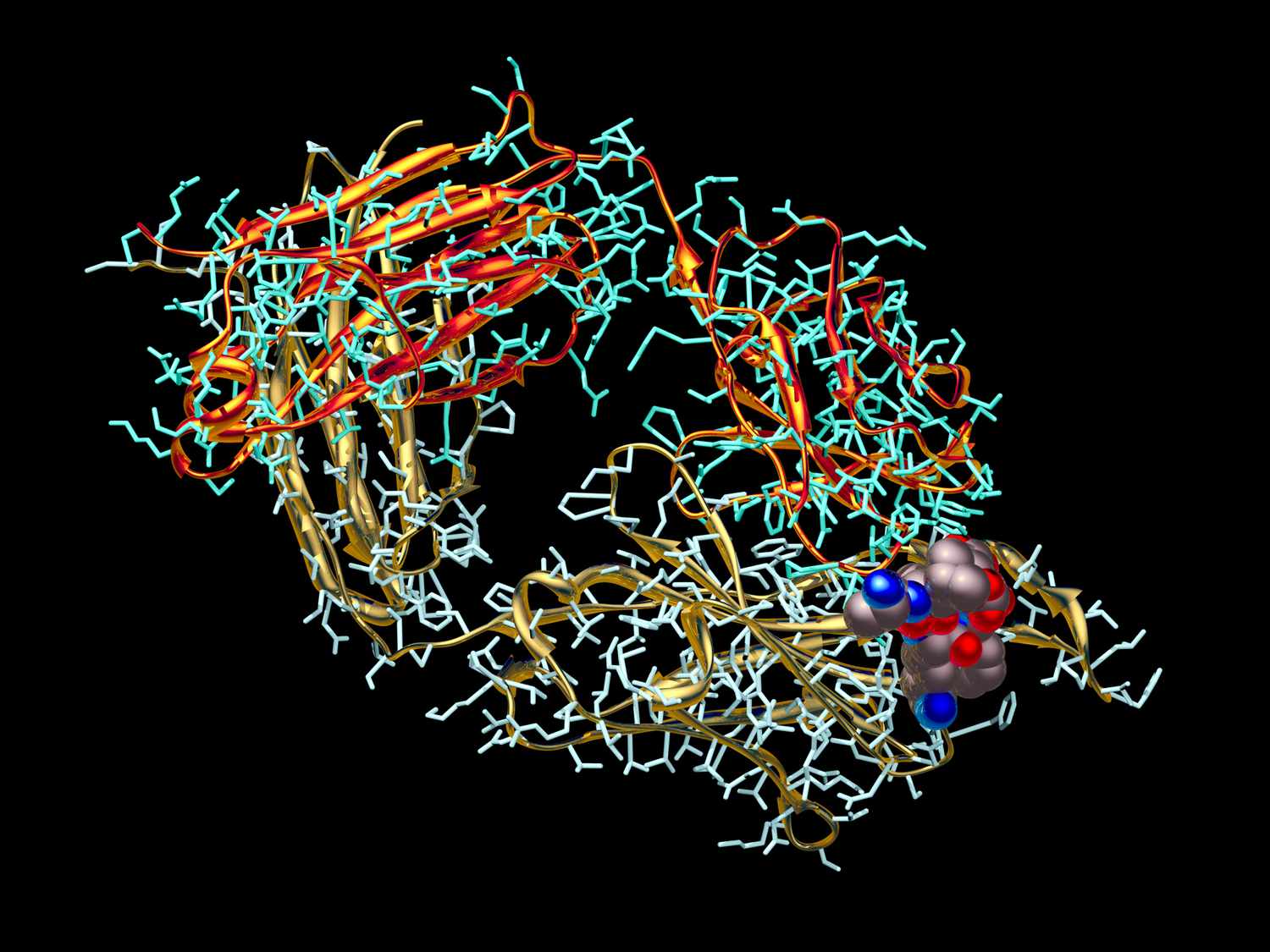
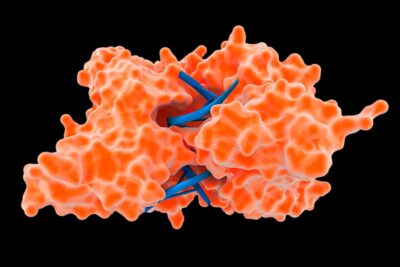
Algunas proteínas están hechas de subunidades en las que las moléculas de proteínas se unen para formar una unidad más grande. Un ejemplo de una proteína de este tipo es la hemoglobina. La estructura cuaternaria describe cómo encajan las subunidades para formar la molécula más grande.