La prueba de llama se usa para determinar visualmente la identidad de un ion metálico o metaloide desconocido en función del color característico que la sal convierte en la llama de un quemador Bunsen. El calor de la llama excita los electrones de los iones metálicos, haciendo que emitan luz visible. Cada elemento tiene un espectro de emisión característico que se puede usar para diferenciar entre un elemento y otro.
Conclusiones clave: Realice la Prueba de Llama
- La prueba de llama es una prueba cualitativa en química analítica que se utiliza para ayudar a identificar la composición de una muestra.
- La premisa es que el calor da energía a los elementos e iones, haciendo que emitan luz en un color característico o espectro de emisión.
- La prueba de llama es una forma rápida de reducir la identidad de una muestra, pero debe combinarse con otras pruebas para confirmar la composición.
Cómo Hacer la Prueba de Llama
Método Clásico de Bucle de Alambre
Primero, necesitas un lazo de alambre limpio. Los bucles de platino o níquel-cromo son los más comunes. Se pueden limpiar sumergiéndolos en ácido clorhídrico o nítrico, seguido de enjuague con agua destilada o desionizada. Pruebe la limpieza del bucle insertándolo en una llama de gas. Si se produce una explosión de color, el bucle no está suficientemente limpio. El bucle debe limpiarse entre pruebas.
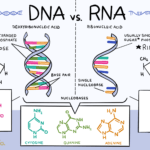 Diferencias entre ADN y ARN
Diferencias entre ADN y ARN
El bucle limpio se sumerge en un polvo o en una solución de una sal iónica (metálica). El bucle con la muestra se coloca en la parte transparente o azul de la llama y se observa el color resultante.
Método de Férula de Madera o Hisopo de Algodón
Las férulas de madera o los hisopos de algodón ofrecen una alternativa económica a los bucles de alambre. Para usar férulas de madera, remójelas durante la noche en agua destilada. Vierta el agua y enjuague las férulas con agua limpia, teniendo cuidado de no contaminar el agua con sodio (como el sudor en las manos). Tome una férula húmeda o un hisopo de algodón humedecido en agua, sumérjalo en la muestra que se va a analizar y agite la férula o el hisopo a través de la llama. No sostenga la muestra en la llama, ya que esto provocaría que la férula o el hisopo se incendien. Use una férula o hisopo nuevo para cada prueba.
Lectura relacionada:
 Cómo Realizar una Recristalización
Cómo Realizar una RecristalizaciónCómo Interpretar los Resultados de la Prueba de Llama
La muestra se identifica comparando el color de llama observado con valores conocidos de una tabla o gráfico.
Rojo
Carmín a Magenta: Compuestos de litio. Enmascarado por bario o sodio.
Escarlata o carmesí: Compuestos de estroncio. Enmascarado por bario.
Rojo: Rubidio (llama sin filtrar)
Amarillo-Rojo: Compuestos de calcio. Enmascarado por bario.
Amarillo
Oro: Hierro
Amarillo intenso: Compuestos de sodio, incluso en pequeñas cantidades. Una llama amarilla no es indicativa de sodio a menos que persista y no se intensifique mediante la adición de NaCl al 1% al compuesto seco.
 Visión general de las Ramas de la Química
Visión general de las Ramas de la Química
Blanco
Blanco brillante: Magnesio
Blanco-Verde: Zinc
Verde
Esmeralda: Compuestos de cobre, distintos de los haluros. Talio.
Verde brillante: Boro
Azul verdoso: Fosfatos, cuando se humedecen con H2ENTONCES4 o B2O3.
Verde tenue: Antimonio y NH4 compuestos.
Amarillo verdoso: Bario, manganeso (II), molibdeno.
Azul
Azul: Plomo, selenio, bismuto, cesio, cobre (I), CuCl2 y otros compuestos de cobre humedecidos con ácido clorhídrico, indio, plomo.
Azul claro: arsénico y algunos de sus compuestos.
Azul verdoso: CuBr2, antimonio
Púrpura
Violeta: Compuestos de potasio distintos de boratos, fosfatos y silicatos. Enmascarado por sodio o litio.
Lila a Rojo Púrpura: Potasio, rubidio y/o cesio en presencia de sodio cuando se observa a través de un vidrio azul.
Limitaciones de la Prueba de Llama
- La prueba no puede detectar concentraciones bajas de la mayoría de los iones.
- El brillo de la señal varía de una muestra a otra. Por ejemplo, la emisión amarilla del sodio es mucho más brillante que la emisión roja de la misma cantidad de litio.
- Las impurezas o contaminantes afectan los resultados de la prueba. El sodio, en particular, está presente en la mayoría de los compuestos y coloreará la llama. A veces, se usa un vaso azul para filtrar el amarillo del sodio.
- La prueba no puede diferenciar entre todos los elementos. Varios metales producen el mismo color de llama. Algunos compuestos no cambian el color de la llama en absoluto.
Debido a la limitación, la prueba de llama podría usarse para descartar la identidad de un elemento en una muestra, en lugar de identificarlo definitivamente. Además de esta prueba, se deben realizar otros procedimientos analíticos.
Colores de Prueba de Llama
Esta tabla enumera los colores esperados para los elementos en la prueba de llama. Obviamente, los nombres de los colores son subjetivos, por lo que la mejor manera de aprender a reconocer elementos de colores cercanos es probar soluciones conocidas para saber qué esperar.
| Símbolo | Elemento | Color |
| Como | Arsénico | Azul |
| B | Boro | Verde brillante |
| Ba | Bario | Verde Pálido / Amarillento |
| Ca | Calcio | Naranja a rojo |
| Cs | Cesio | Azul |
| Cu (I | Cobre (I) | Azul |
| Cu (II) | Cobre(II) sin haluros | Verde |
| Cu (II) | Haluro de cobre(II) | Azul verdoso |
| Fe | Hierro | Oro |
| En | Indio | Azul |
| K | Potasio | Lila a rojo |
| Li | Litio | De magenta a carmín |
| Mg | Magnesio | Blanco brillante |
| Mn (II) | Manganeso (II) | Verde amarillento |
| Mo | Molibdeno | Verde amarillento |
| Na | Sodio | Amarillo intenso |
| P | Fósforo | Verde azulado pálido |
| Pb | Plomo | Azul |
| Rb | Rubidio | Rojo a rojo púrpura |
| Sb | Antimonio | Verde pálido |
| Se | Selenio | Azul celeste |
| Sr | Estroncio | Carmesí |
| Te | Telurio | Verde pálido |
| Tl | Talio | Verde puro |
| Zn | Cinc | Verde azulado a verde blanquecino |
Fuente
- Manual de Química de Lange, 8a edición, Handbook Publishers Inc., 1952.