Un elemento químico, o un elemento, se define como un material que no se puede descomponer o transformar en otra sustancia utilizando medios químicos. Los elementos pueden considerarse como los componentes químicos básicos de la materia. Hay 118 elementos conocidos. Cada elemento se identifica de acuerdo con el número de protones que tiene en su núcleo atómico. Se puede crear un nuevo elemento añadiendo más protones a un átomo. Los átomos del mismo elemento tienen el mismo número atómico o Z.
Conclusiones Clave: Elemento Químico
- Un elemento químico es una sustancia que consta de un solo tipo de átomo. En otras palabras, todos los átomos de un elemento contienen el mismo número de protones.
- La identidad de un elemento químico no se puede cambiar por ninguna reacción química. Sin embargo, una reacción nuclear puede transmutar un elemento en otro.
- Los elementos se consideran los bloques de construcción de la materia. Esto es cierto, pero vale la pena señalar que los átomos de un elemento consisten en partículas subatómicas.
- Hay 118 elementos conocidos. Todavía se pueden sintetizar nuevos elementos.
Nombres y Símbolos de Elementos
Cada elemento puede representarse por su número atómico o por su nombre o símbolo de elemento. El símbolo del elemento es una abreviatura de una o dos letras. La primera letra de un símbolo de elemento siempre está en mayúscula. Una segunda letra, si existe, se escribe en minúsculas. La Unión Internacional de Química Pura y Aplicada (IUPAC) ha acordado un conjunto de nombres y símbolos para los elementos, que se utilizan en la literatura científica. Sin embargo, los nombres y símbolos de los elementos pueden ser diferentes en el uso común en varios países. Por ejemplo, el elemento 56 se denomina bario con el símbolo de elemento Ba por la IUPAC y en inglés. Se llama bario en italiano y bario en francés. El elemento de número atómico 4 es boro para la IUPAC, pero boro en italiano, portugués y español, Bor en alemán y bore en francés. Los símbolos de elementos comunes son utilizados por países con alfabetos similares.
Lectura relacionada: ¿Por Qué Crees Que La Química Es Tan Difícil?
¿Por Qué Crees Que La Química Es Tan Difícil?
Abundancia de Elementos
De los 118 elementos conocidos, se sabe que 94 ocurren naturalmente en la Tierra. Los otros se llaman elementos sintéticos. El número de neutrones en un elemento determina su isótopo. 80 elementos tienen al menos un isótopo estable. Treinta y ocho consisten únicamente en isótopos radiactivos que se descomponen con el tiempo en otros elementos, que pueden ser radiactivos o estables.
En la Tierra, el elemento más abundante en la corteza es el oxígeno, mientras que se cree que el elemento más abundante en todo el planeta es el hierro. En contraste, el elemento más abundante en el universo es el hidrógeno, seguido del helio.
Lectura relacionada: Lista de Elementos Radiactivos
Lista de Elementos Radiactivos
Síntesis de Elementos
Los átomos de un elemento pueden producirse por los procesos de fusión, fisión y desintegración radiactiva. Todos estos son procesos nucleares, lo que significa que involucran a los protones y neutrones en el núcleo de un átomo. Por el contrario, los procesos químicos (reacciones) involucran electrones y no núcleos. En la fusión, dos núcleos atómicos se fusionan para formar un elemento más pesado. En la fisión, los núcleos atómicos pesados se dividen para formar uno o más núcleos más ligeros. La desintegración radiactiva puede producir diferentes isótopos del mismo elemento o de un elemento más ligero.
Cuando se usa el término "elemento químico", puede referirse a un solo átomo de ese átomo o a cualquier sustancia pura que consista solo en ese tipo de hierro. Por ejemplo, un átomo de hierro y una barra de hierro son ambos elementos del elemento químico.
Lectura relacionada: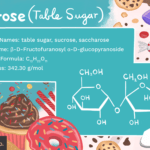 ¿Cuál Es la Fórmula Química del Azúcar?
¿Cuál Es la Fórmula Química del Azúcar?
Ejemplos de Elementos
Los elementos se encuentran en la tabla periódica. La materia que consiste en un solo elemento contiene átomos que tienen el mismo número de protones. El número de neutrones y electrones no afecta la identidad de un elemento, por lo que si tuviera una muestra que contuviera protio, deuterio y tritio (los tres isótopos del hidrógeno), seguiría siendo un elemento puro.
- Hidrógeno
- Oro
- Azufre
- Oxígeno
- Uranio
- Hierro
- Argón
- Americio
- Tritio (un isótopo del hidrógeno)
Ejemplos de Sustancias Que No Son Elementos
Las sustancias que no son elementos consisten en átomos con diferentes números de protones. Por ejemplo, el agua contiene átomos de hidrógeno y oxígeno.
- Latón
- Agua
- Aire
- Plástico
- Fuego
- Arena
- Coche
- Ventana
- Acero
¿Qué Hace Que Los Elementos Sean Diferentes Entre Sí?
¿Cómo se puede saber si dos sustancias químicas son el mismo elemento? A veces, los ejemplos de un elemento puro se ven muy diferentes entre sí. Por ejemplo, el diamante y el grafito (mina de lápiz) son ejemplos del elemento carbono. No lo sabrías por apariencia o propiedades. Sin embargo, los átomos de diamante y grafito comparten el mismo número de protones. El número de protones, partículas en el núcleo de un átomo, determina el elemento. Los elementos de la tabla periódica están ordenados en orden creciente de protones. El número de protones también se conoce como número atómico de un elemento, que se indica con el número Z.
La razón por la que las diferentes formas de un elemento (llamadas alótropos) pueden tener diferentes propiedades a pesar de que tienen el mismo número de protones es que los átomos están dispuestos o apilados de manera diferente. Piénsalo en términos de un conjunto de bloques. Si apilas los mismos bloques de diferentes maneras, obtienes diferentes objetos.
Fuentes
- E. M. Burbidge; G. R. Burbidge; W. A. Fowler; F. Hoyle (1957). "Síntesis de los Elementos en las Estrellas". Reseñas de Modern Physics. 29 (4): 547–650. doi:10.1103/RevModPhys.29.547
- Earnshaw, A.; Greenwood, N. (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann.