La destilación es un proceso de separación importante en química, industria y ciencia de los alimentos. Aquí está la definición de destilación y una mirada a los tipos de destilación y sus usos.
Conclusiones clave: Destilación
- La destilación es el proceso de separar los componentes de una mezcla en función de diferentes puntos de ebullición.
- Ejemplos de usos de destilación incluyen purificación de alcohol, desalinización, refinación de petróleo crudo y fabricación de gases licuados a partir del aire.
- Los seres humanos han estado utilizando la destilación desde al menos 3000 AC en el valle del Indo.
Definición de Destilación
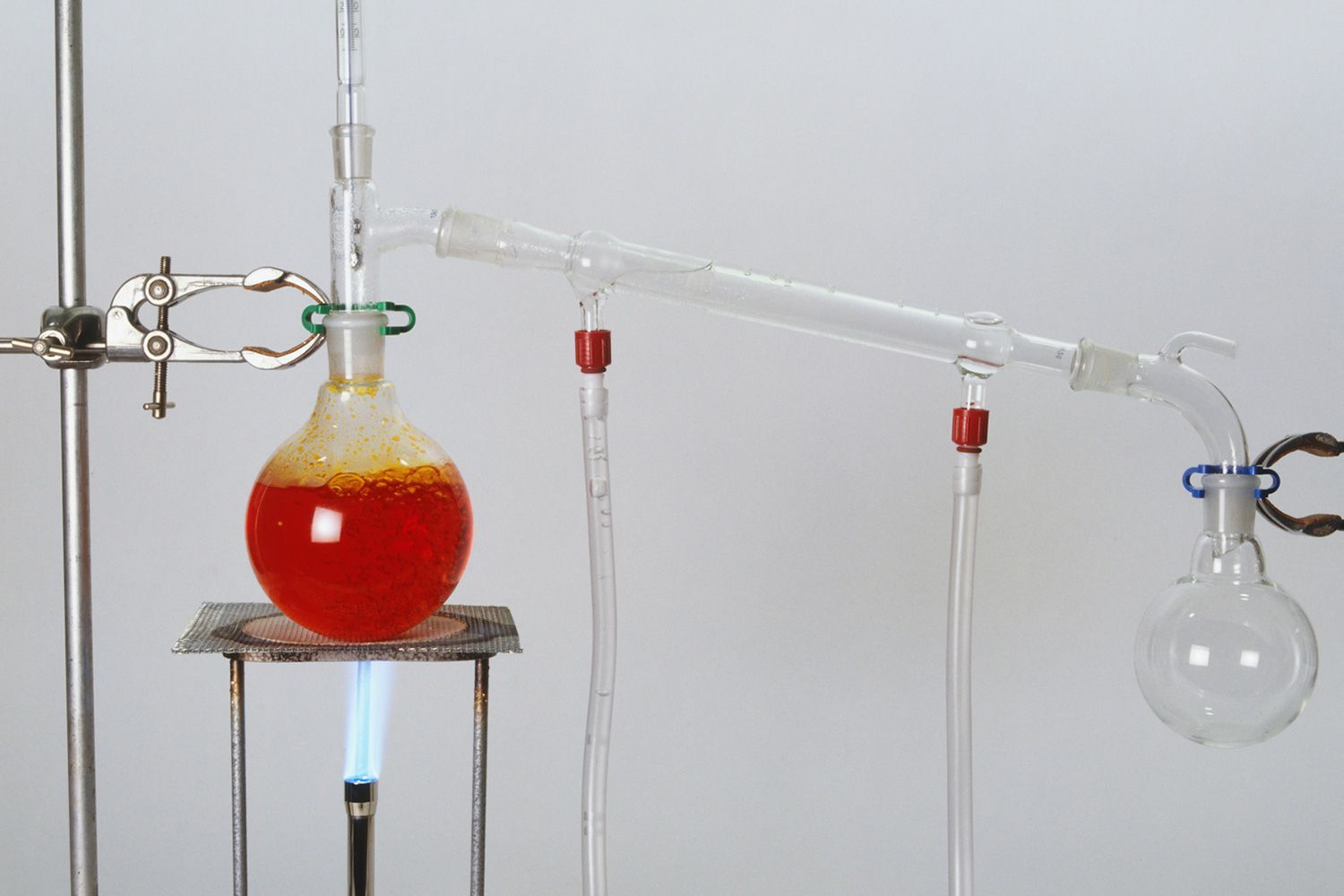
La destilación es un método ampliamente utilizado para separar mezclas basadas en diferencias en las condiciones requeridas para cambiar la fase de los componentes de la mezcla. Para separar una mezcla de líquidos, el líquido puede calentarse para forzar componentes, que tienen diferentes puntos de ebullición, a la fase gaseosa. A continuación, el gas se condensa de nuevo en forma líquida y se recoge. Repetir el proceso en el líquido recogido para mejorar la pureza del producto se denomina doble destilación. Aunque el término se aplica más comúnmente a líquidos, el proceso inverso se puede usar para separar gases licuando componentes usando cambios de temperatura y/o presión.
Lectura relacionada: ¿Cuál Es el Elemento Más Caro?
¿Cuál Es el Elemento Más Caro?
Una planta que realiza destilación se llama destilería. El aparato utilizado para realizar la destilación se llama todavía.
Historia
La evidencia más antigua conocida de destilación proviene de un aparato de destilación de terracota que data del año 3000 a.C. en el valle del Indo de Pakistán. Se sabía que la destilación era utilizada por los babilonios de Mesopotamia. Inicialmente, se cree que la destilación se usó para hacer perfumes. La destilación de bebidas se produjo mucho más tarde. El químico árabe Al-Kindi destiló alcohol en Irag del siglo IX. La destilación de bebidas alcohólicas parece común en Italia y China a partir del siglo XII.
Lectura relacionada: Qué Es La Vaselina? Composición Química
Qué Es La Vaselina? Composición Química
Usos de la Destilación
La destilación se utiliza para muchos procesos comerciales, como la producción de gasolina, agua destilada, xileno, alcohol, parafina, queroseno y muchos otros líquidos. El gas puede licuarse y separarse. Por ejemplo: el nitrógeno, el oxígeno y el argón se destilan del aire.
Lectura relacionada:
 ¿Cuáles Son las Tres Leyes del Movimiento de Newton?
¿Cuáles Son las Tres Leyes del Movimiento de Newton?Tipos de Destilación
Los tipos de destilación incluyen destilación simple, destilación fraccionada (se recogen diferentes "fracciones" volátiles a medida que se producen) y destilación destructiva (generalmente, un material se calienta para que se descomponga en compuestos para su recolección).
Destilación Simple
Se puede usar destilación simple cuando los puntos de ebullición de dos líquidos son significativamente diferentes entre sí o para separar líquidos de sólidos o componentes no volátiles. En la destilación simple, una mezcla se calienta para cambiar el componente más volátil de un líquido a vapor. El vapor se eleva y pasa a un condensador. Normalmente, el condensador se enfría (por ejemplo, haciendo correr agua fría a su alrededor) para promover la condensación del vapor, que se recoge.
Destilación al Vapor
La destilación al vapor se utiliza para separar componentes sensibles al calor. Se agrega vapor a la mezcla, lo que hace que parte de ella se vaporice. Este vapor se enfría y se condensa en dos fracciones líquidas. A veces, las fracciones se recogen por separado, o pueden tener diferentes valores de densidad, por lo que se separan por sí solas. Un ejemplo es la destilación al vapor de flores para producir aceite esencial y un destilado a base de agua.
Destilación Fraccionada
La destilación fraccionada se usa cuando los puntos de ebullición de los componentes de una mezcla están cercanos entre sí, como se determina usando la ley de Raoult. Se utiliza una columna de fraccionamiento para separar los componentes utilizados en una serie de destilaciones denominadas rectificación. En la destilación fraccionada, una mezcla se calienta para que el vapor suba y entre en la columna de fraccionamiento. A medida que el vapor se enfría, se condensa en el material de relleno de la columna. El calor del vapor ascendente hace que este líquido se vaporice de nuevo, moviéndolo a lo largo de la columna y, finalmente, produciendo una muestra de mayor pureza del componente más volátil de la mezcla.
Destilación al Vacío
La destilación al vacío se utiliza para separar componentes que tienen altos puntos de ebullición. La reducción de la presión del aparato también reduce los puntos de ebullición. De lo contrario, el proceso es similar a otras formas de destilación. La destilación al vacío es particularmente útil cuando el punto de ebullición normal excede la temperatura de descomposición de un compuesto.
Fuentes
- Allchin, F. R. (1979). "India: ¿El Antiguo Hogar de la Destilación?". Hombre. 14 (1): 55–63. doi:10.2307/2801640
- Forbes, R. J. (1970). Una breve Historia del Arte de la Destilación desde los Inicios hasta la muerte de Cellier Blumenthal. BRILL. ISBN 978-90-04-00617-1.
- Harwood, Laurence M.; Moody, Christopher J. (1989). Química orgánica experimental: Principios y Práctica (Ilustrado ed.). Oxford: Publicaciones científicas de Blackwell. ISBN 978-0-632-02017-1.